INTRODUCCIÓN
Los arrecifes coralinos son ecosistemas que se desarrollan y prosperan dentro de océanos oligotróficos tropicales y subtropicales (Nelson et al., 2011), siendo considerados dentro de los ecosistemas marino-costeros más productivos (Sorokin, 1993). Tanto en los arrecifes coralinos como en los otros sistemas marinos, el mayor flujo de energía es producto del acoplamiento pelágico-bentónico (Raffaelli et al., 2003). El papel principal en este ensamble lo desarrolla el zooplancton, el cual contribuye con el flujo de energía. Muchos de estos organismos realizan migraciones nictimerales (fenómeno o actividad que se repite en un periodo de 24 horas) y ontogénicas (durante su ciclo de vida), cubriendo toda la columna de agua y estableciendo una conexión entre la superficie y el fondo marino (Schnack-Schiel y Isla, 2005). Además, el zooplancton representa una parte importante de la dieta de varios organismos del arrecife de coral (Robichaux et al., 1981).
Además, los arrecifes coralinos son ecosistemas muy importantes en términos de recursos biológicos, con una elevada diversidad, siendo un banco genético de relevancia vital para usos actuales y futuros de la población humana del planeta. Su estructura tridimensional alberga muchos organismos de diferentes categorías (Crespo y Soares-Gomes, 2009). Están compuestos por una gran variedad de organismos bentónicos, cuyos ciclos de vida incluyen etapas larvales planctónicas como las larvas de invertebrados y peces, que enriquecen a su vez la estructura taxonómica y productividad de las comunidades de zooplancton en la vecindad de los arrecifes y contribuyen con el reabastecimiento de las poblaciones locales (Cowen y Castro, 1994; Esquivel-Garrote, 2015).
El zooplancton de los arrecifes de coral forma conjuntos complejos de diferentes fuentes: especies residentes del arrecife, demersales migratorias, parte del holoplancton de mar abierto transportado hacia el arrecife, y del meroplancton tanto del arrecife, ecosistemas adyacentes o del océano abierto (Heidelberg et al., 2004). Esta diversidad de especies le provee al ecosistema arrecifal un ingreso sustancial de alimento, tanto para los peces de arrecifes, los corales escleratinios, así como para otros invertebrados (Nakajima et al., 2009; Heidelberg et al., 2010).
En el holoplancton arrecifal, se caracteriza por abundancia en copépodos calanoides y ciclopoides, seguido de otros crustáceos como cladóceros, anfípodos y mísidos (Suárez-Morales y Rivera, 1998). Se ha señalado que, durante la noche, el zooplancton demersal se distribuye a través de la columna de agua y en el día se refugian en superficies porosas del arrecife como cascajo, arena y tallos de macrófitas (Alldredge y King, 1980; Esquivel-Garrote, 2015).
Para realizar estudios del zooplancton, las trampas de luz son métodos de captura pasivos, diseñados para poder llevar a cabo muestreos en diferentes tipos de ambientes marinos someros y poco profundos, como, por ejemplo, los arrecifes coralinos. Su principal ventaja es poder capturar especies selectivas, las cuales presentan respuestas a la luz, con ciertas habilidades natatorias y generalmente de mayores dimensiones a los colectados por las redes de arrastre (Doherty, 1987; Thorrold, 1993; Hickford y Schiel, 1999; Chang et al., 2016). Sin embargo, a través de este método no es posible cuantificar el volumen de agua muestreada, y a su vez las eficiencias de captura de este tipo de trampas se encuentran ampliamente influenciados por ciertos factores ambientales tales como las fases lunares, velocidad de corriente, turbidez y/o claridad (Doherty, 1987; Meekan et al., 2000; Lindquist y Shaw, 2005). Los principales factores que diferencian las trampas de luz con respecto a las redes de plancton, son la selectividad taxonómica de las larvas y la distribución de las tallas de los ejemplares colectados (Choat et al., 1993).
Algunos grupos zooplanctónicos reaccionan positivamente a la atracción de luz artificial (Meekan et al., 2001). Por ello, se han desarrollado las técnicas de trampas de luz como atrayentes nocturnos para el zooplancton (Kawagushi et al., 1986), dando un eficiente resultado con larvas de crustáceos decápodos (megalopas y zoeas). En ese sentido, se ha señalado que hay organismos demersales, asociados al fondo marino, tales como larvas de anfípodos y crustáceos cumáceos, que están más representados en las trampas de luz y generalmente no son capturados con las redes (Choat et al., 1993; Meekan et al., 2001).
En estudios de zooplancton en Venezuela la relación holoplancton y meroplancton es poco explotada en formaciones coralinas, y más aun empleando como método de captura las trampas de luz. De esta manera, se plantea como hipótesis que los factores ambientales asociados a las dos épocas del año (surgencia y relajación) características de la zona nororiental de Venezuela y bien establecidas en diferentes trabajos (Jury, 2017; Rueda-Roa et al., 2018), pudieran marcar cambios estacionales y espaciales en la abundancia y en la estructura comunitaria de dichas comunidades. Por ello, se plantea describir los principales cambios espaciotemporales de la abundancia y estructura comunitaria de la taxocenosis de tres grupos del holoplancton (Copepoda, Branchiopoda y Quetognatha) y tres del meroplancton (larvas de crustáceos, larvas de anélidos e ictioplancton) asociado a las formaciones coralinas en la ensenada de Turpialito.
MATERIALES Y MÉTODOS
Área de estudio
Este estudio se realizó en la ensenada de Turpialito, localizada en el golfo de Cariaco, estado Sucre, NE Venezuela (10°44’30’’N; 64°03’40’’W, Figura 1), a 13 km al este de la ciudad de Cumaná (Okuda et al., 1978). Es un cuerpo de agua somero conformado por dos ensenadas separadas por un pequeño promontorio de piedras y escasos corales y está protegida del oleaje por la península de Araya, caracterizada por cambios hidrológicos debido a la surgencia costera estacional que se produce en la región nororiental de Venezuela (Okuda et al., 1978; Quintero et al., 2005; Martínez et al., 2011).
La ensenada de Turpialito, está ubicada al este; es una playa arenosa de 46 m de longitud, que alberga una pradera de Thalassia testudinum de aproximadamente unos 10 m2, posee en sus extremos formaciones rocosas que se prolongan con formaciones coralinas que se extienden hasta aproximadamente 14 m de profundidad. La zona coralina presenta un sustrato arenoso, con predominio de partículas gruesas de diferentes tamaños y a medida que la profundidad aumenta los sedimentos se hacen más finos (Núñez et al., 2011).
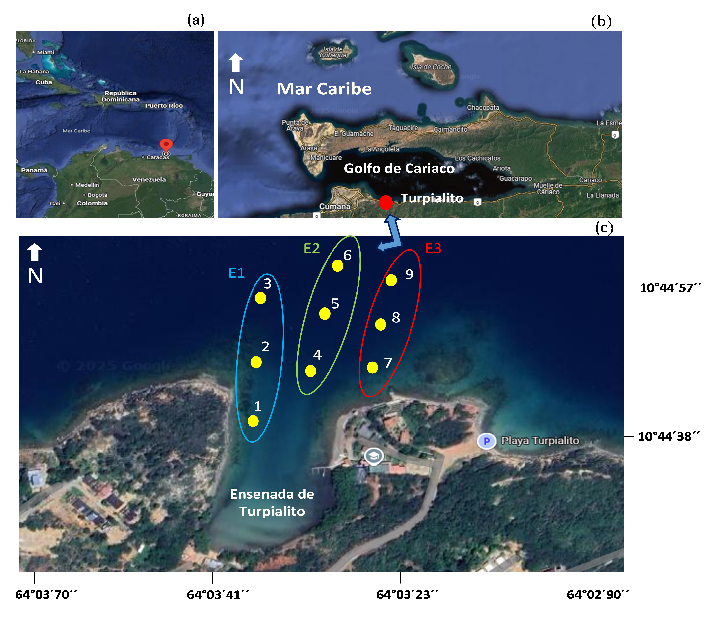 Figura 1
(a) Ubicación geográfica de Venezuela, (b) golfo de Cariaco y (c) ensenada de Turpialito, donde se indica la distribución de las estaciones de muestreo (Google Maps, 2023, 13 de noviembre 2023, https://www.google.es/maps).
Figura 1
(a) Ubicación geográfica de Venezuela, (b) golfo de Cariaco y (c) ensenada de Turpialito, donde se indica la distribución de las estaciones de muestreo (Google Maps, 2023, 13 de noviembre 2023, https://www.google.es/maps).
Se efectuaron muestreos mensuales durante seis meses, abarcando la época de surgencia (enero, febrero y marzo) y relajación (junio, julio y agosto) del año 2018. Dichos muestreos se realizaron entre las 6:00 p.m. a 6:00 a.m. Las muestras de zooplancton se colectaron utilizando trampas de luz, construidas con botellas de agua de 20 L, siguiendo el modelo de Riley y Holt (1993), utilizando lámparas con luces LED (diodos de emisión de luz) de 1 473 lux en promedio. Estas permitirán la captura selectiva de especies de forma pasiva, con mejor desempeño en aguas tranquilas y protegidas (Thorrold, 1993; Hickford y Schiel, 1999).
Para su elaboración, se utilizaron botellones de agua con un área basal de 225 cm2 y una altura de 35 cm, contentivas de cuatro aberturas verticales de aproximadamente 5 mm para permitir el ingreso de los organismos atraídos por una luz permanente colocada en el interior del botellón (Figura 2). Las trampas fueron colocadas en horas de la noche, durante un período de 12 horas a una profundidad entre 3-4 metros. Se establecieron tres estaciones, con tres réplicas, haciendo un total de 9 trampas mensuales (Figura 1). Las concentraciones se expresaron en CPUE (captura por unidad de esfuerzo), tomando el tiempo en horas de exposición de la trampa como unidad de esfuerzo (N° org/12h) de acuerdo con las recomendaciones de Thorrold (1993), Hickford y Schiel (1999) y Chan et al. (2016). Una vez trascurrido el tiempo, se procedió a filtrar las muestras de las trampas de luz mediante de un tamiz de 100 μm, se agregaron en envases plásticos (500 mL) previamente etiquetados, y se fijaron con formaldehído al 4% neutralizado con tetraborato de sodio (Postel et al., 2000). Las muestras se protegieron del ambiente hasta llevar al laboratorio.
En cada estación, se tomaron medidas de temperatura (°C) y salinidad (ppt) mediante una sonda multiparamétrica de calidad de agua (YSI incorporated) modelo 556mps. Se recolectaron muestras de agua superficial en botellas de polietileno (250 mL) para determinar la abundancia microalgal, las cuales se fijaron con formalina al 4 % neutralizada con hexametilentetramina (Sournia, 1978).
Paralelamente, se recolectaron muestras de agua en botellas de polietileno oscuras (2 L) para la clorofila a (Clor a) en la superficie, la cual se determinó según el método descrito por Lorenzen, modificado y mejorado por Parsons et al. (1984), utilizando un espectrofotómetro GENESYS 8 (ColeParmer, Vernon Hills, IL, EUA).
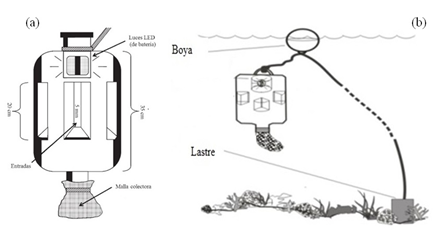 Figura 2
- (a) Modelo de trampa de luz empleada en la presente investigación, elaborada siguiendo las recomendaciones de Riley y Holt (1993) y (b) ubicación de las trampas de luz sobre los parches coralinos de la ensenada de Turpialito, Venezuela.
Figura 2
- (a) Modelo de trampa de luz empleada en la presente investigación, elaborada siguiendo las recomendaciones de Riley y Holt (1993) y (b) ubicación de las trampas de luz sobre los parches coralinos de la ensenada de Turpialito, Venezuela.
Para determinar la variabilidad estacional (surgencia y relajación) en la zona de estudio, se utilizaron las mediciones de las precipitaciones (mm), la velocidad y dirección del viento para posteriormente calcular el índice de surgencia (IS); estos datos fueron suministrados por el proyecto POWER del Centro de Investigación Langley de la NASA (https://power.larc.nasa.gov/). El índice de surgencia (IS) fue calculado por la fórmula IS = [tsx/ rw·f·] 100 (1); donde rw es la densidad del agua (cte)= 1025 kg·m-3; f= parámetro de coriolis (cte) =2w sen fin=2,64.10-7; tsx=fricción superficial del viento sería tsx = k ra·w2 (2), donde k= coeficiente empírico de dragado (cte)= 1.11(si w< 5) y 1.45 (si w>5); ra= densidad media del aire (cte)= 122·10-8 kg·cm-3; w= velocidad del viento (Bowden, 1983). Una vez obtenido los valores del IS, se multiplicaron por 1000 para facilitar la presentación gráfica e interpretación.
Para calcular la abundancia de los grupos holo y meroplanctónicos seleccionados, se tomaron tres alícuotas de 10 mL lo que representó el 10% del stock total de la muestra (300 mL). Para el conteo de cada una de las alícuotas, se empleó una cámara de Bogorov (9 ml: 80x50 mm) y un microscopio estereoscópico marca Motic. Para la ubicación taxonómica de los organismos se utilizaron las referencias de Smith (1977), Tregouboff y Rose (1978), Gasca y Suárez (1996) y Boltovskoy (1999).
La determinación de la abundancia microalgal se realizó según el método de sedimentación de Utermöhl descrito por Edler y Elbrächter (2010). Por problemas de logística no se realizó el muestreo en enero de la abundancia microalgal. La identificación del fitoplancton se hizo según los trabajos de Cupp (1943), Tomas (1997), Bérard-Thierrault et al. (1999) y Rivera-Tenenbaum (2006).
Análisis estadísticos
Para establecer las posibles diferencias entre los periodos climáticos con respecto a la abundancia de los grupos holoplanctónicos y meroplanctónicos se realizó la prueba de Mann-Whitney-U (W), mientras que para las estaciones se utilizó la prueba de Kruskal-Wallis (KW; Sheskin, 2004). En los casos de diferencias significativas se realizó la prueba a posteriori de Dunn para evaluar las diferencias en cada parámetro ambiental y la abundancia de los grupos planctónicos. Posteriormente, se realizaron figuras de cajas y bigotes, representados sin valores extremos (outliers), por medio del programa Statgraphics Plus versión 5.1.
Con el fin de conocer las posibles relaciones entre los grupos del holoplancton y meroplancton y las variables ambientales registradas, se efectuó un análisis de correspondencia canónica (ACC) (Ter Braak y Verdonshot, 1995), previa estandarización para cumplir con la linealidad y la normalidad del conjunto de datos. La matriz de disimilitud de Bray-Curtis se construyó a partir de los datos de abundancia de los grupos holo y meroplanctónicos transformados mediante raíz cuadrada (Zar, 1999). Este procedimiento permite posicionar los grupos zooplanctónicos con respecto al gradiente ambiental sintetizado a partir de las variables ambientales en un sistema de coordenadas (componentes 1 y 2). Para ello se empleó el software CANOCO 4.5 (Ter Braak y Smilauer, 2002).
RESULTADOS
Índice de surgencia (IS) y Precipitación
El nivel del IS durante enero y agosto del 2018 osciló entre 0,94 y 6,25 m3.s-1. 1000 m (Figura 3a). A partir de enero se observó un aumento progresivo de los registros hasta obtener los valores más altos en febrero ( = 4,18 m3.s-1. 1000 m). A inicios de marzo se registró una evidente disminución (1,03 m3.s-1. 1000 m) para luego conservar niveles sostenidos > 3,5 m3.s-1. 1000 m. El IS en abril y mayo se fortaleció con mayor constancia y medias de 4,26 y 4,47 m3.s-1. 1000 m, respectivamente, a diferencia de junio donde se observó mayor fluctuación de este índice, con valores relativamente bajos (2,20 - 4,99 m3.s-1. 1000 m), incluso se registró el valor más bajo de todo el estudio (0,94 m3.s-1. 1000 m; Figura 3a).
Los valores de lluvia acumulada entre enero y agosto del 2018 fluctuaron entre 0,80 y 10,80 mm ( = 3,64 mm; Figura 3b). Durante los cuatro primeros meses del estudio las precipitaciones fueron escasas (< 3 mm); en mayo se registraron precipitaciones con valores de 8,50 mm, mientras que en agosto se cuantificó los valores más altos de lluvias en todo el estudio (10,80 mm; Figura 3b).
Variables abióticas
La temperatura superficial del agua fluctuó entre 22,9 y 26,3ºC, con una media de 24,3ºC (Figura 4a), se registraron diferencias temporales significativas (KW = 34,48; p <0,05). La prueba de Dunn genero 15 pares de subgrupos, entre los cuales solo se observaron diferencias estadísticas de la temperatura entre enero y marzo (Dunn= 2,95, p= 0,047), enero y junio (Dunn= 3,33, p= 0,013), febrero y agosto (Dunn= 4,04, p= 0,0001), marzo y agosto (Dunn= 4,30, p= 0,0001), y junio y agosto (Dunn= 4,68, p= 0,0001). No se hallaron diferencias significativas en la temperatura en relación con las estaciones (KW = 1,82, p > 0,05) y períodos (W = 1,08; p > 0,05, Figura 4b).
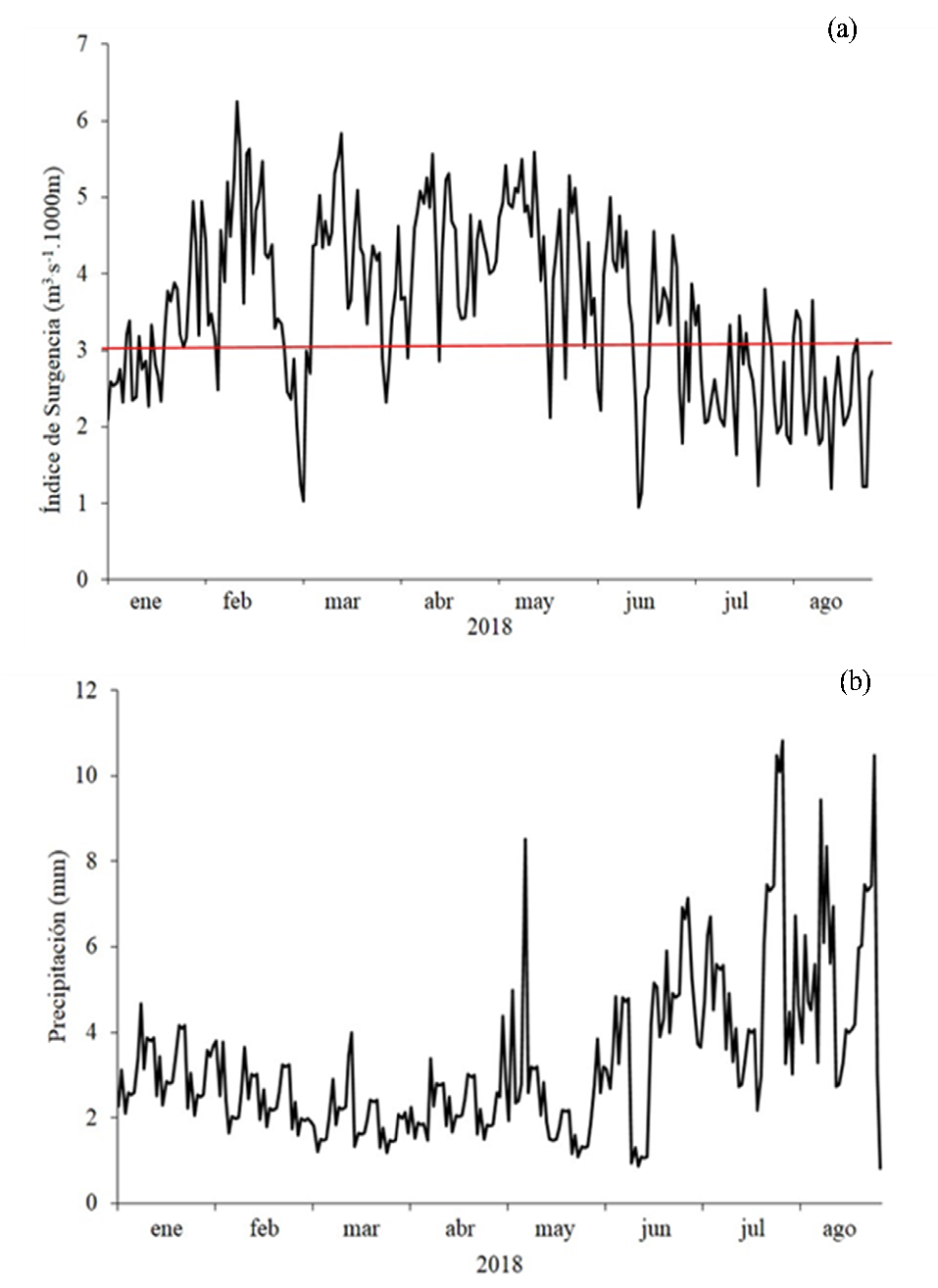 Figura 3
- (a) Variación mensual del índice de surgencia (m3.s-1. 1000 m) y (b) Variación mensual de la precipitación (mm) en la ensenada de Turpialito, estado Sucre, Venezuela. La línea roja define los meses de surgencia con valores del IS 3 m3.s-1. 1000 m.
Figura 3
- (a) Variación mensual del índice de surgencia (m3.s-1. 1000 m) y (b) Variación mensual de la precipitación (mm) en la ensenada de Turpialito, estado Sucre, Venezuela. La línea roja define los meses de surgencia con valores del IS 3 m3.s-1. 1000 m.
Figura 3.- (a) Variación mensual del índice de surgencia (m3.s-1. 1000 m) y (b) Variación mensual de la precipitación (mm) en la ensenada de Turpialito, estado Sucre, Venezuela. La línea roja define los meses de surgencia con valores del IS > 3 m3.s-1. 1000 m.
La salinidad osciló entre 33,8 y 35,1 ppt con una media de 34,6 ppt, Se detectaron diferencias significativas con respecto al tiempo (KW = 24,77, p < 0,05, Figura 4c). La prueba de Dunn generó 15 pares de subgrupos, entre los cuales solo se observaron diferencias estadísticas de la salinidad entre enero y marzo (Dunn= 3,74, p= 0,003), enero y agosto (Dunn= -3,18, p= 0,027) y febrero y marzo (Dunn= 3,46, p= 0,008). Por estaciones, no observaron diferencias significativas (KW = 5,07, p > 0,05); no obstante, por períodos también se detectaron diferencias significativas (W = 4,31, p < 0,05, Figura 4d), registrándose en surgencia los valores más bajos.
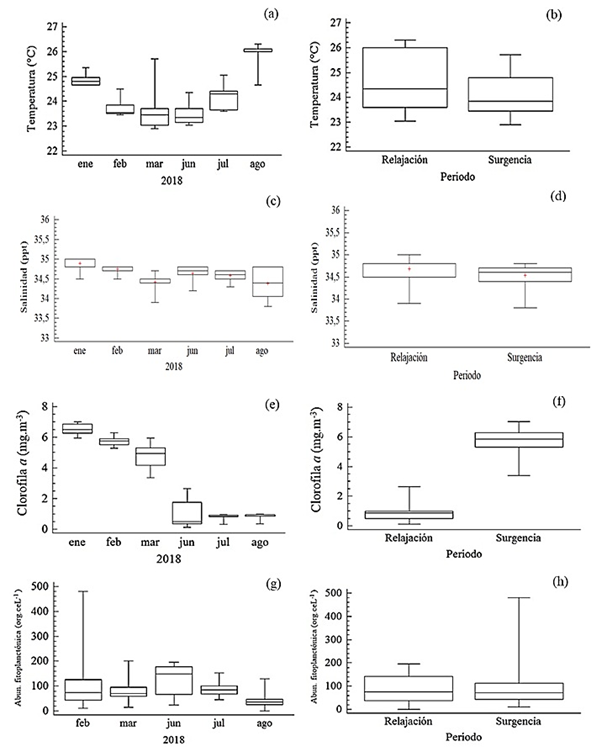 Figura 4
Variación temporal y por periodos climáticos de la temperatura superficial del agua (a,b), de la salinidad (c,d), de la Clorofila a (e,f) y de la abundancia fitoplanctónica en la ensenada de Turpialito, golfo de Cariaco, durante el periodo de muestreo en el 2018.
Figura 4
Variación temporal y por periodos climáticos de la temperatura superficial del agua (a,b), de la salinidad (c,d), de la Clorofila a (e,f) y de la abundancia fitoplanctónica en la ensenada de Turpialito, golfo de Cariaco, durante el periodo de muestreo en el 2018.
Variables bióticas
La concentración de clorofila a (Clor a) varió entre 0,11 y 7,01 mg.m-3 con una media de 3,28 mg.m-3. Se detectaron diferencias significativas con respecto a los meses (KW = 4,62, p < 0,05, Figura 4e). Durante los tres primeros meses se registraron las concentraciones más elevadas para el sector ( = 5,76 – 4,78 mg.m-3), reportando el valor más alto en enero ( = 6,54 mg.m-3). En los meses sucesivos disminuyó marcadamente la concentración de Clor a hasta llegar a los valores más bajos en julio ( = 0,81 mg.m-3) y agosto ( = 0,84 mg.m-3). La prueba de Dunn generó 15 pares de subgrupos, entre los cuales solo se observaron diferencias estadísticas de la concentración de Clor a entre enero y junio (Dunn= 4,92; p= 0,0001), enero y julio (Dunn= 4,83; p= 0,0001), enero y agosto (Dunn= 4,61; p= 0,0001), febrero y junio (Dunn= 3,65; p= 0,004), febrero y julio (Dunn= 3,56; p= 0,006), febrero y agosto (Dunn= -3,33; p= 0,013). Esta variable no presentó diferencias significativas con respecto a las estaciones (KW = 0,06, p > 0,05). En cambio, en esta variable sí se encontró diferencias estadísticamente significativas entre los periodos estudiados (W = 3,67, p < 0,05, Figura 4f).
La abundancia fitoplanctónica varió entre 0 y 479,5 cel.mL-1, con una media de 93,7 cel.mL-1. No se observaron diferencias significativas mensuales (KW = 9,15, p >0,05; Figura 4g), ni entre las estaciones (KW = 0,06, p > 0,05). A diferencia de los períodos, que si se detectaron diferencias estadísticamente significativas (W = 0,54, p <0,05, Figura 4h), registrándose mayor abundancia fitoplanctónica durante el período de surgencia (479,5 cel.mL-1).
El zooplancton estuvo constituido por 22 grupos taxonómicos. La abundancia zooplanctónica varió entre 433 y 13.5214 org/12 horas ( = 14.295 org/12 horas). Esta variable presentó diferencias significativas con respecto a los meses (KW = 19,09, p < 0,05). Las mayores capturas de organismos se registraron en enero ( = 31.910 org/12 horas), y en febrero ( = 15.706 org/12 horas); posteriormente se evidenció un descenso en los valores, detectándose en marzo el valor más bajo ( = 2.541 org/12 horas). En junio y julio se registraron valores de abundancia promedio de 13.080 y 3.391 org/12 horas, respectivamente. En agosto se contabilizó un ligero incremento ( = 21.101 org/12 horas, Figura 5a). La prueba de Dunn genero 15 pares de subgrupos, entre los cuales solamente se observaron diferencias estadísticas de la abundancia zooplanctónica entre marzo y agosto (Dunn= 3,13, p= 0,026). No se detectaron diferencias significativas entre las estaciones (KW = 0,18, p > 0,05), ni entre épocas (W = 0,77, p > 0,05, Figura 5b).
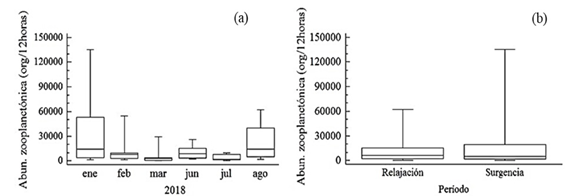 Figura 5
- Variación temporal (a) y por períodos climáticos (b) de la abundancia zooplanctónica (org/12 horas) en la ensenada de Turpialito, golfo de Cariaco, durante el periodo de muestreo en el 2018.
Figura 5
- Variación temporal (a) y por períodos climáticos (b) de la abundancia zooplanctónica (org/12 horas) en la ensenada de Turpialito, golfo de Cariaco, durante el periodo de muestreo en el 2018.
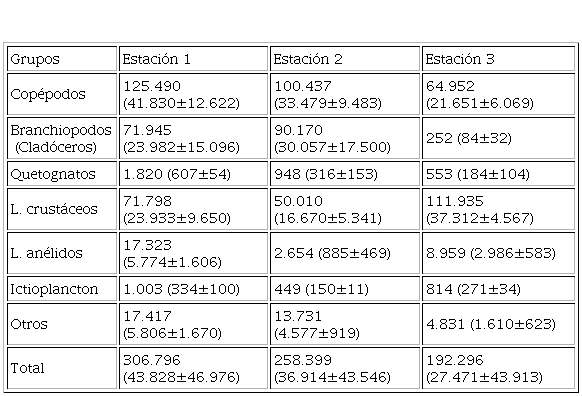
La abundancia zooplanctónica total y por grupos en las estaciones estudiadas en la ensenada de Turpialito osciló entre 19.2296 y 30.6796 org/12 horas (Tabla 1), destacando la estación 1 con la mayor abundancia de organismos en todo el estudio (306.796 org/12 horas) y la menor correspondió a la estación 3 (192.296 org/12 horas). En la estación 1 y 2 los copépodos fueron los más abundantes con 125.490 org/12 horas y 100.437 org/12 horas, respectivamente. En estas estaciones el segundo lugar lo ocuparon los branchiopodos con 71.945 y 90.170 org/12 horas, respectivamente.
Tabla 1. Abundancia total del zooplancton capturados con las trampas de luz (org/12 horas), promedio y desviación estándar en las estaciones de muestreo en la ensenada de Turpialito durante el 2018.
Tabla 1
Abundancia total del zooplancton capturados con las trampas de luz (org/12 horas), promedio y desviación estándar en las estaciones de muestreo en la ensenada de Turpialito durante el 2018.
| Grupos | Estación 1 | Estación 2 | Estación 3 |
| Copépodos | 125.490 (41.830±12.622) | 100.437 (33.479±9.483) | 64.952 (21.651±6.069) |
| Branchiopodos (Cladóceros) | 71.945 (23.982±15.096) | 90.170 (30.057±17.500) | 252 (84±32) |
| Quetognatos | 1.820 (607±54) | 948 (316±153) | 553 (184±104) |
| L. crustáceos | 71.798 (23.933±9.650) | 50.010 (16.670±5.341) | 111.935 (37.312±4.567) |
| L. anélidos | 17.323 (5.774±1.606) | 2.654 (885±469) | 8.959 (2.986±583) |
| Ictioplancton | 1.003 (334±100) | 449 (150±11) | 814 (271±34) |
| Otros | 17.417 (5.806±1.670) | 13.731 (4.577±919) | 4.831 (1.610±623) |
| Total | 306.796 (43.828±46.976) | 258.399 (36.914±43.546) | 192.296 (27.471±43.913) |
La estación 3 no reflejó el mismo comportamiento de las estaciones 1 y 2; el grupo con mayor captura correspondió a las larvas de crustáceos con 111.935 org/12 horas, seguido por los copépodos (64.952 org/12 horas). En esta estación los branchiopodos fueron los organismos menos abundantes (252 org/12 horas). En relación con el ictioplancton las estaciones 1 y 3 fueron las que registraron las mayores capturas con 1.003 y 814 org/12 horas, respectivamente (Tabla 1).
Relación Holoplancton-Meroplancton
La fluctuación del holoplancton y meroplancton durante el periodo de estudio estuvo dominada por el holoplancton (Figura 6a). En enero, el holoplancton fue mucho mayor que el meroplancton (218.475 org/12 horas), en febrero, marzo, junio y julio predominó el meroplancton ( = 79.983, 16.551, 74.214 y 17.550 org/12 horas, respectivamente), en agosto, al igual que en enero, fue más abundante el holoplancton (132.956 org/12 horas). Con respecto a las tres estaciones analizadas en este estudio, el holoplancton sobresalió en las estaciones 1 y 2 ( =204.647 y 198.234 org/12 horas, respectivamente); mientras en la estación 3, el meroplancton fue más abundante ( = 121.978 org/12 horas, Figura 6b). En relación con los períodos estudiados, el holoplancton fue el más abundante en surgencia ( = 285.051 org/12 horas) que en relajación ( = 185.304 org/12 horas, Figura 6c).
Grupos del Holoplancton
Dentro de los principales grupos taxonómicos del holoplancton en la bahía de Turpialito, predominaron los copépodos, branchiopodos (cladóceros) y quetognatos. Los copépodos fueron los organismos que dominaron en todo el estudio; la mayor abundancia (135.66 org/12 hora) se reportó en agosto y la mínima (58 org/12 horas) en julio; los promedios de abundancia más elevados se hallaron en enero, febrero y agosto ( = 8.738, 5.837 y 12.396 org/12 horas, respectivamente). Se hallaron diferencias significativas con respecto a los meses (KW = 19,70, p < 0,05), mientras que con las estaciones (KW = 0,30, p > 0,05) y por periodos (W = 0,76, p > 0,05, Figura 7a) no se observaron diferencias. La prueba de Dunn generó 15 pares de subgrupos, entre los cuales solo se observaron diferencias estadísticas en la abundancia de los copépodos entre marzo y agosto (Dunn= 3,53, p= 0,006) y entre julio y agosto (Dunn= 2,99, p= 0,042).
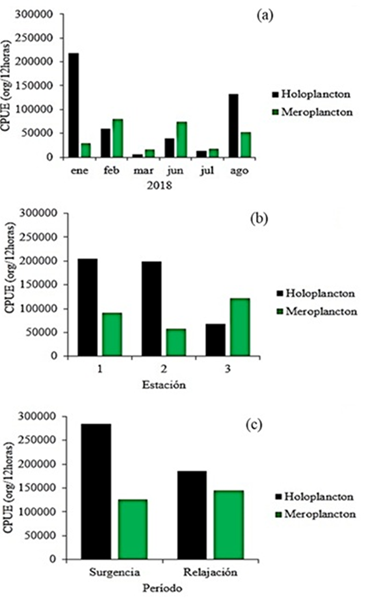 Figura 6
Relación holoplacton-meroplancton de los organismos colectados en la ensenada de Turpialito, en función a los meses (A), estación (B) y periodo (C), durante el periodo de muestreo en el 2018.
Figura 6
Relación holoplacton-meroplancton de los organismos colectados en la ensenada de Turpialito, en función a los meses (A), estación (B) y periodo (C), durante el periodo de muestreo en el 2018.
Los branchiopoda siguieron en abundancia, con magnitudes elevadas en enero (23.429 org/12 horas), y en agosto con un ligero aumento (2.782 org/12 horas; Fig. 7b), no presentaron diferencias significativas temporales (KW = 6,61, p >0,05), espaciales (KW = 0,56, p > 0,05), ni por período (W = 1,21, p > 0,05). Los quetognatos constituyeron el tercer grupo en abundancia dentro del holoplancton, registrando valores de máxima abundancia en junio y agosto (= 185 y 244 CPUE org/12 horas, Figura 7c), mientras que el mínimo de observó en enero (38 org/12horas). No hubo diferencias significativas temporales (KW = 8,07, p >0,05), espaciales (KW = 0,58, p > 0,05), ni por periodo (W = 0,93, p > 0,05).
Grupos del Meroplancton
El meroplancton, estuvo representado por larvas de crustáceos, larvas de anélidos e ictioplancton. Dentro de las larvas de crustáceos se agruparon las etapas tempranas (zoea) y posteriores (megalopa) de crustáceos decápodos, constituyendo un grupo amplio de larvas de crustáceos. Este grupo de crustáceos fueron los más abundantes (Figura 7d); en marzo se obtuvo la menor abundancia (129 org/12 horas), a diferencia de las magnitudes en febrero y junio, cuando se registraron dos picos de abundancia (11.168 y 7.889 org/12 horas, respectivamente, Figura 7d), sin embargo, no se hallaron diferencias significativas con respecto a los meses (KW = 10,5, p > 0,05), ni el periodo (W = 1,05, p > 0,05). En contraste se detectaron diferencias significativas en relación a las estaciones (KW = 2,64, p < 0,05), contabilizándose mayor abundancia de larvas de crustáceos en la estación 3 ( = 6.584 org/12 horas). A este grupo, le siguieron las larvas de anélidos, con máxima abundancia al principio del estudio, principalmente en enero y febrero (839 y 1.010 CPUE org/12 horas, respectivamente; Figura 7e), mientras que en julio se observó la menor abundancia (38 org/12horas); no hubo diferencias significativas en estos organismos en cuanto a los meses (KW = 3,07, p > 0,05), las estaciones (KW = 0,17, p > 0,05), ni al periodo (W = 1,08, p > 0,05). Finalmente el ictioplancton, constituido por huevos y larvas de peces, cuyo mínimo de abundancia se registró en enero (3 org/12 horas), mientras que las mayores abundancias se detectaron en febrero y agosto (105 y 77 org/12 horas, respectivamente, Figura 7f); en este grupo no hubo diferencias con respecto a las estaciones (KW = 0,55, p > 0,05), pero si presentaron diferencias entre los meses (KW = 27,63, p < 0,05) y el periodo (W = 1,61; p < 0,05), con la mayor captura en la época de relajación ( = 48 CPUE org/12 horas).
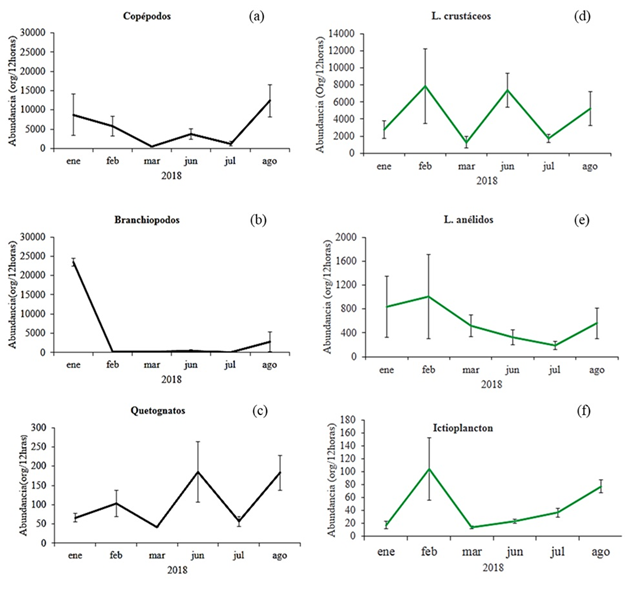 Figura 7
Abundancia de organismos holoplanctónicos (a: larva de crustáceos, b: larvas de anélidos y c: ictioplancton) y organismos meroplanctónicos (d: larvas de crustáceos, e: larvas de anélidos y f: ictioplancton) capturados con trampas de luz en la ensenada de Turpialito, golfo de Cariaco, durante el periodo de muestreo en el 2018. La línea negra representa los organismos holoplanctónicos y la línea verde los organismos meroplanctónicos.
Figura 7
Abundancia de organismos holoplanctónicos (a: larva de crustáceos, b: larvas de anélidos y c: ictioplancton) y organismos meroplanctónicos (d: larvas de crustáceos, e: larvas de anélidos y f: ictioplancton) capturados con trampas de luz en la ensenada de Turpialito, golfo de Cariaco, durante el periodo de muestreo en el 2018. La línea negra representa los organismos holoplanctónicos y la línea verde los organismos meroplanctónicos.
Riqueza, equidad y diversidad mensual del zooplancton
La diversidad y equidad durante los meses del estudio variaron entre 2,59 y 4,46 bits.ind-1 y 0,48 a 0,76, respectivamente, mientras la riqueza de grupos varió entre 6 y 22 (Figura 8). La diversidad mensual presentó valores altos en junio y agosto (4,25 y 4,46 bits.ind-1, respectivamente) y el más bajo se registró en marzo (2,59 bits.ind-1); no obstante, la equidad mostró el valor más alto en marzo (0,76) y los más bajos en febrero y agosto (0,49 y 0,48). Durante los últimos tres meses del estudio, se registraron los máximos valores de riqueza (19, 17 y 22, respectivamente). En marzo se obtuvo el valor más bajo de la riqueza, con seis grupos zooplanctónicos (Figura 8).
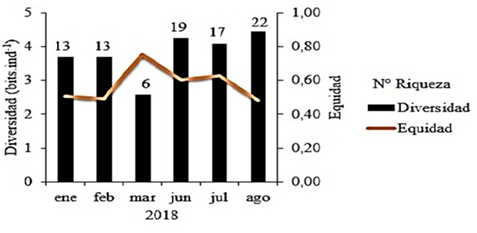 Figura 8
Variación temporal de la diversidad (bits.ind-1), equidad y riqueza de los organismos capturados con trampas de luz en la ensenada de Turpialito, golfo de Cariaco, Venezuela.
Figura 8
Variación temporal de la diversidad (bits.ind-1), equidad y riqueza de los organismos capturados con trampas de luz en la ensenada de Turpialito, golfo de Cariaco, Venezuela.
Correspondencia canónica
El ACC de la temporada de surgencia mostró la correlación biológica ambiental de 0,75 en el primer componente y 0,24 en el segundo componente, totalizando 94% en los dos primeros componentes. En el primer componente se estableció correlación positiva entre copépodos (Copep), branchiópodos (Branch) y anélidos (Anel) con la Clorofila a (Chla), y estos en forma negativa con la salinidad (Sal). Mientras en el segundo componente se relacionaron en forma negativa la temperatura (Temp) y abundancia fitoplanctónica (Abfito, Figura 9a).
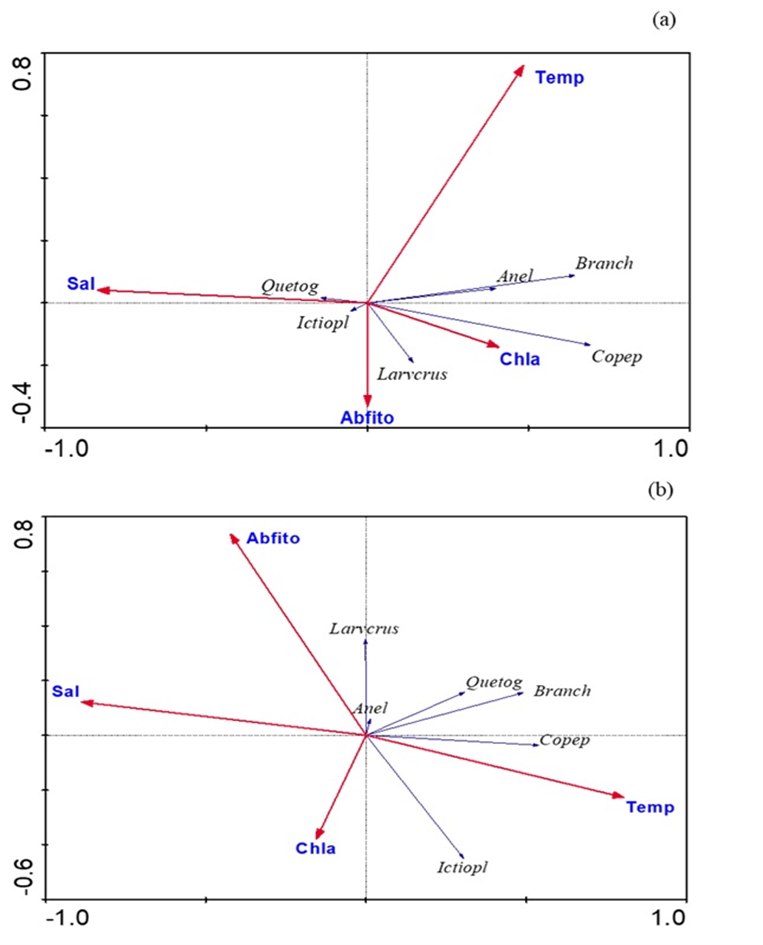 Figura 9
Proyección ortogonal de los dos primeros componentes del análisis de correspondencia canónica en la ensenada de Turpialito, Venezuela, (a) durante la temporada de surgencia (enero, febrero y marzo) y (b) relajación (junio, julio y agosto). Las flechas rojas corresponden a las variables ambientales y las flechas azules a los grupos planctónicos estudiados.
Figura 9
Proyección ortogonal de los dos primeros componentes del análisis de correspondencia canónica en la ensenada de Turpialito, Venezuela, (a) durante la temporada de surgencia (enero, febrero y marzo) y (b) relajación (junio, julio y agosto). Las flechas rojas corresponden a las variables ambientales y las flechas azules a los grupos planctónicos estudiados.
Figura 9. Proyección ortogonal de los dos primeros componentes del análisis de correspondencia canónica en la ensenada de Turpialito, Venezuela, (a) durante la temporada de surgencia (enero, febrero y marzo) y (b) relajación (junio, julio y agosto). Las flechas rojas corresponden a las variables ambientales y las flechas azules a los grupos planctónicos estudiados.
Durante la relajación, el ACC mostró la relación biológica ambiental de 0,80 en el primer componente y 0,17 en el segundo componente, sumando 97,1% en los dos primeros componentes. En el componente 1, se relacionaron los quetognatos (Quetog), copépodos (Copep) y branquiópodos (Branch) con la temperatura (Temp), y a su vez en forma negativa con la salinidad (Sal). Mientras que en el componente 2, la relación negativa entre abundancia de fitoplancton (Abfito) con la clorofila a (Chla), que se relacionan con el ictioplancton (Ictiopl, Figura 9b).
DISCUSIÓN
La costa nororiental venezolana está sujeta al fenómeno de surgencia costera estacional (Alvera-Azcárate et al., 2011; Jury, 2017; Rueda-Roa et al., 2018) quienes señalan que este fenómeno ocurre en un periodo comprendido entre diciembre/abril para el golfo de Cariaco y áreas adyacentes, asociándolo con una serie de cambios en las condiciones físico-químicas del agua que caracterizan dicho fenómeno, que coincide con lo registrado en el presente estudio; febrero y marzo registró la temperatura más baja, elevados valores en el índice de surgencia y bajas precipitaciones. Mientras en julio y agosto, coincidió con la época de relajación o de lluvias, con la temperatura más alta, menor intensidad de los vientos y fuertes precipitaciones. Resultados similares fueron reportados por Blanco et al. (2016) en su estudio de los foraminíferos en la ensenada de Turpialito, presentando el mismo patrón de variación de la temperatura y del índice de surgencia. De igual forma, Serrano-Zabala et al. (2020) para la misma ensenada registro los valores más bajos de temperatura (< 24°) durante los primeros meses de su estudio (enero – marzo).
Se detectó variabilidad marcada de la salinidad entre los dos periodos de muestreo. Estos resultados no concuerdan con los datos históricos de las condiciones hidrográficas en el golfo de Cariaco (Gade, 1961; Rao y Urosa, 1974). Además, los resultados obtenidos en la presente investigación no coinciden con el patrón típico de valores altos de salinidad durante el período de surgencia. Estas diferencias podrían deberse a que en la costa sur del golfo de Cariaco, desembocan 34 cursos de agua, con caudales anchos y de largo recorrido (Quintero et al., 2005; Martínez et al., 2011), aunado a que la ensenada de Turpialito, está rodeada de una zona urbana con casas, la cual vierte el agua producto de la actividad humana directamente a la bahía, además de posibles escorrentía originada por riachuelos cercanos (Calvo-Trujillo et al., 2015; Blanco et al., 2016; Serrano-Zabala et al., 2020). Las asociaciones observadas en los ACC de las trampas zooplanctónicas se corresponden con lo esperado en los periodos climatológicos muestreados, siendo típico el ascenso de aguas más salinas con menor temperatura en la época de surgencia con baja abundancia fitoplanctónica producto del efecto de crecimiento y pastoreo por parte de los organismos holoplanctónicos, principalmente copépodos y branchiopodos, tal y como fueron observados sus máximas abundancias a inicios de los meses de muestreo.
Los mayores valores de clorofila a y abundancia fitoplanctónica, se obtuvieron en el periodo de surgencia costera. Diversos autores (Margalef, 1965; Soto et al., 2015) indicaron que la surgencia es la principal fuente de nutrientes a la capa eufótica, lo que explicaría la alta productividad biológica del golfo de Cariaco. Durante el periodo de relajación las concentraciones de clorofila a descendieron de manera progresiva, concordando con el estudio de Marín et al. (2004) y Márquez-Rojas et al. (2011) en dicho golfo. No obstante, es importante mencionar que los valores de clorofila a y abundancia fitoplanctónica fueron muy bajos, cuando se comparan con otros estudios en la época de surgencia [Márquez-Rojas et al. (2016): 21 - 13726 org.mL-1 y Calvo-Trujillo et al. (2018): 24 – 1847 org.mL-1]. Estas diferencias en cuanto a las magnitudes pueden ser atribuidas a la biomasa autotrófica por sí misma, la radiación solar, temperatura, procesos horizontales y verticales, el viento como fuente de mezcla y transporte vertical de nutrientes, historia de vida y distribución taxonómica del fitoplancton (Platt y Sathyendranath, 1999; Espinosa-Carreón y Valdez-Holguin, 2007).
La abundancia zooplanctónica en la bahía de Turpialito no mostró un claro patrón de estacionalidad. Sin embargo, la mayor captura (CPUE) del zooplancton se registró en la época de surgencia, al igual que lo reportado por Brito (2013). Las altas abundancias registradas en enero y febrero pueden estar asociada con el fenómeno de surgencia costera, característica de la zona nororiental de Venezuela, inducido por los vientos alisios, los cuales propician el ascenso de aguas subsuperficiales ricas en nutrientes (Jury, 2017; Rueda-Roa et al., 2018) durante el primer semestre del año, incrementando la abundancia y biomasa planctónica (Ferraz-Reyes, 1989). La abundancia zooplanctónica capturada con trampas de luz en la ensenada de Turpialito fue alta (433 - 135214 org/12 horas) cuando se compara con el trabajo de Brito (2013) realizado en las formaciones coralinas de la bahía de Mochima, Venezuela, empleando el mismo método de captura, donde él reporto valores entre 539 - 33018 org/12 horas.
A diferencia de la abundancia, se encontró mayor diversidad en la época de relajación. En ese sentido, está bien documentado que en esta época se incrementa el número de especies (Da Costa et al., 2011; Márquez-Rojas et al., 2017). Además, las precipitaciones tienden a proporcionar nutrientes y materia orgánica (Quintero et al., 2005), producto de las escorrentías, las cuales permiten condiciones y alimentos que pueden ser aprovechados por los organismos zooplanctónicos. Para tener referencia con los valores de diversidad en la zona, se pueden mencionar los trabajos Figueroa (2002) en la misma ensenada de Turpialito (1,70 - 2,78 bits.ind-1) y Márquez-Rojas et al. (2017) en el golfo de Cariaco (1,36 - 2,85 bits.ind-1). Estas diferencias de valores más altos de diversidad en la presente investigación en relación con otros estudios, podrían estar relacionadas con el método de captura empleado, ya que en los trabajos mencionados anteriormente emplearon redes estándar de zooplancton. Con las trampas de luz hay mayor cantidad de horas de exposición (10-12 horas), adicionalmente se le incorpora luz, la cual atrae organismos con fototactismo positivo (Moriarty et al., 2021).
Al considerar la variabilidad espacial de la abundancia zooplanctónica, la estación 1 destaco con la mayor cantidad de organismos en todo el estudio, con mayor predominio de organismos holoplanctónicos. Esta mayor abundancia se debió posiblemente a la ubicación de esta estación, la cual está situada en el sector occidental, con las menores profundidades (2-3 metros) del estudio, caracterizada por la presencia de litoral rocoso y aislados parches de coral. La estación 2, reportó valores similares a la estación 1 en holoplancton; en esta localidad predomina el fondo arenoso con praderas de Thalassia testudinum, con profundidades inferiores a los 4 m, mientras que la mayor abundancia de meroplancton se alcanzó en la estación 3, liderado por las larvas de crustáceos y secundados por las larvas de anélidos, pudo ser debido a la mayor profundidad (> 5 metros), aunado a una zona amplia de fondo rocoso y la mayor extensión de parches de coral de la ensenada. Esto último coincide con Goldstein et al. (2016) y Sponaugle et al. (2021) quienes indicaron que las poblaciones de organismos marinos bentónicos que producen larvas pelágicas (meroplancton) son más abundantes en sitios de arrecifes menos profundos (< 10 m) en relación con las mayores profundidades (20-30 m), además las crías recién desovadas deberían ser más abundantes cerca de estas poblaciones adultas. Sin embargo, son necesario más estudios en el área, así como zonas con mayor profundidad para confirmar lo anterior.
El grado de interacción biológica entre los grupos de zooplancton en la ensenada de Turpialito puede ser una respuesta a las interacciones con los ecosistemas vecinos, como por ejemplo praderas de Thalassia testudinum y el litoral rocoso, lo que probablemente refleja la diferencia entre las estaciones estudiadas. En la estación 3, se registró mayor abundancia de meroplancton, especialmente larvas de crustáceos, larvas de anélidos e ictioplancton, corroborando su afinidad con la mayor extensión de parches coralinos de la ensenada. Por lo que estos resultados, sugieren que el zooplancton de la bahía de Turpialito corresponde más a un zooplancton pelágico que a un zooplancton demersal.
Los resultados obtenidos dentro de la relación holoplancton-meroplancton en la ensenada de Turpialito, sugieren la dominancia del holoplancton tanto a nivel temporal como espacial, coincide con lo reportado por Márquez et al. (2017) en el golfo de Cariaco. Esto también concuerda con Morales y Murillo (1996) y Carrillo-Baltodano y Morales-Ramírez (2016) en Costa Rica donde reportaron mayor concentración de organismos holoplanctónicos. A diferencia de los resultados obtenidos por Santos et al. (2019) para los arrecifes de coral brasileños y Sponaugle et al. (2021) en los cayos de la Florida, empleando trampas de luz, donde encontraron mayor predominio de meroplancton. A su vez, Sponaugle et al. (2021) sugieren que la proporción de meroplancton en cualquier sitio puede ser muy variable debido a los patrones reproductivos periódicos de diferentes taxones. Además, estos autores también indicaron que el meroplancton y el plancton demersal fueron significativamente más abundantes en los arrecifes de coral de plataforma poco profundos, desempeñan un papel fundamental en la reposición de diversos organismos marinos bentónicos.
Dentro de los taxones del holoplancton estudiados, los copépodos fueron los más abundantes durante todo el estudio, con porcentajes del 41%, 39% y 34% en orden con las estaciones. Estos porcentajes han sido mencionados por Márquez-Rojas et al. (2011, 2016, 2017, 2020) y Márquez-Rojas y Zoppi (2023) para el golfo de Cariaco. Los branchiopodos (Cladóceros) los secundaron, se identificó a Pseudoevadne tergestina y Penilia avirostris; sin embargo, difiere con el trabajo de Brito (2013) realizado en las formaciones coralinas de la bahía de Mochima, Venezuela, empleando el mismo método de captura, donde reporto a los copépodos calanoides, larvas de brachiura y otras larvas de crustáceos, como los principales grupos con frecuencia de aparición, asociando a estos pequeños crustáceos como buenos indicadores a reaccionar a la atracción de la luz. Los quetognatos ocuparon el tercer lugar dentro del holoplancton. Sin embargo, estos resultados difieren de Sponaugle et al. (2021) en las muestras de trampas de luz en los cayos de la Florida, donde ocuparon el sexto lugar en abundancia sobre la plataforma profunda (20-30 m) y siendo menos comunes sobre la plataforma poco profunda (< 10 m), coincidiendo también con Brito (2013), donde estuvieron ausentes en las muestras de trampas de luz en la bahía de Mochima.
Como se mencionó anteriormente, las larvas de crustáceos fueron las más abundantes dentro del meroplancton. Sin embargo, cuando se compara con el trabajo de Brito (2013) en las formaciones coralinas de la bahía de Mochima, empleando el mismo método de captura, nuestras abundancias fueron superiores, a pesar que las larvas de crustáceos en su estudio ocuparon el segundo lugar en abundancia. En cambio, Sponaugle et al. (2021) reportaron a las larvas de decápodos como el taxón más abundante en los cayos de la Florida, seguidos de anfípodos hipéridos, camarones mísidos y estomatópodos. En la presente investigación los anfípodos hipéridos y los misidaceos estuvieron presentes, aunque en muy bajas abundancias, sin embargo, no se identificaron estomatópodos.
Las larvas de anélidos fueron el segundo grupo más abundante dentro del meroplancton; las mayores abundancias se registraron en la estación 1 y 3, lo que corrobora su asociación con el litoral rocoso y los parches coralinos de la ensenada. Las cifras obtenidas en la presente investigación son superiores y no coincide con Brito (2013) en los arrecifes coralinos de la bahía de Mochima, empleando el mismo método de captura. Los poliquetos constituyen la clase más importante del phylum Annelida, son uno de los grupos más diversos y abundantes en los sedimentos marinos desde zonas intermareales hasta grandes profundidades (Gasca y Suárez, 1996); sin embargo, existe poca información sobre estos organismos asociados a los arrecifes.
El ictioplancton fue el grupo minoritario de todo el estudio. Durante el periodo de relajación se evidenció un aumento progresivo, obteniéndose el mayor promedio del ictioplancton. Flores–Coto et al. (2009), mencionan que la abundancia del ictioplancton tiende a ser mayor durante el periodo de lluvias, debido a la mayor cantidad de nutrientes y mejores condiciones ambientales para el desarrollo de las larvas y huevos de peces. La lluvia puede aportar nutrientes a los ecosistemas acuáticos, lo que estimula el crecimiento del zooplancton, que a su vez es la base de la dieta de muchas larvas de peces.
Hacer comparaciones entre estudios empleando el mismo método de captura, en este caso trampas de luz, puede resultar complicado, debido a las diferencias en la metodología, el diseño de muestreo y la configuración del arrecife. Por ejemplo, en un estudio reciente de trampas de luz para examinar la composición del zooplancton en dos profundidades (15 y 40 m) en la barrera de coral mesoamericana frente a Honduras, encontraron que la composición del zooplancton y la riqueza taxonómica eran similares entre las profundidades (Andradi-Brown et al., 2017). En marcado contraste con los resultados obtenidos por Sponaugle et al. (2021) en trampas de luz en los arrecifes en los cayos de la Florida, quienes estudiaron el zooplancton sobre la plataforma poco profunda (<10 m), plataforma profunda (20 - 30 m) y en profundidades mesofóticas (40 - 70 m). Por consiguiente estas diferencias pueden ser atribuibles a diferencias en el diseño de las trampas de luz (por ejemplo, niveles de luz utilizados para atraer el zooplancton a las trampas), tiempo del ciclo lunar durante el cual se desplegaron las trampas, muestreo de una zona menos profunda, o sitios que están más cerca de la costa. De igual manera, también puede haber diferencias regionales o específicas del sitio. Otro factor que puede influir en el número de organismos recolectados en trampas de luz puede estar relacionado con la magnitud de las corrientes y la capacidad fototáxica de nadar con éxito hacia las trampas (Moriarty et al., 2021).
El zooplancton demersal, principalmente mísidaceos, que se sabe que emerge del hábitat del arrecife bentónico hacia la columna de agua durante la noche (Brito-Lolaia et al., 2020), no fue abundante en nuestra región de muestreo. Por consiguiente, los copépodos, cladóceros y quetognatos, los representantes más abundantes del holoplancton en este estudio, impulsaron un aumento de la biomasa nocturna de zooplancton sobre los parches de coral debido posiblemente a la advección durante sus migraciones verticales diurnas (Nakajima et al., 2009). Por lo tanto, es posible que la mayor parte de la abundancia de zooplancton muestreada no esté disponible de manera fácil o constante para los corales que se alimentan cerca del bentos durante la noche (Sebens et al., 1998) o para los peces planctívoros que se alimentan durante las horas del día (Lesser et al., 2018).
En general, en los arrecifes de coral existe una gran abundancia de formas meroplanctónicas como consecuencia de la presencia de muchos filos bentónicos (Mendoza-Portillo, 2013). La baja diversidad de formas larvarias reportadas en la presente investigación puede estar asociada a que en Turpialito, no existen densas extensiones de corales, otro posible factor que pudiera estar influyendo seria la alta tasa de sedimentación y una alta tasa de resuspensión de sedimentos, que son características comunes en los arrecifes coralinos del golfo de Cariaco (Núñez et al., 2011). Es importante destacar también, que cada especie tiene un nicho propio y causa una influencia diferencial en la totalidad de la comunidad planctónica. Sin embargo, la premisa fundamental es que las especies numéricamente dominantes (o en biomasa) ejercen mayor influencia en la transferencia de energía de la producción primaria a niveles tróficos superiores, como es el caso de los copépodos, y constituyen relevantes nodos de biomasa en la trama trófica del ecosistema epipelágico del golfo de Cariaco (Márquez-Rojas et al., 2020; Márquez-Rojas y Zoppi, 2023).
CONCLUSIÓN
La ensenada de Turpialito mostró variabilidad bimodal típica de la región nororiental de Venezuela, con régimen de surgencia costera estacional entre febrero y marzo, mientras la época de relajación se manifestó a partir de mayo. El análisis cualitativo sugiere que el zooplancton muestreado en esta ensenada corresponde más a un zooplancton pelágico que a un zooplancton demersal y este último fue poco representativo en relación a estudios similares. Entre los periodos estudiados, se detectó una diferencia significativa entre la abundancia de holo y merozooplancton; la población del holozooplancton dominó tanto en número como en diversidad en surgencia. Los copépodos fueron el grupo más abundante dentro del holoplancton, mientras que en el meroplancton las larvas de crustáceos fueron los más numerosos.
AGRADECIMIENTO
La segunda autora quiere agradecer al Instituto Oceanográfico de Venezuela, Universidad de Oriente, Venezuela, por todo el apoyo logístico. Este trabajo estuvo enmarcado dentro del proyecto Variación y composición del zooplancton asociado a las formaciones coralinas de la Ensenada de Turpialito, estado Sucre, Venezuela, financiado por el Consejo de Investigación de la Universidad de Oriente, Código Nº CI-02-030603-1966-17.
LITERATURA CITADA
Alvera-Azcárate, A., Barth, A., Weisberg, R., Castañeda, J., Vandenbulcke, L., y Beckers, J. (2011). Thermocline characterization in the Cariaco basin: A modeling study of the thermocline annual variation and its relation with winds and chlorophyll-a concentration. Cont. Shelf. Res. 31(1): 73-84. https://doi.org/10.1016/j.csr.2010.11.006
Alldredge, A. y King, J. (1980). Effects of moonlight on the vertical migration patterns of demersal zooplankton. J. Exp. Mar. Bio. Ecol. 84: 253-260.
Andradi-Brown, D. A., Head, C. E., Exton, D. A., Hunt, C. L., Hendrix, A., Gress, E. y Rogers, A. D. (2017). Identifying zooplankton community changes between shallow and upper-mesophotic reefs on the Mesoamerican Barrier Reef, Caribbean. PeerJ. 5: e2853. https://doi.org/10.7717/peerj.2853
Bérard-Therriault, L., M. Poulin y L. Bossé. (1999). Guide d'identification du phytoplancton marin de l' estuaire et du Golfe du Saint-Laurent. CNRC.
Blanco, A., Márquez-Rojas, B. y Díaz-Díaz, O. (2016). Abundancia y distribución de los foraminíferos planctónicos, en la ensenada de Turpialito, golfo de Cariaco, Venezuela. Bol. Inst. Oceanogr. Venez. 55(2): 60-71.
Boltovskoy, D. (1999). Zooplankton south Atlantic the Netherlands. Volumen I y II. Backhuys Publishers. Leiden,
Bowden, K. F. (1983). Physical oceanography of coastal waters. Ellis Horwood Ltd.
Brito, A. (2013). Variación y composición del zooplancton asociado a las formaciones coralinas de la bahía de Mochima, estado Sucre, Venezuela. Trabajo de Grado, Lic. Biología, Universidad de Oriente. Cumaná, Venezuela.
Brito-Lolaia, M., Santos, G. S., Neumann-Leitão, S. y Schwamborn, R. H. (2020). Micro- and mesozooplankton at the edges of coastal tropical reefs (Tamandaré, Brazil). Helgol. Mar. Res. 74 (7):1–14. https://doi.org/10.1186/s10152-020-00539-4
Calvo-Trujillo, A., Díaz-Ramos, J., Subero, S., Charzeddine-Charzeddine, L., Rincones-Reye, K., Troccoli-Ghinaglia, L. y Márquez, B. (2015).Variación a corto plazo del fitoplancton en la bahía de Turpialito, golfo de Cariaco, Venezuela, durante la época de lluvias. Bol. Inst. Oceanogr. Venez. 54(1): 13-24.
Calvo-Trujillo, A., Rincones-Reyes, K., Díaz-Ramos, J. R., Márquez-Rojas, B., Subero-Pino, S., Elista-Ramírez, E. y Troccoli-Ghinaglia, L. (2018). Distribución espacial y temporal del fitoplancton en el golfo de Cariaco, estado Sucre, Venezuela, febrero 2014 – enero 2015. Bol. Investig. Mar. Costeras, 47(2); 63-82. https://doi.org/10.25268/bimc.invemar.2018.47.2.747
Carrillo-Baltodano, A. y Morales-Ramírez, Á. (2016). Changes in abundance and composition of a Caribbean coral reef zooplankton community after 25 years. Rev. Biol. Trop, 64(3):1029-1040. http://dx.doi.org/10.15517/rbt.v64i3.21449.
Chan, B. K., Shao, K. T., Shao, Y. T. y Chang, Y. W. (2016). A simplified, economical, and robust light trap for capturing benthic and pelagic zooplankton. J. Exp. Mar. Bio. Ecol., 482, 25-32. https://doi.org/10.1016/j.jembe.2016.04.003.
Choat, J., Doherty, P., Kerrigan, B. y Leis, J. (1993). A comparison of two nets, purse seiner and light-aggregation devices for sampling larvae and pelagic juveniles of coral reef fishes. Fish. Bull. 91: 195-209.
Cowen, R. y Castro, L. (1994). Relation of coral reef fish larvae distributions to island scale circulation around Barbados, West Indies. Bull. Mar. Sci., 541: 228-244.
Crespo, R. y Soares-Gomes, A. (2009). Biología marina. Segunda Edición. Editorial Interciencia.
Cupp, E. (1943). Marine plankton diatoms of North America. Bulletin of the Scripps Institution of Oceanography.
Da Costa, R., Atique, P., Da Costa, K. y Pereira, L. (2011). Seasonal and spatial variation in hydrological parameters and microzooplankton communities in an Amazonian estuary. J. Coast. Res, 64: 1477-1481.
Doherty, P. (1987). Light-Traps: selective but useful devices for quantifying the distributions and abundance of larval fishes. Bull. Mar. Sci., 41: 423-431.
Edler, L. y M. Elbrächter. (2010). The Utermöhl method for quantitative phytoplankton analysis. En: Bengt, K., C. Cusack and E. Bresnan (Eds.). Microscopic and molecular methods for quantitative phytoplankton analysis. (pp. 13-20). UNESCO.
Espinosa-Carreón, L. y J. Eduardo Valdez-Holguín. 2007. Variabilidad interanual de clorofila en el golfo de California. Ecol. Apl. 6 (1 y 2): 83-92
Esquivel-Garrote, O. (2015). Abundancia, diversidad, biomasa y composición del zooplancton asociados a los parches de arrecifes coralinos en el Parque Nacional Isla del Coco, Pacifico de Costa Rica. Trabajo de Grado, Lic. Biología, Universidad de Costa Rica. San José, Costa Rica.
Ferraz-Reyes, E. (1989). Influencia de los factores físicos e la distribución vertical de la biomasa fitoplanctónica en el golfo de Cariaco (Venezuela). Bol. Inst. Oceanogr. Venez., 28(1 y 2): 47-56.
Figueroa, D. (2002). Zooplancton de formaciones coralinas, composición y distribución espacial en dos ambientes neríticos. Trabajo de Grado, Lic. Biología, Universidad de Oriente. Cumaná, Venezuela.
Flores-Coto, César., Espinosa Fuentes, María de la Luz., Zavala García, Faustino y Sanvicente Añorve, Laura. (2009). Ictioplancton del sur del Golfo de México: Un compendio. Hidrobiológica, 19(1), 49-76.
Gade, G. (1961). Further hydrographic observations in the southeastern Caribbean Sea and the adjacent Atlantic Ocean with special reference to the influence of the Orinoco River. Bol. Inst. Oceanogr. Venez., 1(2): 359-395.
Gasca, R. y Suárez, E. (1996). El zooplancton marino. El Colegio de la Frontera Sur (ECOSUR), Consejo Nacional de Ciencia y Tecnología.
Goldstein, E., D’Alessandro, E., Reed, J. y Sponaugle, S. (2016). Habitat availability and depth-driven population demographics regulate reproductive output of a coral reef fish. Ecosphere. 7(11): e01542. https://doi.org/10.1002/ecs2.1542
Heidelberg, K., Sebens, K. y Purcell, J. (2004). Composition and sources of near reef zooplankton on a Jamaican fore reef along with implications for coral feeding. Coral Reefs. 23(2): 263-276. https://doi.org/10.1007/s00338-004-0375-0
Heidelberg, K., O´Neil, K., Bythell, J. y Sebens, K. (2010). Vertical distribution and diel patterns of zooplankton abundance and biomass at Conch Reef, Florida Keys (USA). J. Plankton Res. 32(1): 75-91. https://doi.org/10.1093/plankt/fbp101
Hickford, M. y Schiel, D. (1999). Evaluation of the performance of light traps for sampling fish larvae in inshore temperate water. Mar. Ecol. Prog. Ser., 186: 293-302.
Jury, R. (2017). Eastern Venezuela coastal upwelling in context of regional weather and climate variability. Reg. Stud. Mar. Sci., 18: 219-228. https://doi.org/10.1016/j.rsma.2017.10.010
Kawagushi, K., Matsuda, O., Ishikawa, S. y Naito, Y. (1986). A light trap to collet krill and other micronektonic and plankton animals under the Antarctic coastal fast ice. Polar Biology, 6: 37-42.
Lesser, M. P., Slattery, M. y Mobley, C. D. (2018). Biodiversity and functional ecology of Mesophotic coral reefs. Annu. Rev. Ecol. Evol. Syst., 49: 49–71. https://doi.org/10.1146/annurev-ecolsys-110617-062423
Lindquist, D. y Shaw, R. (2005). Effects of current speed and turbidity on stationary light-trap catches of larval and juvenile fishes. Fishery Bulletin, 103(2): 438-444.
Margalef, R. (1965). Composición y distribución del fitoplancton. Mem Soc Cienc Nat La Salle, 25: 141-205.
Marín, B., Lodeiros, C., Figueroa, D. y Márquez, B. (2004). Distribución vertical y abundancia estacional del microzooplancton y su relación con los factores ambientales en Turpialito, golfo de Cariaco, Venezuela. Revista Científica, FCV-LUZ. 14 (2): 133-139. https://produccioncientificaluz.org/index.php/cientifica/article/view/15036
Márquez-Rojas, B., Troccoli, L., Marcano, L., Morales, J., Allen, T., Marín, B. y Díaz-Ramos, J. (2011). Estructura comunitaria del zooplancton en dos localidades del Golfo de Cariaco, Venezuela. Bol. Inst. Oceanogr. Venez., 50(2): 3-21.
Márquez-Rojas, B., Benítez, M. y Troccoli, L. (2016). Hidrografía y cambios estructurales del mesozooplancton en el golfo de Cariaco, en dos períodos contrastantes. Rev. Biodivers. Neotrop., 6(2): 135-146. https://doi.org/10.21068/c2017.v18n01a9
Márquez-Rojas, B., Zoppi de Roa, E., Troccoli, L. y Montiel, E. (2017). Cambios estructurales del mesozooplancton en relación a las condiciones hidrográficas en el golfo de Cariaco, Venezuela. Biota Colomb. 18(1): 148-171. https://doi.org/10.21068/c2017. v18n01a9.
Márquez-Rojas, B., Zoppi De Roa, E. y Zegarra-Narro, J. (2020). An updated checklist of copepod species (Arthropoda: Crustacea) from the Gulf of Cariaco, Venezuela. Pan-Am. J. Aquat. Sci., 15(3):143-150.
Márquez-Rojas, B. y Zoppi, E. (2023). Copépodos planctónicos del Caribe nororiental y Atlántico venezolano. Bol. Investig. Mar. Costeras. 52(2): 9-40. https://doi.org/10.25268/bimc.invemar.2023.52.2.1187.
Martínez G, Hernández D, Quintero A, Márquez A, Senior W, González A. (2011). Estudio físico-químico de las aguas del sector oriental del golfo de Cariaco, Venezuela. Bol. Inst. Oceanogr. Venez., 50(2): 273-287.
Meekan, M., Doherty, P. y White, L. (2000). Recapture experiments show the low sampling efficiency of light traps. Bull. Mar. Sci. 67: 975-885.
Meekan, M., Wilson, S., Halford, A. y Retzel, A. (2001). Comparison of catches of fish and invertebrates by two light traps designs in tropical NW Australia. Mar. Biol., 139: 373-381. https://doi.org/10.1007/s002270100577
Mendoza-Portillo, F. (2013). Estructura de la comunidad del holoplancton y meroplancton durante invierno y verano en el golfo de California. Trabajo de Maestría. Postgrado en Manejo de Recursos Marinos, Instituto Politécnico Nacional La Paz, México.
Morales, A. y Murillo, M. (1996). Distribution, abundance and composition of coral reef zooplankton, Cahuita National Park, Limon, Costa Rica. Rev. Biol. Trop. 44(2): 619-630. https://revistas.ucr.ac.cr/index.php/rbt/article/view/21652
Moriarty, V. W., Lucius, M. A., Johnston, K. E., Borrelli, J. J., Mattes, B. M., Pezzuoli, A. R., ... y Relyea, R. A. (2021). Fluorometer optical path interference via zooplankton phototaxis: Implications for high‐frequency data collection. Limnol. Oceanogr.:Methods, 19(3), 160-175.
Nakajima, R., Yoshida, T., Othman, B. y Toda, T. (2009). Diel variation of zooplankton in the tropical coral-reef water of Tioman Island, Malaysia. Aquat. Ecol., 43(4): 965-975. http://dx.doi.org/10.1007/s10452-008-9208-5
Nelson, C., Alldredge, A., McCliment, E., Amaral-Zettler, L. y Carlson, C. (2011). Depleted dissolved organic carbon and distinct bacterial communities in the water column of a rapid flushing coral reef ecosystem. ISME J., 5(8): 1374-1387. https://doi.org/10.1038/ismej.2011.12
Núñez, J., Ariza, L. y Jiménez, M. (2011). Evaluación de la estructura de las comunidades coralinas en la franja sublitoral de la zona costera sur del golfo de cariaco, Venezuela. Parte I: eje Turpialito-Quetepe. Bol. Inst. Oceanogr. Venez., 50(2): 149-159.
Okuda, T., Álvarez, J., Bonilla, J. y Cedeño, G. (1978). Características hidrográficas del golfo de Cariaco, Venezuela. Bol. Inst. Oceanogr. Venez., 17(1-2): 69-88.
Parsons, T., Maita, Y. and Lally, C. (1984). A manual of chemical and biological methods of seawater analysis. Pergamon Press.
Platt, T. y Sathyendranath, S. (1999). Spatial structure of pelagic ecosystem processes in the global ocean. Ecosyst., 2: 384-394.
Postel, L., Fock, H., y Hagen, W. (2000). Biomass and abundance. En: R. P. Harris, P. H. Wiebe, J. Lenz, H. R. Skjoldal y M. Huntley (Eds.). ICES Zooplankton Methodology Manual (pp. 83-174). Academic Press.
Quintero, A., Terejova, G. y Bonilla, J. (2005). Morfología costera del golfo de Cariaco, Venezuela. Bol. Inst. Oceanogr. Venez., 44(2): 133-143.
Raffaelli, D., Bell, E., Weithoff, G., Matsumoto, A., Cruz-Motta, J., Kerhaw, P., Parker, R., Parry, D. y Jones, M. (2003). The ups and downs of benthic ecology: considerations of scale, heterogeneity and surveillance for benthic-pelagic coupling. J. Exp. Mar. Bio. Ecol., 285(6): 191-203. http://dx.doi.org/10.1016/S0022-0981(02)00527-0
Rao, T. y Urosa, L. (1974). Ecología del zooplancton en el golfo de Cariaco. Parte І variabilidad de la biomasa del zooplancton durante el periodo de agosto a noviembre de 1973. Bol. Inst. Oceanogr. Venez., 13(1-2): 67-78.
Riley, C. y Holt, J. (1993). Gut contents of larval fishes from light trap and plankton net collections at Enmedio Reef near Veracruz, México. Rev. Biol. Trop., 41(1): 53-57.
Rivera-Tenenbaum, D. (2006). Dinoflagelados e tintinídeos da região central da Zona Econômica Exclusiva Brasileira: guia de identificação. Museo Nacional Rio de Janeiro.
Robichaux, D., Cohen, A., Reaka, M. y Allen, D. (1981). Experiments with zooplankton on coral reef, or, will the real demersal plankton please come up?. Mar. Ecol., 2(1): 77-94. https://doi.org/10.1111/j.1439-0485.1981.tb00092.x
Rueda-Roa, D., Ezer, T. y Müller-Karger, F. (2018). Description and mechanisms of the mid-year upwelling in the Southern Caribbean Sea from remote sensing and local data. J. Mar. Sci. Eng., 6(2): 36-46. http://dx.doi.org/10.3390/ jmse6020036.
Santos, G. S., Stemmann, L., Lombard, F. y Schwamborn, R. (2019). Are tropical coastal reefs sinks or sources of mesozooplankton? A case study in a Brazilian marine protected area. Coral Reefs. 38(6): 1107–1120. http://dx.doi.org/10.1007/s00338-019-01860-2
Sebens, K. P., Grace, S. P., Helmuth, B., Maney, E. J. y Miles, J. S. (1998). Water flow and prey capture by three scleractinian corals, Madracis mirabilis, Montastrea cavernosa and Porites porites, in a field enclosure. Mar. Biol., 131(2): 347–360. http://dx.doi.org/10.1007/s002270050328
Serrano-Zabala, R., Márquez, B., Troccoli, L., Rincones, K., Díaz, J. y Reyes, J. (2020). Variabilidad de la abundancia del zooplancton en dos ambientes neríticos del nororiente de Venezuela. Bol. Inst. Oceanogr. Venez., 59(1): 85-108.
Sheskin, D. (2004). Handbook of Parametric and nonparametric statistical procedures. Second edition. Chapman & Hall/CRC.
Schnack-Schiel, S. y Isla, E. (2005). The role of zooplankton in the pelagic-benthic coupling of the Southern Ocean. Sci. Mar. 69(S2): 39-55. https://doi.org/10.3989/scimar.2005.69s239
Smith, D. (1977). A guide to marine coastal plankton and marine invertebrate larvae. Kendall-Hunt Publishing Company.
Soto, P. G., Troccoli, L., Díaz, J. R., Martínez, G. y Crescini, R. (2015). Variabilidad a corto plazo de la hidrografía y fitoplancton en la Ensenada de Turpialito, Venezuela. Bol. Inst. Oceanogr. Venez., 54: 125-137
Sorokin, Y. (1993). Coral reef ecology. Springer.
Sournia, A. (1978). Phytoplankton Manual (Ed). Muséum National d’Histoire Naturelle.
Sponaugle, S., Goldstein, E., Ivory, J., Doering, K., D’Alessandro, E., Guigand, C. y Cowen, R. K. (2021). Near-reef zooplankton differs across depths in a subtropical seascape. J. Plankton Res. 43(4): 586–597. https://doi.org/10.1093/plankt/fbab043
Suárez-Morales, E. y Rivera, A. (1998). Zooplancton e hidrodinámica en zonas litorales y arrecifales de Quintana Roo, México. Hidrobiológica, 8(1): 19-32.
Ter Braak, C. J. y Verdonschot, P. F. (1995). Canonical correspondence analysis and related multivariate methods in aquatic ecology. Aquat. Sci., 57: 255-289.
Ter Braak, C. y Smilauer, P. (2002). CANOCO reference manual and canodraw for windows user's guide: software for canonical community ordination (version 4.5). (Microcomputer Power). https://edepot.wur.nl/405659.
Thorrold, S. (1993). Evaluating the performance of light traps for sampling small fish and squid in open waters of the central Great Barrier Reef lagoon. Mar. Ecol. Prog. Ser., 89: 277-285.
Tomas, C. (1997). Identifying marine diatoms and dinoflagellates. Academic Press.
Tregouboff, G. y Rose, M. (1978). Manuel de plantonologie medditerraneenne. I y II. Editions du Centre de la Recherche Scientifique.
Zar, J. H. (1999). Biostatistical analysis. Prentice Hall.















