Introducción
El Departamento de Apurímac tiene el 14.75 % de la población nacional de equinos (597 969 animales) entre potros, yeguas y caballos1. El caballo criollo Alto Andino está presente en la serranía peruana, se caracteriza por su adaptabilidad a los pisos ecológicos de la agreste serranía, muestran gran resistencia, fortaleza y rusticidad, son utilizados para transporte, carreras, paseos y en corridas de toros, durante las festividades religiosas2. Además, su empleo de su fuerza animal, conlleva a labores complementarias en la finca, estancias, huertos, plantación o bosque, para reducir todo período de inactividad, su alimentación es a base de pasturas de baja calidad nutricional de la finca y pastizales vecinos, ya que los caballos transforman los residuos de la cosecha de manera productiva, y eficaz, aportando abono orgánico en forma de estiércol que refuerza la fertilidad del suelo3. El caballo castrado o capón se desempeña mejor, por su docilidad, es manejable cuando está en grupo e ideal para el trabajo diario en transporte y carga4.
El perfil lipídico (PL) en caballos está constituido por la concentración de triacilgliceroles (TG), colesterol total (CT) y sus fracciones contenidas en las lipoproteínas de alta densidad (HDL-CT) y baja densidad (LDL-CT) en el suero o plasma, ya que los lípidos están implicados en la formación de membranas, síntesis de hormonas esteroides, aporte y transporte de combustibles metabólico5.
La alimentación es uno de los factores que podría modificar el perfil lipídico, se ha observado qué en ciertas estaciones del año, tendría efectos en la presencia de obesidad en caballos (27 a 35 %), en comparación con equinos que viven al aire libre y pastorean por encima de 6 h al día6. En otro estudio, caballos castrados alimentados únicamente con forraje, después del ejercicio, provocó el incremento de ácidos grasos no esterificados en plasma, este comportamiento indicaría una mayor utilización de grasa corporal para el mantenimiento7. Además, en caballos castrados, durante la competición de salto, se incrementó TG y disminuyó en el período de recuperación, durante la competición y después de 24 h de descanso se observó la disminución significativa de CT y LDL-CT e incrementó moderadamente de HDL-CT, este comportamiento sugiere el transporte inverso del colesterol desde los tejidos periféricos al hígado para nuevos procesos bioquímicos8.
La edad sería otro de los factores que incrementarían o modificarían la composición de los lípidos circulantes en sangre5, como los niveles séricos de CT y TG9. En caballos sementales con edades < 5años, 6 a 11 años y > 11 años, tienden a incrementar el CT, HDL-CT y LDL-CT y disminuir TG10. Además, se deben tomar en cuenta factores que alteran el PL, como la hiperlipidemia equina, el síndrome metabólico equino (SME), obesidad, el estado físico del animal o sedentarismo y sobre todo la nutrición11. Los TG son indicadores de lipidosis hepática, el incremento a nivel sérico se asocia con la acumulación de lípidos en el hígado, lo que interfiere con su función12. Estudios del perfil lipídico en equinos castrados criados en condiciones de inactividad y para el trabajo a grandes altitudes está limitado, en caballos y mulas trabajados en altitudes de 2700-4000 m durante 45 días, con una alimentación a base de granos más 10 % de aceite y acceso libre a pastos nativos durante toda la noche, se ha observado que durante el ejercicio se ha incrementado los niveles séricos de ácidos grasos libres y no hubo diferencias entre dietas y animales13.
En caballos de carrera castrados se observó, que la relación entre la edad y el colesterol fue r = 0.128, entre la edad y los TG fue r = 0.267 y no hubo efecto del envejecimiento sobre la concentración de TG (r = -0.022, P = 0.906). Cabe señalar que el balance energético negativo y el movimiento excesivo de ácidos grasos fuera del tejido adiposo conducen a niveles elevados de TG en sangre, además de la lipemia14, en tal sentido, se evaluó los niveles séricos de CT, HDL-CT, LDL-CT y TG, por efecto de la edad de caballos (Equus caballus) criollos castrados criados en el distrito de Antabamba, Apurímac.
Materiales y métodos
Se utilizaron 98 caballos criollos castrados (CCC) criados en 3 comunidades del distrito de Antabamba, agrupados en 4 rangos de edad: 3 a 5 años (n = 14), 6 a 9 años (n = 42), 10 a 15 años (n = 32) y mayor a 16 años (n = 10).
La edad de los CCC fue estimada de acuerdo al desarrollo dentario. Para la edad 3 a 5 años, se consideró la erupción de los incisivos permanentes hasta el reemplazo de los incisivos extremos y la emergencia de los caninos, para la edad 6 a 9 años, se consideró la muda de todos los incisivos que finaliza a los 5 años e inicia el rasamiento o desgaste de los dientes permanentes hasta que aparece la estrella dentaria en los extremos, para la edad 10 a 15 años, se consideró la forma redonda de la cara oclusal de los incisivos, además, aparece una mancha café en el extremo superior y el surco de Galvayne, y mayor a 16 años, se consideró cuando el surco de Galvayne sobrepasa la mitad del diente y la forma triangular que toma la cara oclusal de los extremos15.
Los propietarios de los animales mencionaron que no tienen el hábito de realizar evaluaciones sanitarias, menos la administración de medicamentos u otros. La alimentación fue en base a rastrojos de cosecha especialmente de maíz chala y pasturas naturales en las áreas de las comunidades, mediante pastoreo con estaca, y no recibieron suplementación.
Por las condiciones medioambientales, temperatura entre 0.6 a 25° C, y altitud de 3600 a 4200 m, además, de la lejana ubicación de los animales, la obtención de las muestras se realizó desde las 10:00 a 14:00 h, los CCC estuvieron en periodo de inactividad y se encontraban en las zonas de pastoreo, se sometieron a sujeción y en algunos casos con la ayuda de los propietarios y en otros casos se cubrieron los ojos, se realizó la extracción de sangre por venopunción de la yugular, las muestras de sangre se colectaron en tubos al vacío de 6 mL con activador de coágulos.
El suero se obtuvo mediante sedimentación, después de 2 h el suero sanguíneo (libre de hemolisis) fue transferido a viales de 5 mL con ayuda de pipetas Pasteur descartables y se congelaron a -20° C.
Para determinar los niveles séricos de CT (Valtek diagnostics, Cl, Lot: 230606) se utilizó el método enzimático16, las HDL-CT (Valtek diagnostics, Cl, Lot: 230425) mediante reactivo precipitante (Fosfotungstato/Mg++)17, las LDL-CT (Valtek diagnostics, Cl, Lot: 230602) mediante reactivo precipitante (heparina)17 y los TG (Bialex, USA, Lot: 23TT0701) mediante el método enzimático18, cada uno de los reactivos contenía calibrador o estándar. Se realizó 2 lecturas por cada muestra de suero sanguíneo, en un analizador bioquímico semiautomatizado (StatFax 3300) previo test de autocalibración.
Los niveles séricos del PL fueron evaluados mediante la prueba de Shapiro-Wilk. Los niveles séricos de los TG al no cumplir con la prueba de normalidad, se aplicó la transformación de datos mediante logaritmo natural.
Los datos para los 4 rangos de edades de CCC fueron analizados bajo el diseño completamente al azar (DCA) y para la comparación de medias se aplicó el contraste de Dunnett (p≤0.05), previamente se realizó la prueba de homogeneidad de varianzas a través de Levene. Además, se determinó el coeficiente de correlación lineal múltiple (r), para medir la intensidad de asociación lineal entre las variables19.
Resultados
En la Figura 1, se observan los niveles séricos de CT en CCC, el mayor nivel sérico se observó en el rango etario de 10 a 15 años de edad (95.4 mg dL-1) y disminuyeron en el último rango etario (93.3 mg dL-1), estos valores no presentaron diferencias significativas (P > 0.05). El valor mínimo se observó en los animales de 3 a 5 años (64.5 mg dL-1) y el valor máximo de 10 a 15 años de edad (136.4 mg dL-1).
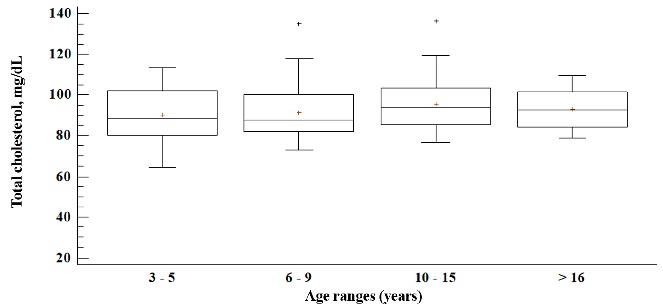 Figura 1
Niveles séricos de colesterol total (mg dL-1) en caballos criollos castrado
Figura 1
Niveles séricos de colesterol total (mg dL-1) en caballos criollos castrado
En la Figura 2, se observan los niveles séricos de las HDL-CT, el mayor nivel sérico estuvo en los de 3 a 5 años de edad (37.3 mg dL-1), los rangos etarios desde 10 años (35.8 mg dL-1) y mayores a los 16 años fueron similares (35.9 mg dL-1) y el menor nivel sérico fue en 6 a 9 años (33.0 mg dL-1), los valores tuvieron diferencias significativas (P < 0.05). El valor mínimo se observó en el rango etario de 6 a 9 años (15.5 mg dL-1) y el valor máximo ocurrió en los de 3 a 5 años de edad (47.3 mg dL-1).
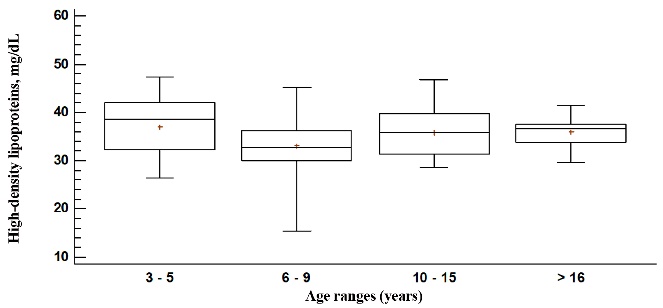 Figura 2
Niveles séricos de HDL-CT (mg dL-1) en caballos criollos castrados
Figura 2
Niveles séricos de HDL-CT (mg dL-1) en caballos criollos castrados
En la Figura 3, se observa los niveles séricos de LDL-CT, el mayor nivel sérico se observó en el rango etario de 10 a 15 años (52.2 mg dL-1), fue similar con relacion a la edad, mayor a 16 años (50.6 mg dL-1), los rangos etarios desde 3 hasta los 9 años tuvieron los menores valores y fueron similares entre sí (42.2 y 42.5 mg dL-1 respectivamente), los valores presentaron diferencias significativas (P < 0.05). El valor mínimo se observó en el rango etario de 6 a 9 años (28.4 mg dL-1) y el valor máximo de 10 a 15 años de edad (79.4 mg dL-1).
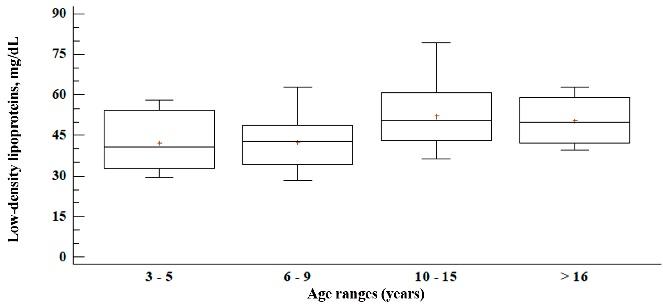 Figura 3
Niveles séricos de LDL-CT (mg dL-1) en caballos criollos castrados
Figura 3
Niveles séricos de LDL-CT (mg dL-1) en caballos criollos castrados
En la Figura 4, se observa los niveles séricos de TG, estos valores se incrementaron hasta los 10 a 15 años de edad (33.3 mg dL-1) y disminuyeron en el último rango etario (28.4 mg dL-1), no hubo diferencias significativas (P > 0.05). El valor mínimo y máximo se observó en el grupo de 6 a 9 años de edad (7.4 y 92.4 mg dL-1 respectivamente).
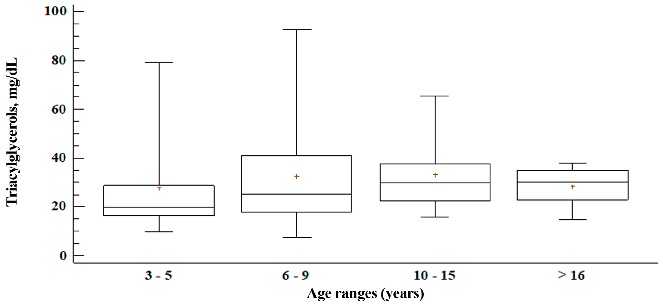 Figura 4
Niveles séricos de triacilgliceroles (mg dL-1) en caballos criollos castrados
Figura 4
Niveles séricos de triacilgliceroles (mg dL-1) en caballos criollos castrados
Tabla 1
Correlación lineal del perfil lipídico en caballos criollos castrados

| CT | HDL-CT | LDL-CT | TG |
| Edad | .1074 p = .2923 | .0970 p = .3422 | .3509 p = .0004 | .0040 p = .9690 |
| CT | | .3001 p = .0027 | .7792 p = .0000 | .2666 p = .0080 |
| HDL-CT | | | .0720 p = .4808 | .3813 p = .0001 |
| LDL-CT | | | | .0823 p = .4207 |
En la Tabla 1, se observa la relación entre los niveles séricos del PL y la edad de los CCC, existe una correlación lineal positiva entre las variables. Además, se observa que existe una correlación muy baja (r = 0.2 a r = 0.3) entre la edad y los niveles séricos de LDL-CT significativa (P < 0.05), también, entre los niveles séricos del CT y de la HDL-CT y TG existe una correlación muy baja (r = 0.2 a r = 0.3) que fueron significativas (P < 0.05) y ocurre lo contrario entre el CT y LDL-CT, existe una correlación alta (r = 0.6 a r = 0.7) que fueron significativas (P < 0.05); además, entre los niveles séricos de la HDL-CT y TG existe una correlación muy baja (r = 0.2 a r = 0.3) que fue significativa (P < 0.05).
Discusión
La relación de los datos de CT, 90.3 a 95.4 mg dL-1, guardan cierta similitud con Halo Jr. et al.20, Burlikowska et al.21 & Diakakis et al.22, sin embargo, resultan ser bajos, si se los relaciona con los de Adedokun et al.23 & Abeni et al.24, lo que significa que el CT, dependerá de la actividad que realicen estos animales y el tipo de dieta, lo que da lugar a estas diferencias.
Con respecto a la edad, los niveles séricos de CT hallados en CCC de 6 a 9 años tuvieron valores (91.3±13.1 mg dL-1) por debajo de caballos castrados que a la edad de 9 años (128.9±14.1 mg dL-1)25, además, los valores hallados son similares a los descritos en caballos peruanos de paso capones (103.5±17.2 mg dL-1) con edades entre 3 y 15 años26 y ocurre el mismo comportamiento con caballos machos menores de 4 años (98.6±13.4 mg dL-1) y machos mayores de 4 años (100.5±11.0 mg dL-1) que no hubo diferencias significativas entre edades11. En la época que se obtuvieron las muestras de sangre, los caballos estaban sin realizar trabajos de carga, la relativa variación en los niveles séricos de CT con respecto a la edad, tendrían relación con la adaptación de estos animales al clima local27 y la poca actividad física28.
Desde el punto de vista nutricional, los niveles séricos están por encima con respecto a caballos crónicamente hambrientos que tuvieron valores de (73.8 a 79.0 mg dL-1)29, por otro lado, si comparamos los valores con otros reportados en caballos criollos (172.6±72.6 mg dL-1) resultan ser inferiores, esta diferencia probablemente se debería a su adaptación al medio y al tipo de actividad física del caballo criollo, además, los rangos de edad y el sexo no hubo diferencias significativas30. En otro estudio, los niveles séricos de CT tienden a incrementarse de 78.8 a 84.4 mg dL-1 en caballos que fueron sometidos de forma regular y repetida a múltiples tipos diferentes de cargas y se observó que los valores estuvieron dentro del rango de referencia para caballos31.
Los niveles séricos de HDL-CT descritos en CCC está entre 33.0 a 37.3 mg dL-1, estos valores resultaron ser similares a los indicados por Adedokun et al.23 e inferiores a los valores reportados por Burlikowska et al.21, además, sus valores son inferiores a los observados en caballos peruanos de paso capones (18.0±8.7 mg dL-1) con edades entre 3 y 15 años, esto indicaría, que tendrían menor riesgo aterogénico26 y ocurre el mismo comportamiento con caballos machos menores de 4 años (60.8±9.6 mg dL-1) y machos mayores de 4 años (60.3±9.8 mg dL-1) que no tuvieron diferencias significativas entre edades11.
Los niveles séricos de LDL-CT observados en CCC está entre 42.2 a 52.2 mg dL-1, estos valores resultaron ser superiores a los indicados por Burlikowska et al.21 e inferiores a los reportados por Adedokun et al.23, además, los valores fueron superiores a los descritos en caballos peruanos de paso capones (21.2±12.0 mg dL-1) con edades entre 3 y 15 años26 y ocurre el mismo comportamiento con caballos machos menores de 4 años (28.2±6.4 mg dL-1) y machos mayores de 4 años (27.7±6.8 mg dL-1) que no hubo diferencias significativas entre edades11.
Los niveles séricos de TG hallados en CCC está entre 27.5 a 33.3 mg dL-1, estos tuvieron cierta similitud con Halo Jr. et al.20 y Diakakis et al.22, sin embargo, resultan ser bajos con respecto a Burlikowska et al.21 e inferiores a los reportados por Adedokun et al.23, por otro lado, están por debajo del rango superior propuesto por Abeni et al.24.
Si tenemos en consideración la edad, los niveles séricos de TG en caballos castrados criollos de 6 a 9 años tuvieron valores (32.4±21.0 mg dL-1) por encima de caballos castrados de una edad de 9 años (20.2±2.2 mg dL-1)25, además, se observó el mismo comportamiento con los valores en caballos peruanos de paso capones (19.7±9.1 mg dL-1) con edades entre 3 y 15 años, esto indicaría, que son poco susceptibles a sufrir hipertrigliceridemia26 y ocurre todo lo contrario con caballos machos menores de 4 años (48.2±14.0 mg dL-1) y machos mayores de 4 años (43.4±13.1 mg dL-1) que no tuvieron diferencias significativas entre edades11. La similitud en los niveles séricos de TG en los rangos de edad, podrían deberse a la inactividad física que realizan los CCC, ya que los niveles de TG se correlacionan positivamente con la intensidad del ejercicio32.
Desde el punto de vista nutricional, los niveles séricos están por encima con respecto a caballos crónicamente hambrientos con una condición corporal menor a 3, tuvieron valores de 19.3±3.6 mg dL-1, y los caballos con mejor condición corporal con valores de 48.0±4.0 mg dL-1)29, por otro lado, si comparamos los valores hallados con caballos que fueron sometidos de forma regular y repetida a múltiples tipos diferentes de cargas con, valores que tienden a disminuir de 44.4 a 38.0 mg dL-1, pero que estuvieron dentro del rango de referencia para caballos31.
Los niveles de CT en CCC no tuvieron variaciones entre las edades, estos nos indicaría el equilibrio entre la ingesta y la síntesis de colesterol, por lo tanto, no se formarían placas ateroscleróticas33 y no tendrían trastornos de hiperlipemia34. Por otro lado, en animales aparentemente sanos bien mantenidos y alimentados, criados a una altitud de 250 m en clima tropical, se observó niveles elevados de CT (146.20±12.9 mg dL-1) y TG (61.55±10.30 mg dL-1) por encima del rango de referencia, sin diferencias entre edades23, estas variaciones podrían atribuirse a factores climáticos o ambientales.
La altitud no afectaría los niveles séricos de los CCC posiblemente por la adaptación al medio ambiente, en condiciones de inactividad y con pesos normales, se ha reportado en ratas expuestas a altitudes de 2200 a 3500 m mediante la simulación de hipoxia, con valores más bajos de CT, LDL y TG, pero más altos de HDL, pero sin diferencias notables debido a la altitud35. Además, la aclimatación a gran altitud (4300 m) se asocia con niveles elevados de ácidos grasos libres en plasma, por ende, una mayor utilización de grasa corporal36.
La correlación lineal observada entre el CT y las lipoproteínas fue significativa (P < 0.05), en especial con LDL-CT que tienen una correlación alta (r = 0.78) y con la HDL-CT que mantienen una correlación muy baja (r = 0.30), cabe mencionar, que las LDL transportan mayor cantidad de colesterol y con las lipoproteínas HDL transportan cerca del 90 % del colesterol en el plasma37, estos niveles de colesterol, nos darían la posibilidad de indicar que los CCC no presentarían insuficiencia hepática, y a menudo tendrían concentraciones elevadas de colesterol en suero, y la disminución del colesterol a veces se asocia con disfunción hepática grave38.
La síntesis de LDL se forman a partir de las lipoproteínas de muy baja densidad (VLDL) a nivel sanguíneo37, la correlación muy baja (r = 0.35) observada entre la edad y LDL-CT, nos indicaría posiblemente que los CCC mayores a 10 años de edad podrían presentar parasitismo, además, de infiltración grasa en el hígado, corazón y riñones37.
La correlación lineal observada entre las HDL-CT y los TG fue significativa (P < 0.05), que tienen una correlación muy baja (r = 0.38), cabe mencionar, que las moléculas de TG circulan en partículas de lipoproteínas34, también, si la síntesis de TG excede la capacidad de exportación hepática, estos se acumularán en las vesículas de los hepatocitos, dando lugar al hígado graso39, además, los TG están relacionados con la hiperlipidemia40, patologías que no tendrían implicancias con los CCC, pero que si estarían afectados por la raza, la edad, el estilo de vida, el estrés, el clima y otros factores41.
Literatura citada
1. Instituto Nacional de Estadística e Informática. Resultados definitivos. IV Censo Nacional Agropecuario [Internet]. Lima: Instituto Nacional de Estadística e Informática; 2013 [citado 12 de junio de 2024]. 63 p. Recuperado a partir de: https://dataspace.princeton.edu/handle/88435/dsp016969z391v
2. Gutiérrez Holguín E. Caracterización zoométrica del caballo criollo altoandino en las provincias de Espinar y Chumbivilcas de la región cusco [tesis licenciatura]. [Cusco]: Universidad Nacional de San Antonio Abad del Cusco; 2019 [citado 26 de octubre de 2024]. Recuperado a partir de: https://repositorio.unsaac.edu.pe/handle/20.500.12918/3688
3. Chirgwin JC. Work animals and sustainable development. In: Diouf J, Daldin T, Gumprecht, editors. World animal review [Internet]. Rome: Food and Agriculture Organization of the United Nations; 1997. Retrieved from: https://www.fao.org/4/v8180t/v8180T0p.htm#los%20animales%20de%20trabajo%20y%20el%20desarrollo%20sostenible
4. Mota-Rojas D, Braghieri A, Álvarez-Macías A, Serrapica F, Ramírez-Bribiesca E, Cruz-Monterrosa R, et al. The use of draught animals in rural labour. Animals (Basel) 2021;11(9):2683. DOI: https://doi.org/10.3390/ani11092683
5. Márquez A, De Abreu JC, Márquez YC, López A. Perfiles lipídico y proteico en plasma de yeguas de raza cuarto de milla en diferentes etapas reproductivas. Rev Vet 2014;25(1):54-7. DOI: https://doi.org/10.30972/vet.251551
6. Giles SL, Rands SA, Nicol CJ, Harris PA. Obesity prevalence and associated risk factors in outdoor living domestic horses and ponies. Peer J 2014;20 (2):e299 DOI: https://doi.org/10.7717/peerj.299
7. Jansson A, Lindberg JE. A forage-only diet alters the metabolic response of horses in training. Animal 2012;6(12):1939-46. DOI: https://doi.org/10.1017/S1751731112000948
8. Assenza A, Arfuso F, Zanghì E, Fazio F, Bruschetta D, Piccione G. Lipid and lipoprotein profiles modification in athletic horses after repeated jumping events. J Equine Vet Sci 2016;43:28-31. DOI: http://doi.org/10.1016/j.jevs.2016.05.001
9. Rukavina D, Alilovic I, Crnkic C, Ajanovic A, Preldzic D, Coralic A, et al. Serum biochemical parameters in clinically healthy adult Bosnian mountain horse. Vet Stanica 2019;50(5):415-21.
10. Basiru A, Ishola AO, Sanusi F, Olaifa FH. Influence of age on haematology, serum biochemistry and lipid profile of stallions in Ilorin, Nigeria. Sahel J Vet Sci 2022;19(2):21-5. DOI: http://dx.doi.org/10.54058/saheljvs.v19i2.302
11. Osorio JH, Quenan Y, Castañeda JA. Comparación de perfil lipídico por sexo y edad en una población de equinos en Caldas (Colombia). Rev Med Vet Zoot 2020;67(2):149-58. DOI: https://doi.org/10.15446/rfmvz.v67n2.90708
12. Last R. Clinical pathology basics for equine practitioners - Liver disease. Equine [Internet]. 2020 [cited 15 September 2024];22(1):48-54. Retrieved from: https://www.cpdsolutions.co.za/Publications/article_uploads/EHU_2020_Issue_01_Clinical_Pathology.pdf
13. Wickler SJ, Pauley PS, Bray RE, London C, Gabbard M. Performance at high altitude of horses and mules receiving fat supplemented diets. Equine Vet J 1995;27 Suppl 18:406-9. DOI: https://doi.org/10.1111/j.2042-3306.1995.tb04962.x
14. Satue K, Fazio E, Medica P, Miguel L, Gardón JC. Biochemical and hematological indexes of liver dysfunction in horses. J Equine Vet Sci 2023;126 (7):104294. DOI: https://doi.org/10.1016/j.jevs.2023.104294
15. Cardona JA, Álvarez J. Estimación de la edad de los caballos basado en el examen dentario. Rev UDCA Actual Divulg Cient 2010;13(1):29-39. DOI: https://doi.org/10.31910/rudca.v13.n1.2010.706
16. Watson D. A simple method for the determination of serum cholesterol. Clin Chim Acta 1960; 5(5):637-43. DOI: https://doi.org/10.1016/0009-8981(60)90004-8
17. Lopes-Virella MF, Stone P, Ellis S, Colwell JA. Cholesterol determination methods in high-density lipoproteins separated by three different methods. Clin Chem 1977;23(5):882-4. DOI: https://doi.org/10.1093/clinchem/23.5.882
18. Fossati P, Prencipe L. Serum triglycerides determined colorimetrically with an enzyme that produces hydrogen peroxide. Clin Chem 1982;28 (10):2077-80. DOI: https://doi.org/10.1093/clinchem/28.10.2077
19. Ibañez V. Análisis y diseño de experimentos. Puno: Editorial Universitaria; 2009. 449 p.
20. Halo Jr M, Massányi M, Strecansky M, Kovácik A, Formicki G, Gren A, et al. The effect of age on biochemical parameters on horses. Anim Sci Biotechnol 2020;53(2):117-20.
21. Burlikowska K, Boguslawska-Tryk M, Szymeczko R, Piotrowska A. Haematological and bio-chemical blood parameters in horses used for sport and recreation. J Cent Eur Agric 2015;16(4):370-82. DOI: https://doi.org/10.5513/JCEA01/16.4.1634
22. Diakakis N, Mylonakis ME, Roubies N, Koutinas C, Fytianou A, Koutinas AF. Reference values of 23 clinically important biochemical parameters in 107 normal pleasure horses residing in northern Greece. J Hellenic Vet Med Soc 2018;53(2):138-46. DOI: https://doi.org/10.12681/JHVMS.15370
23. Adedokun RA, Olaogun SC, Alaba BA. Haematological and biochemical profile of apparently healthy horses in Ibadan, Nigeria. Alex J Vet Sci 2023;77(1):156-64. DOI: https://doi.org/5455/ajvs.10877
24. Abeni F, DalPra A, Bertin G, Calamari L. Serum protein fraction in mature horses and relationship with metabolic and hematological parameters. J Equine Vet Sci 2013;33(11):905-11. DOI: https://doi.org/10.1016/j.jevs.2013.01.006
25. Ju JC, Cheng SP, Fan YK, Hsu JC, Chiang SK, Chen EV, et al. Investigation of equine hematological constituents in central Taiwan. I. Distribution of the blood cell parameters and the biochemical compositions of serum. Asian-Australas J Anim Sci 1993;6(1):147-53. DOI: https://doi.org/10.5713/ajas.1993.147
26. Díaz C, Plaza E, Chimoy P. Niveles séricos de triglicéridos y colesterol en caballos peruanos de paso bajo dos sistemas de crianza. Rev Investig Vet Perú 2008;19(2):134-9. DOI: https://doi.org/10.15381/rivep.v19i2.1127
27. Hasso SA, Al-Hadithy HA, Hameed RM. Serum glucose concentration and lipid profile in racing horses. Iraqi J Vet Sci 2012;26(1):1-3. DOI: https://doi.org/10.33899/ijvs.2012.46823
28. Vincze A, SzabO C, Hevesi A, Veres S, Uto D, Babinszky L. Effect of age and event on post exercise values of blood biochemical parameters in show jumping horses. Acta Agr Kapos 2010; 14(2):185-91.
29. Muñoz A, Riber C, Trigo P, Castejón F. Hematology and clinical pathology data in chronically starved horses. J Equine Vet Sci 2010;30(10):581-9. DOI: https://doi.org/10.1016/j.jevs.2010.09.002
30. Lacerda L, Campos R, Sperb M, Soarse E, Barbosa P, Goginho E, et al. Hematologic and biochemical parameters in three high performance horse breeds from southern Brazil. Arch Vet Sci 2006;11(2):40-4. DOI: https://doi.org/10.5380/avs.v11i2.6783
31. Massányi M, Halo MJr, Massányi P, Mlyneková E, Gren A, Formicki G. Changes in haematological and biochemical parameters in blood serum of horses during exposition to workload stress. Heliyon 2022;8(12):e12241. DOI: https://doi.org/10.1016/j.heliyon.2022.e12241
32. Czech A, Kiesz M, Kiesz A, Próchniak T, Rózanski P, Klimiuk K. Influence of type of use, age and gender on haematological and biochemical blood parameters of Malopolski horses. Ann Anim Sci 2019;19(1):85-96. DOI: https://doi.org/10.2478/aoas-2018-0031
33. Garrido Pertierra A, coordinador. Bioquímica Metabólica Conceptos y Tests. Madrid: Editorial Tebas S.L.; 2001. 392 p.
34. Stockham SL. Interpretation of equine serum biochemical profile results. Vet Clin North Am Equine Pract 1995;11(3):391-414. DOI: https://doi.org/10.1016/s0749-0739(17)30307-3
35. Du X, Girard O, Fan RY, Ma F. Effects of Active and passive hypoxic conditioning for 6 weeks at different altitudes on blood lipids, leptin, and weight in rats. High Alt Med Biol 2020;21(3):243-8. DOI: https://doi.org/10.1089/ham.2020.0003
36. Kennedy SL, Stanley WC, Panchal AR, Mazzeo RS. Alterations in enzymes involved in fat metabolism after acute and chronic altitude exposure. J Appl Physiol (1985) 2001;90(1):17-22. DOI: https://doi.org/10.1152/jappl.2001.90.1.17
37. Díaz González FH, Ceroni da Silva S. Introducción a bioquímica clínica veterinaria [Internet]. Barcelona: Editorial Unillanos; 2019 [citado 02 de mayo de 2024]. 473 p. Recuperado a partir de: https://editorial.unillanos.edu.co/index.php/editorial-unillanos/catalog/view/4/12/28
38. Kerr M. Veterinary laboratory medicine, Clinical biochemistry and haematology [Internet]. New Jersey: Blackwell Science; 2002 [cited May 2, 2024]. 472 p. Retrieved from: https://www.google.com/webhp?hl=es&sa=X&ved=0ahUKEwj0v53ew_CKAxXUKrkGHVpGLp4QPAgI
39. Bruss ML. Lipids and ketones. In: Kaneko JJ, Harvey JW, Bruss ML, editors. Clinical Biochemistry of Domestic Animals [Internet]. London: Academic Press; 1997. p. 83-115. DOI: https://doi.org/10.1016/B978-012396305-5/50005-1
40. Agina OA. Haematology and clinical bioche-mistry findings associated with equine diseases - a Review. Not Sci Biol 2017;9(1):1-21. DOI: https://doi.org/10.15835/nsb919939
41. Massányi M, Halo M, Halo JrM, Massányi P. Influence of different levels of load on the metabolic profile of horses- a Review. Sci Pap Anim Sci Biotechnol 2020;53(2):128-36.
Notas
Fuente de financiamiento: Autofinanciado por los autores.
__________
Conflictos de intereses: Los autores no tenemos ningún conflicto de intereses.
__________
Agradecimientos: A la Facultad de Medicina Veterinaria y Zootecnia de la Universidad Nacional Micaela Bastidas de Apurímac.
___________
Consideraciones éticas: Los caballos fueron sometidos a sujeción y la extracción de sangre fue sin causar dolor o sufrimiento, se realizó de acuerdo a las normas vigentes (Ley de protección y bienestar animal, Ley 30407).
___________
Aporte de los autores en el artículo: Liz Lizbeth Huacho Felix, toma de muestras y ejecución del experimento, redacción y preparación del borrador original.
Ruth Ramos-Zuñiga, ejecución del experimento y administración del proyecto.
Ludwing Angel Cárdenas-Villanueva, supervisión de resultados y discusión, búsqueda de información, redacción y revisión final del documento para publicación.
__________
Limitaciones en la investigación: No hubo limitaciones en la presente investigación.
__________
Acceso a los datos: Los datos e información de esta investigación están presente en el artículo.
___________
Permisos para la publicación: No aplicable.
___________
ID del artículo: 142/JSAAS/2024
___________
Nota del Editor: Journal of the Selva Andina Animal Science (JSAAS). Todas las afirmaciones expresadas en este artículo son únicamente de los autores y no representan necesariamente las de sus organizaciones afiliadas, o las del editor, editores y los revisores. Cualquier producto que pueda ser evaluado en este artículo, o la afirmación que pueda hacer su fabricante, no está garantizado o respaldado por el editor.
Notas de autor
* Dirección de contacto: Universidad Nacional Micaela Bastidas de Apurímac. Facultad de Medicina Veterinaria y Zootecnia. Laboratorio de Farmacología, Toxicología y Bioquímica Veterinaria. Esquina Calle Los Lirios con Álamos s/n. Abancay, Apurímac, Perú.
Ludwing Angel Cárdenas-Villanueva E-mail address: lcardenas@unamba.edu.pe
Enlace alternativo
http://www.scielo.org.bo/scielo.php?script=sci_arttext&pid=S2311-25812025000100058&lng=es&nrm=iso (html)










