La papa (Solanum tuberosum L.) es el cuarto cultivo más importante del mundo, después del arroz, maíz y el trigo, debido a sus propiedades alimenticias y su rápido crecimiento. Sus tubérculos son parte de la dieta alimenticia de millones de personas en todo el mundo (Lim, 2016). En Nicaragua, la papa representa un cultivo de mucha importancia después de los granos básicos y se cultiva en zonas altas de Estelí, Jinotega y Matagalpa. Según el Instituto Nicaragüense de Tecnología Agropecuaria (INTA, 2020), el consumo per cápita en nuestro país es de ocho kilogramos anuales, se siembra entre 800 y 1 200 hectáreas con una producción que satisface entre el 35 % y el 40 % de la demanda nacional.
El cultivo de papa es más apto para cultivarse a altitudes entre 1 500 y 2 500 msnm, pero también puede cultivarse en alturas menores. Se adapta mejor a suelos francos, franco-arenosos, franco-limosos y franco-arcillosos, de textura liviana, con buen drenaje y con una profundidad efectiva (mayor de 0.50 m), que permitan el libre crecimiento de los estolones, tubérculos y faciliten la cosecha. Las temperatura que favorece el desarrollo de tuberculos es de 18°C a 25°C,con una variacion mínima 10 °C entre el día y la noche (Román y Hurtado, 2002).
A pesar de la importancia que tiene el cultivo de papa, este se ve afectado por diversos factores que reducen el rendimiento y calidad de los tubérculos, y elevan los costos de producción. La papa es susceptible a más de 100 enfermedades causadas por diversos organismos como hongos, bacterias, micoplasmas y virus, y problemas fisiológicos (Esquivel, 2017).
La marchitez bacteriana causada por Ralstonia solanacearum [Smith (1896) Yabuuchi et al., 1996], es una de las enfermedades más importantes en el cultivo de papa. Su distribución está registrada desde el sur de Estados Unidos hasta Argentina (Ríos, 2007). Actualmente está ampliamente distribuida en zonas tropicales y subtropicales, esto representa una limitante para la producción, no solo de papa, sino también de maní, tabaco, banano, tomate y otros cultivos. Se estima que las pérdidas económicas exceden los USD 950 millones anuales (Esquivel, 2017).
Los síntomas iniciales inducidos por R. solanacearum consisten en marchitamiento de las hojas más jóvenes en las partes terminales de las ramas durante las horas más calurosas del día. En esta etapa, sólo una o la mitad de una rama se puede marchitar y las plantas parecerán recuperarse por la noche, cuando la temperatura es más fresca. A medida que la enfermedad se desarrolla bajo condiciones favorables, la planta entera se puede marchitar rápidamente y desecarse, aunque las hojas secas se mantengan verdes, conduciendo a marchitamiento general, amarillamiento del follaje, y finalmente a la muerte de la planta (Champoiseau et al., 2009).
Tradicionalmente las cepas de R. solanacearum son clasificadas en cinco razas, de acuerdo con su gama de hospederos y en seis biovares (Bv1, Bv2, Bv3, Bv4, Bv5 y Bv6), según su capacidad metabólica para la utilización de diversas fuentes de carbono relacionados con sus propiedades bioquímicas; es una devastadora enfermedad que afecta varios cultivos hortícolas y en solanáceas es de importancia a nivel mundial y nacional. La capacidad de supervivencia del patógeno y la ocurrencia de infecciones latentes hace que el diagnóstico tenga una importante función en la prevención de la enfermedad (Naranjo y Martínez, 2013).
La resistencia bacteriana es un problema continuo y en aumento, cuando un microorganismo presenta más de un mecanismo de resistencia y tiene la facultad de transmitirlo, no solo a su descendencia, sino a otras bacterias de su misma o diferente especie (Moreno et al., 2009). Las bacterias, por su capacidad de adaptación, pueden desarrollar mecanismos de resistencia a los antibióticos; uno de los mecanismos más utilizados por las bacterias es disminuir la presencia de los antibióticos en su interior, modificando su permeabilidad, esto altera su mecanismo de transporte activo en la membrana celular y genera el mecanismo de eliminación activa del antibiótico. Existe resistencia natural en las bacterias si carecen de sitios diana para el antibiótico (falta de pared celular y ribosomas) y resistencia adquirida, que son modificaciones de la carga genética de la bacteria que aparecen por mutación cromosómica o por mecanismos de transferencia genética (Duarte-Raya y Granados-Ramírez, 2012). Existen métodos para detección de mecanismos de resistencias bacterianas, como micro diluciones en caldos, prueba de difusión de discos de Kirby Bauer, prueba de aproximación de doble disco, prueba de asociación con ácido clavulánico y el método E-test (Echevarría, 1998).
En Nicaragua no existen estudios de mecanismos de resistencia en bacterias fitopatógenas, pero debido al manejo de la enfermedad, principalmente al uso de antibióticos, probablemente existen razas y biovares resistentes. Por tanto, el objetivo de esta investigación es aportar información sobre las razas, biovares y mecanismos de resistencia de R. solanacearum en el cultivo de papa.
MATERIALES Y MÉTODOS
El estudio se realizó de septiembre del 2020 a febrero del 2021 en el laboratorio de microbiología e invernadero de la Universidad Nacional Agraria (UNA), Managua, Nicaragua.
El estudio se realizó en dos etapas, en la primera se colectaron muestras de tejido vegetal y de suelo, para aislar e identificar a R solanacearum; en la segunda etapa se realizaron pruebas bioquímicas para la identificación de biovares, caracterización de razas y determinación de mecanismos de resistencia de R solanacearum.
Colecta de muestras
Para la
obtención de las muestras se seleccionaron plantas que presentaban los síntomas
característicos de marchitamiento por R. solanacearum
tales como marchitez a nivel de follaje, coloración verde pálida en hojas y
caída de las hojas básales seguidos por la marchitez total de la planta (Ríos,
2007). El muestreo se realizó en dos reservas naturales del
departamento de Estelí, ubicadas en la parte central norte del país. Se
colectaron 22 muestras en la Reserva Natural Tisey (154
km al norte de Managua, capital de Nicaragua) y 26 muestras en la Reserva
Natural Miraflor a 192 km de Managua. Las variedades de papa presentes en estas
fincas fueron Granola, Hactri, Evora
y Picasso. Las muestras consistieron en tejido vegetal y suelo; que se
colocaron en bolsas plásticas, con cierre hermético dentro de una hielera para
ser trasladadas al laboratorio de microbiología y fueron almacenadas a 4 oC,
previamente al aislamiento bacteriano.
Aislamiento de R.
solanacearum a partir de muestras de tejido y suelo
Se realizó la prueba de flujo
bacteriano, la que consistió en realizar cortes transversales, desinfectarlos
con hipoclorito de sodio al 1 % y lavarlos con agua destilada estéril (ADE).
Posteriormente los trozos de tallo se sumergieron en ADE y se observó la
presencia o ausencia de un hilo blanco, que consiste en el flujo bacteriano (Perea et al., 2011). Con las muestras de suelo se utilizó la técnica de dilución seriada. Se
preparó una solución madre a partir de 10 g de suelo y 90 ml de agua destilada
estéril, en un Erlenmeyer de 150 ml, a partir de la cual se prepararon las diluciones
10-3, 10-4 y 10-5 (Agrios, 1997).
Identificación de R. solanacearum
El flujo bacteriano obtenido
del tejido vegetal fue inoculado con una asa bacteriológica en el medio de
cultivo agar cloruro de tetrazolium (TZC); las placas
petri fueron incubadas a 30 °C. Después de 48 horas
de incubación se observaron las características macroscópicas (tamaño, forma,
superficie, bordes, color y producción de pigmento) del crecimiento bacteriano
(Kelman, 1954). En el caso de aislamiento de suelo se
utilizaron las diluciones 10-3,
10-4 y 10-5, las que fueron inoculadas el medio de
cultivo agar cloruro de tetrazolium (TZC 1 %), depositando
la cantidad de 100 µl en cada plato petri. Se
realizaron pruebas bioquímicas de oxidasa, catalasa y KOH 3 % para determinar la presencia de la bacteria
según su reacción (Schaad et al., 2001).
Identificación de biovares y razas
Para la identificación de biovares se realizó prueba individual de carbohidratos, observando las reacciones de oxidación–fermentación a partir de los disacáridos Lactosa, Maltosa y Celobiosa, y la oxidación de las hexosas alcohólicas Dulcitol, Manitol y Sorbitol. Los tubos de ensayo que contenían los carbohidratos fueron examinados a los 3, 7, 14 y 28 días después de la inoculación. El cambio de coloración en el medio de purpura a amarillo indicaron resultados positivos (Schaad et al., 2001; French et al., 1995).
Las razas fueron caracterizadas en plantas individuales de tabaco (prueba de hipersensibilidad), se preparó una suspensión bacteriana a partir de cultivos puros con 24-48 horas de incubación y agua destilada estéril hasta obtener una concentración de 1 x 108 UFC (unidades formadoras de colonia), (0.5 solución escala Mackfarland), posteriormente se hicieron orificios sobre el haz de la hoja en zonas intervenales con una aguja hipodérmica N° 29; se inoculó la suspensión bacteriana con una jeringa sin aguja, apoyando la jeringa sobre la superficie de la hoja y presionando por debajo con los dedos. Los resultados se monitorearon en un periodo de 12 a 96 horas, observando síntomas como clorosis, marchitamiento y reacción de hipersensibilidad. Según Lozano y Sequeira (1970) la raza 1 causa clorosis a los dos días después de la inoculación y marchitamiento típico después de 7-8 días, la raza 2 causa clorosis a los dos días después de la inoculación y marchitamiento típico después de 7-8 días, mientras que la raza 3 provoca reacción hipersensitiva 12-24 horas después de la inoculación.
Identificación fenotípica de mecanismos de resistencia bacteriana
Se
realizó mediante prueba de difusión de discos de Bauer et al. (1966) que
consiste en la medición y observación visual del tamaño y forma de los halos de
inhibición producida por la sinergia entre los discos de antibióticos Cefoxitina
(FOX), Cefepima (FEP), Ceftazidima (CAZ) Amoxicilina más ácido clavulánico
(AMC), Ampicilina (AMP), Meropenem (MER), Imepenem
(IMP) e inductor EDTA. Los aislados de R. solanacearum
con ausencia de halo o halo menor a 14 mm indica que son resistentes a
Cefoxitina, debido a la presencia de AmpC; en el caso
de observar aplastamiento en la zona de sinergia con AMC indica resistencia a CAZ
y a FEP, debido a la presencia de betalactamasas de espectro extendido (BLEE).
La utilización en este estudio de Meropenem e Imepinem
fue para descartar la posibilidad de aislados con presencia de Carbapenemasas (Clinical and Laboratory Standards Institute, 2016).
RESULTADOS Y DISCUSIÓN
Identificación de biovares
Se obtuvieron 29 muestras
negativas de R. solanacearum
y 19 aislados positivos, 11 aislados de la Reserva Natural Miraflor y ocho de
la Reserva Natural Tisey; ya que manifestaron reacciones
positivas a las pruebas de oxidasa, catalasa y KOH 3 %, además se caracterizaron
macroscópicamente por las colonias de crecimiento acuoso grandes, blancas y
centro de color rosado en el medio cultivo TZC al 1 % de Kelman.
Estos permitieron identificar 14 aislados pertenecientes al biovar
1, los cuales mostraron reacciones negativas en cada uno de los carbohidratos
utilizados (Lactosa, Maltosa, Celobiosa,
Dulcitol, Manitol y Sorbitol), y cinco identificados como biovar 3 que mostraron
reacciones positivas en cada carbohidrato, según French et al. (1995). En este estudio
tuvo mayor incidencia el biovar 1 en comparación con el biovar
3.
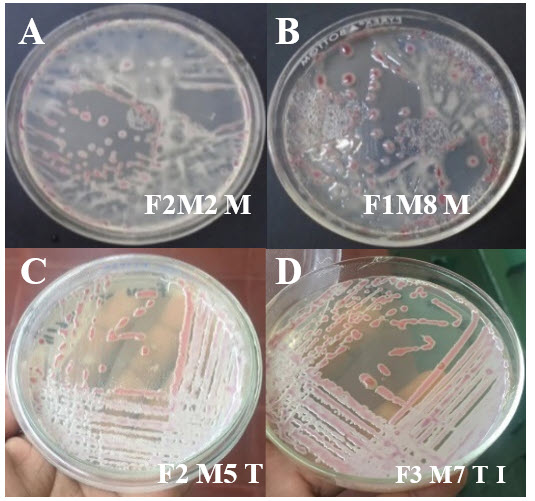 Figura 1.
Aislados de Ralstonia solanacearum
en medio de cultivo TZC 1 %.
Figura 1.
Aislados de Ralstonia solanacearum
en medio de cultivo TZC 1 %.
Caracterización de
razas de Ralstonia solanacearum
Los resultados
de la prueba de hipersensibilidad en planta de tabaco (Lozano y Sequeira 1970),
indican que pasadas 48 horas después de la infiltración se observó clorosis en
la zona infiltrada, ocho días después se observó marchitamiento de las plantas.
Estas características indican que los aislados pertenecen a la raza 1.
 Figura 2.
Caracterización de aislados de R. solanacearum procedentes
de muestras de suelo y tejido
vegetal del cultivo de papa. Clorosis a partir
de las 48 horas posteriores a la
infiltración (A y B), y marchitamiento a partir
de los siete y ocho días
posteriores a la infiltración (C y D).
Figura 2.
Caracterización de aislados de R. solanacearum procedentes
de muestras de suelo y tejido
vegetal del cultivo de papa. Clorosis a partir
de las 48 horas posteriores a la
infiltración (A y B), y marchitamiento a partir
de los siete y ocho días
posteriores a la infiltración (C y D).
Los resultados de este estudio tienen similitud con los datos obtenidos por Ríos (2007), quien determinó mediante pruebas de fermentación-oxidación de carbohidratos e inoculación de plantas de tabaco la presencia de raza 1, biovar 1 y biovar 3 en el cultivo de papa en zonas de Estelí, y la caracterización de razas y biovares de R. solanacearum realizado por Díaz (2005) en Nicaragua, determinó que 20 aislados pertenecían a la raza 1 biovar 3 y siete pertenecían a la raza 2 biovar 3 prevaleciendo en los sitios muestreados el biovar 3.
Estudio realizado por Chavarro y Ángel (2006), en 200 muestras colectadas del cultivo de papa (Solanum tuberosum L.) y plátano (Musa paradisiaca), mediante la técnica NCM-ELISA, determinaron 36 aislamientos de R. solanacearum. Las razas y biovares se determinaron mediante reacción en cadena de la polimerasa (PCR) y secuenciación, obteniendo como resultado agrupaciones correspondientes a la raza 3, biovar 2, en aislados de papa (Solanum tuberosum L.) y agrupaciones de raza 2, biovar 1 en aislamiento de plátano (Musa paradisiaca).
Determinación
fenotípica de mecanismo de resistencia
Se encontró que
12 aislados, ocho aislados de la reserva natural Miraflor y cuatro de la
reserva natural Tisey, no mostraron halos de
inhibición indicando la presencia del fenotipo AmpC hiperproducido (derreprimido) lo que
corresponde a resistencia a Cefoxitina; mientras tanto, siete aislados fueron
susceptibles a los antibióticos utilizados para determinar mecanismos de
resistencia y catalogados como aislados salvajes. No se encontró presencia de
aislados de R. solanacearum con presencia de
Betalactamasas de espectro extendido (BLEE).
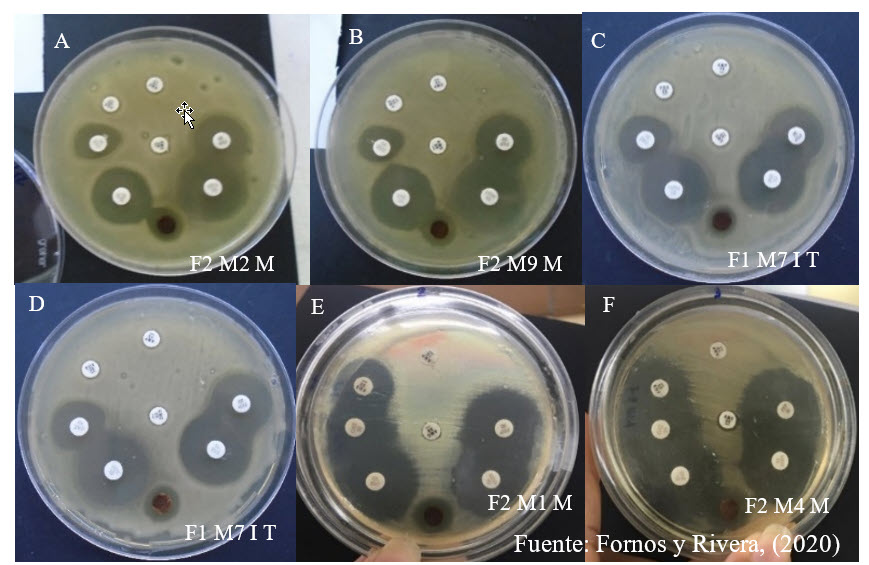 Figura 3.
Aislados
de R. solanacearum
con fenotipos AmpC hiperproducido
(A, B, C y D) y fenotipos salvajes (E y F) aislados de las zonas de
muestreo.
Figura 3.
Aislados
de R. solanacearum
con fenotipos AmpC hiperproducido
(A, B, C y D) y fenotipos salvajes (E y F) aislados de las zonas de
muestreo.
Según Schmidtke y Hanson (2006), se han encontrado en plás-midos genes AmpC de diferentes orígenes genéticos, incluidos C. freundii y M. morganii. El movimiento de estos genes en plásmidos aumentó la prevalencia de este mecanismo de resistencia mediante la diseminación del gen en organismos gramnegativos que naturalmente no portan genes que codifiquen AmpC, como Salmonella spp. y Klebsiella pneumoniae, además confirma que el gen AmpD es un mecanismo involucrado en la sobreproducción de AmpC que conduce a un fenotipo dereprimido y una enzima importante en la vía de reciclaje de la pared célula.
Tans-Kersten et al. (2000), demuestran la presencia del gen AmpD en la bacteria Ralstonia solanacearum, que codifica para la enzima AmpD, que consiste en una amidasa citoplasmática (N-acetilmuramil-L-alanina amidasa), además proponen la posibilidad que AmpD realice otras funciones desconocidas en la célula bacteriana, tales como factor de virulencia para el marchitamiento bacteriano o bien podría funcionar como autolisina durante patogénesis de la marchitez bacteriana.
CONCLUSIONES
De acuerdo con la
prueba de hipersensibilidad, todos los aislados de R. solanacearum obtenidos en las reservas
naturales de Miraflor y Tisey presentaron clorosis 48
horas después de la inoculación y marchitamiento a los siete y ocho días
después de la inoculación, indicando que corresponde a la raza 1. De los aislados
R. solanacearum
obtenidos, 14 corresponden al biovar 1 y 5 al biovar 3 y se identificron 12
aislados de Ralstonia solanacearum
con mecanismo de resistencia AmpC hiperproducido
y siete aislados catalogados como salvajes, se presume que dicho mecanismo de
resistencia identificado en los aislados de R. solanacearum
es adquirido, y posiblemente esté relacionado con una mutación en el DNA del plásmido.
Referencias
Agrios, G. W. (1997). Fitopatología. Academic Press.
Bauer, A. W., Kirby, W. M., Sherris, J. C., y Turck, M. (1966). Antibiotic susceptibility testing by a standardized single disk method. American journal of clinical pathology, 45(4), 493–496. https://doi.org/10.1093/ajcp/45.4_ts.493
Champoiseau, P. G., Jones, J. B., y Allen, C. (2009). Ralstonia solanacearum race 3 biovar 2 causes tropical losses and temperate anxieties. Plant Health Progress, 10(1). https://doi.org/10.1094/PHP-2009-0313-01-RV
Chavarro, M., y Ángel, J. (2006). Establecimiento de un sistema diagnóstico para la detección de Ralstonia solanacearum y diferenciación genética utilizando marcadores moleculares RAPD. Revista Colombiana de Biotecnología, 8(1), 14-31. https://revistas.unal.edu.co/index.php/biotecnologia/article/view/503
Clinical and Laboratory Standards Institute. (2016). Performance standards for antimicrobial susceptibility testing.
Díaz, U. (2005). Caracterización preliminar de razas y biovares de Ralstonia solanacearum (E.F. Smith) Yabuuchi et al., en Nicaragua. La Calera, 5(5). 24-31. https://lacalera.una.edu.ni/index.php/CALERA/article/view/67
Duarte-Raya, F., y Granados-Ramírez, M. (2012). Resistencia antimicrobiana de bacterias en un hospital de tercer nivel. Revista Médica del Instituto Mexicano del Seguro Social, 50(3), 289- 300. https://www.redalyc.org/pdf/4577/457745495012.pdf
Echevarría Zarate, J. (1998). Resistencia bacteriana. Revista Médica Herediana, 9(2), 53-55. https://doi.org/10.20453/rmh.v9i2.2384
Esquivel Solano, M. A. (2017). Evolución de la susceptibilidad a la marchitez bacteriana (Ralstonia solanacearum) en genotipos promisorios y parientes silvestres de la papa en Costa Rica [Tesis de grado, Universidad de Costa Rica]. Repositorio del SIBDI-UCR. http://repositorio.sibdi.ucr.ac.cr:8080/jspui/handle/123456789/3425
French, E., Gutarra, L., y Aley, P. (1995). Medios de cultivo para el aislamiento e identificación de Pseudomonas solanacearum. Centro Internacional de la Papa (CIP).
Instituto Nicaragüense de Tecnología Agropecuaria. (2020). Recomendaciones para la producción de papa en la época de primera 2020. https://inta.gob.ni/wp-content/uploads/2020/04/Recomendaciones-produccion-Papa-DEPARTAMENTAL-ESTELI-2020.pdf
Kelman, A. (1954). The relationship of pathogenicity in Pseudomonas solanacearum to colony appearance on a tetrazolium médium. Phytopathology, 44, 693-695.
Lim, T. K. (2016). Solanum tuberosum. En T. K. Lim (Ed.), Edible Medicinal and Non-Medicinal Plants, (pp. 12-93). Springer. https://doi.org/10.1007/978-3-319-26065-5_2
Lozano, J., y Sequeira, L. (1970). Differentiation of races of by a leaf infiltration tecnique. Phytopathology, 60(5), 833-838. https://www.apsnet.org/publications/phytopathology/backissues/Documents/1970Articles/Phyto60n05_833.pdf
Moreno, C., González, R., y Beltrán, C. (2009). Mecanismos de resistencia antimicrobiana en patógenos respiratorios. Revista de Otorrinolaringología y Cirugía de Cabeza y Cuello, 69(2), 185–192. http://doi.org/10.4067/S0718-48162009000200014
Naranjo, E., y Martínez, Y. (2013). Avances en el diagnóstico de la marchitez bacteriana (Ralstonia solanacearum): situación actual y perspectivas en Cuba. Revista de Protección Vegetal, 28(3), 160–170. http://scielo.sld.cu/scielo.php?script=sci_abstract&pid=S1010-27522013000300001
Perea, S., García, R., Allende, R., Carrillo, J., León, J., Valdez, B., y López, F. (2011). Identificación de razas y biovares de aisladas de plantas de tomate. Ralstonia solanacearum. Revista Mexicana de Fitopatología, 29(2). 98-108. https://www.redalyc.org/pdf/612/61222864002.pdf
Ríos, G. (2007). Distribución y variabilidad de Ralstonia solanacearum E.F. Smith, agente causal de marchitez bacteriana en el cultivo de papa (Solanum tuberosum L), en tres departamentos del norte de Nicaragua (Estelí, Matagalpa y Jinotega) [Tesis de grado, Universidad Nacional Agraria]. Repositorio Institucional UNA. https://repositorio.una.edu.ni/1366/1/tnh20r586.pdf
Román, M., y Hurtado, G. (2002). Cultivo de la papa. Centro Nacional de Tecnología Agropecuaria y Forestal. http://www.centa.gob.sv/docs/guias/hortalizas/Guia%20Papa.pdf
Schaad, N. W., Jones, J. B., y Chun, W. (2001). Laboratory guide for the identification of plant pathogenic bacteria. American Phytopathological Society (APS press).
Schmidtke, A., y Hanson, N. (2006). Model system to evaluate the effect of ampD mutations on AmpC- mediated β-lactam resistance. Antimicrob Agents and Chemother, 50(6), 2030-2037. https://doi.org/10.1128/AAC.01458-05
Tans-Kersten, J., Gay, J., y Allen, C. (2000). Ralstonia solanacearum AmpD is required for wild-type bacterial wilt virulence. Molecular Plant Pathology, 1(3), 179–185. https://doi.org/10.1046/j.1364-3703.2000.00023.x
Notas de autor
1 Graduado, Universidad Nacional Agraria
2 Graduado, Universidad Nacional Agraria
3 MSc. Sanidad vegetal
4 PhD. Entomología
5 MSc. Sanidad vegetal








