Resumen: La falla hepática aguda sobre crónica (ACLF) es un síndrome que se presenta en pacientes con cirrosis descompensada, y se caracteriza por una mortalidad elevada a 28 días, que se diagnostica con la combinación de falla hepática y extrahepática. Se han publicado numerosas definiciones, de las cuales se resalta la realizada por la Asociación Europea para el Estudio del Hígado (EASL), la cual tiene en cuenta 6 sistemas orgánicos (hígado, riñón, pulmón, cerebro, coagulación y circulación), y gradúa su gravedad basada en el número de sistemas comprometidos en el momento de la presentación. Entre los pilares en el abordaje del paciente con ACLF es imperiosa la búsqueda de los factores precipitantes, siendo los más frecuentes las infecciones bacterianas, el consumo excesivo de alcohol, la hemorragia de vías digestivas, la injuria hepática inducida por medicamentos y la cirugía hepática o cirugía mayor, teniendo en cuenta que aproximadamente en el 50 % de los casos no se logrará establecer la causa. Los pilares angulares del tratamiento constarán de la reversión o interrupción del factor precipitante, el soporte orgánico y, en aquellos pacientes que cumplan los criterios para trasplante, su realización oportuna.
Palabras clave: insuficiencia hepática crónica agudizada,falla hepática,cirrosis hepática,trasplante hepático.
Abstract: Acute-on-chronic liver failure is a syndrome that occurs in patients with acute decompensated cirrhosis and is characterized by high 28-day mortality that is diagnosed with a combination of hepatic and extrahepatic organ failure. Numerous definitions have been published with great concern related to the etiology and cause of the decompensation, of which the one made by the European Association for the Study of the Liver (EASL) stands out, taking into account 6 organic systems (liver, kidney, lung, brain, coagulation, and circulation), and grades its severity based on the number of systems involved at the time of presentation. Among the pillars in the approach to the patient with ACLF, the search for precipitating factors is imperative, the most frequent being bacterial infections, excessive alcohol consumption, digestive tract bleeding, drug-induced liver injury, liver surgery or major surgery, keeping in mind that in approximately 50% of cases the cause will not be established. The cornerstones of treatment will consist of the reversal or interruption of the precipitating factor, organ support and, in those patients who meet the criteria for transplantation, its timely performance.
Keywords: acute on chronic liver failure, liver failure, cirrhosis, liver transplant.
Artículos de revisión
Falla hepática aguda sobre crónica
Recepción: 17 Junio 2022
Aprobación: 29 Enero 2023

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
El término falla hepática aguda sobre crónica (ACLF, del inglés, Acute on Chronic Liver Failure) se ha utilizado para definir un síndrome que se observó en pacientes con cirrosis agudamente descompensada, caracterizado por una alta mortalidad a los 28 días [1,2], y que se diagnostica con una combinación de fallas orgánicas, incluidas tanto la hepática como extrahepáticas. El papel de la predicción de ACLF, los factores precipitantes, las fallas de órganos individuales, las estrategias de manejo, el impacto en el trasplante de hígado y la atención al final de la vida está evolucionando [3-5]; por lo que se hace indispensable tanto el reconocimiento de esta entidad como el tratamiento oportuno por parte del personal médico asistencial.
Aunque se han publicado en todo el mundo numerosas definiciones con sistemas de puntuación y pronósticos, que varían respecto a la etiología predominante y la causa de descompensación debido a la variabilidad poblacional, resaltan las definiciones realizadas por la Asociación Europea para el Estudio del Hígado (EASL), el Consorcio de América del Norte para el Estudio de la Enfermedad Hepática en Etapa Terminal (NACSELD) y la Asociación del Pacífico Asiático para el Estudio del Hígado (APASL) [6-8], las cuales se resumen en la tabla 1 [9].
Independiente de los criterios que se utilicen para definir ACLF, existe un consenso en todas las organizaciones internacionales sobre los precipitantes comunes, entre los cuales se destacan la infección viral, ya sea por reactivación o sobreinfección, el sangrado variceal, el consumo de alcohol, el daño hepático inducido por fármacos, la isquemia, cirugía y sepsis [10-14]. Además, otro punto de confluencia entre las distintas organizaciones, radica en la vía desencadenante común hacia la ACLF, que está mediada por la inflamación, provocando falla orgánica y muerte [9,11].
Comparación de las definiciones disponibles para falla hepática aguda sobre crónica. Tomado y adaptado de [9].
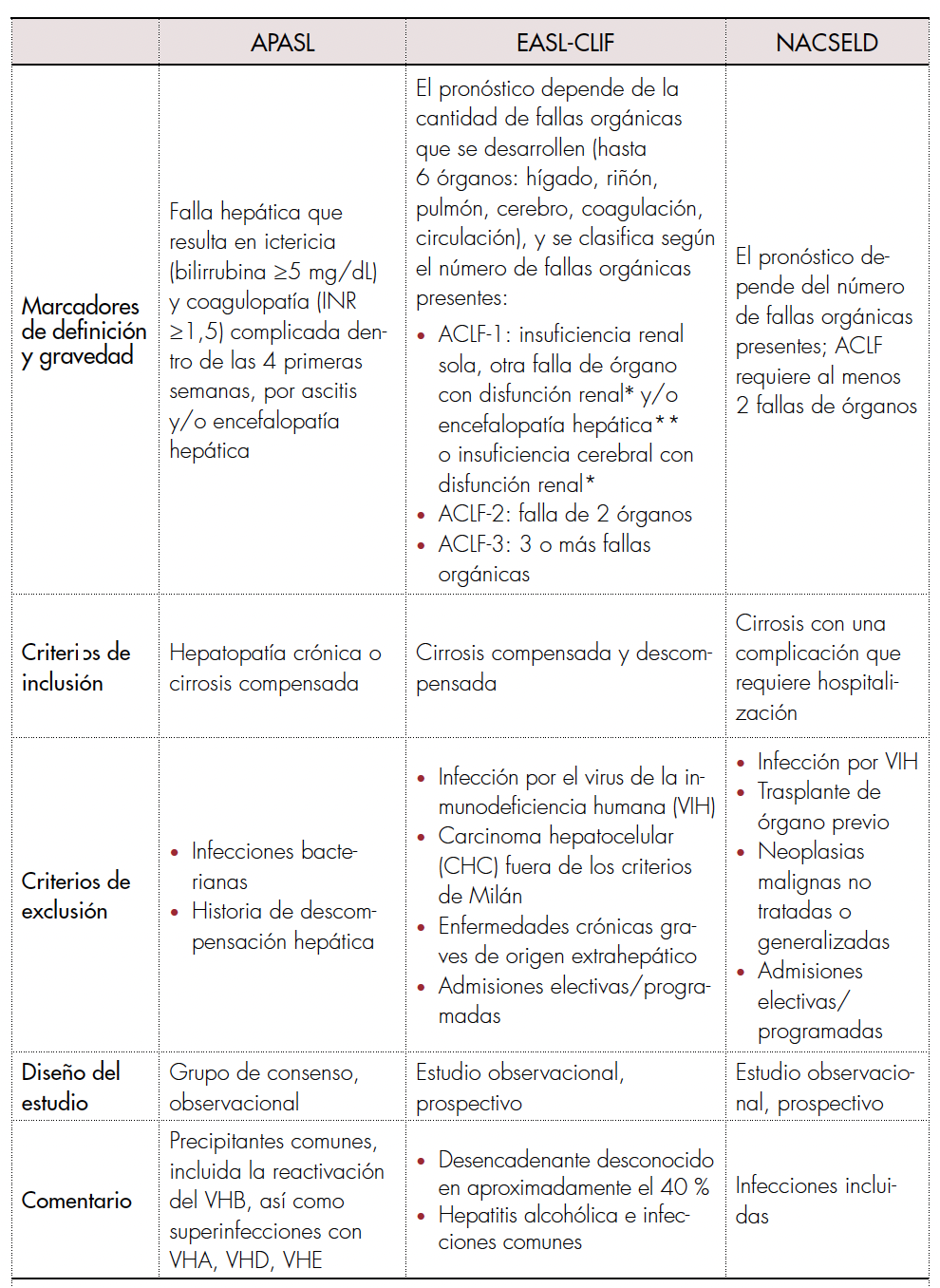
* Disfunción renal definida como una creatinina sérica de 1,5 mg/dL a 1,9 mg/dL.** Encefalopatía hepática definida como grado 1 y 2 de West Haven. APASL: Asociación del Pacífico Asiático para el Estudio del Hígado; EASL-CLIF: Asociación Europea para el Estudio del Hígado-Falla Hepática Crónica; NACSELD: Consorcio de América del Norte para el Estudio de la Enfermedad Hepática en Etapa Terminal; INR: índice internacional normalizado; ACLF: falla hepática aguda sobre crónica; VHA: virus de la hepatitis A; VHB: virus de la hepatitis B; VHD: virus de la hepatitis delta; VHE: virus de la hepatitis E.
La gravedad de la falla orgánica puede evaluarse mediante la puntuación de falla orgánica EASL-CLIF o la puntuación de falla orgánica NACSELD [15], presentadas en la tabla 2 [3]. Los diferentes consorcios y guías de clasificación recomiendan que los pacientes con ACLF sean manejados en una unidad de cuidados intensivos (UCI) [1,3,16]. No obstante, las tasas de mortalidad en la UCI siguen siendo altas en ciertos grupos de pacientes, y se pueden utilizar algunos factores adicionales para guiar el ingreso de estos pacientes a las UCI. Como recomendación adicional, algunos de estos pacientes pueden beneficiarse de un trasplante de hígado temprano [17-19].
Variabilidad en la definición de falla orgánica. Tomado y adaptado de [3].
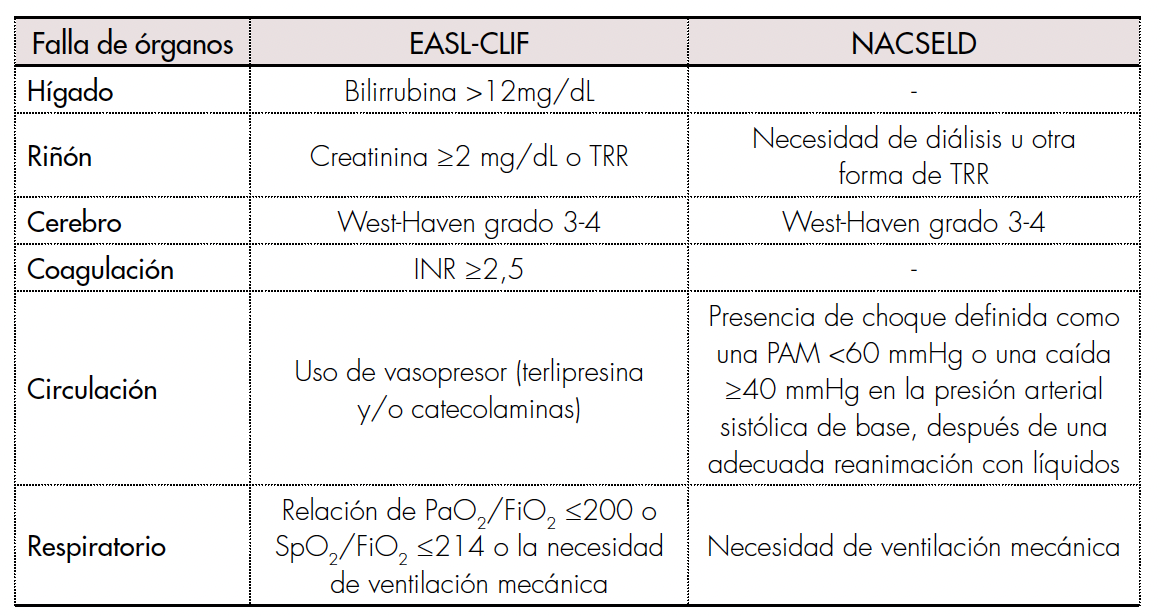
EASL-CLIF: Asociación Europea para el Estudio del Hígado-Falla Hepática Crónica; NACSELD: Consorcio de América del Norte para el Estudio de la Enfermedad Hepática en Etapa Terminal; TRR: terapia de reemplazo renal; INR: índice internacional normalizado; PAM: presión arterial media; PaO2: presión parcial de oxígeno; FiO2: fracción inspirada de oxígeno; SpO2: saturación de oxígeno en sangre.
Los eventos precipitantes para el desarrollo de ACLF varían según las áreas geográficas y pueden clasificarse como hepáticos o extrahepáticos [20] (tabla 3). Se reconoce, por ejemplo, que los datos en población asiática ubican como causas primarias de descompensación a la reactivación del virus de la hepatitis B (VHB), la infección aguda por el virus de la hepatitis A (VHA) o el virus de la hepatitis E (VHE) [21-23], mientras que en la población occidental se destacan el alcoholismo activo, el sangrado variceal y las infecciones bacterianas [24,25], sin embargo, en ambos grupos poblacionales existe una proporción considerable de pacientes en los cuales no hay un evento precipitante reconocible [26,27].
Factores precipitantes de falla hepática aguda sobre crónica (ACLF).

DILI: lesión hepática inducida por fármacos; TIPS: derivación portosistémica transyugular intrahepática (por sus siglas en inglés).
Es bien conocido que los principios fundamentales del tratamiento se basan en la detección y reconocimiento del evento precipitante y la terapia de soporte a las fallas orgánicas documentadas [13]. Realizar un manejo basado en una estrategia estructurada por pasos facilitará el manejo de estos pacientes:
- 1.
Dia
Diagnóstico deACLF. En este punto es primordial realizar una anamnesis, un examen físico y paraclínicos encaminados a la documentación de la enfermedad hepática crónica o cirrosis y del factor precipitante del evento.
- 2. Admisión a unidad de cuidados intensivos o especializados [28,29].
- 3. Nutrición, manteniendo la ingesta calórica de 35 cal/kg/día a 40 cal/kg/día, que incluya una ingesta de proteína entre 1,2 g/kg/día a 2 g/kg/día. En aquellos pacientes que no pueden satisfacer sus necesidades nutricionales vía oral, la nutrición enteral es la mejor opción. La nutrición parenteral queda reservada para aquellos pacientes cuyas necesidades nutricionales no pueden satisfacerse por el tracto gastrointestinal o en aquellos con vía aérea no asegurada con compromiso del estado de consciencia, como en pacientes con encefalopatía hepática grado 3-4 [3,30].
- 4. Confirmación de la causa desencadenante para realizar tratamiento específico, recordando que hasta en un 50 % de los casos no se logrará encontrar el factor precipitante [9,30].
- 5. Prevención y manejo de la falla orgánica.
- 6. Decisión de trasplante y referencia a centro especializado en esto, en pacientes seleccionados [31,32].
- 7. Opciones de manejo, para aquellos pacientes no candidatos a trasplante [30].
Los factores precipitantes, para fines prácticos y de tratamiento, podrían clasificarse en extrahepáticos, de los cuales los más importantes son las infecciones y la hemorragia variceal aguda; y hepáticos, en los que se destacan la hepatitis alcohólica severa y la falla hepática aguda sobre crónica relacionada con VHB [33,34].
Es la principal causa de ACLF en países occidentales. Entre las infecciones más frecuentes en pacientes con cirrosis se encuentran: peritonitis bacteriana espontánea (23 %), infección del tracto urinario (19 %), infecciones de piel y tejidos blandos (10 %), infecciones respiratorias (9 %) e infecciones por C. difficile (5 %) [3].
En una cuarta parte de los pacientes no se logra documentar el patógeno causal y la fuente de infección, en un 33 % de los casos se reporta que son causadas por bacterias Gram positivas, y en un 27 % por Gram negativas [3,35].
Inicialmente se deben administrar antibióticos de amplio espectro, idealmente en la primera hora en pacientes con choque o ACLF 3, recordando que no se puede retrasar el inicio de la terapia antimicrobiana cuando existen atrasos en la toma de cultivos [36]; a su vez, es imperioso el ajuste del tratamiento empírico al patrón epidemiológico de resistencia local, la aplicación de estrategias de optimización farmacocinéticas como las infusiones extendidas o continuas de algunos betalactámicos, y el ajuste y desmonte de la terapia antimicrobiana dirigida por los resultados del cultivo. Una estrategia razonable de tratamiento antimicrobiano empírico se resume en la tabla 4.
Tratamiento empírico en pacientes con falla hepática aguda sobre crónica. Tomado y adaptado de [37].
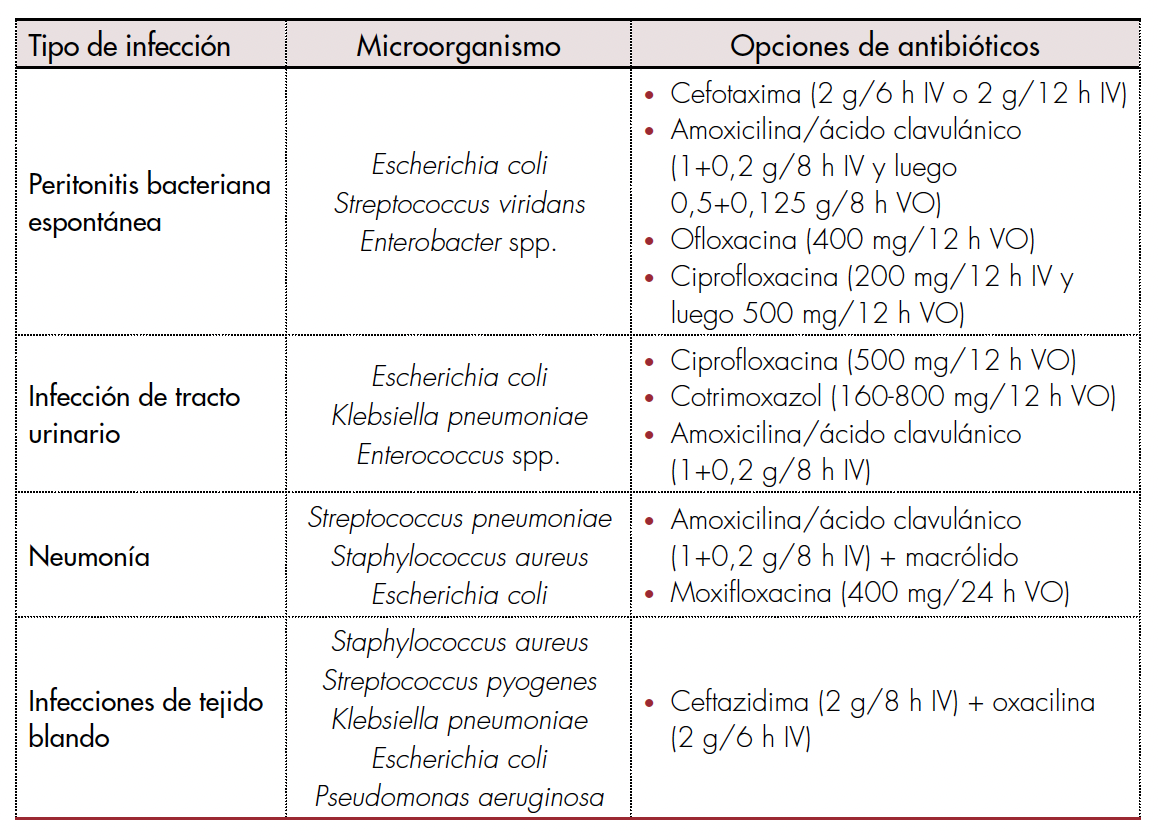
Para el manejo de la hemorragia variceal aguda se utilizará la combinación de vasoconstrictores como terlipresina, con dosis máxima de 2 mg intravenoso (IV) cada 4 horas con titulación según respuesta, o somatostatina 250 mg en bolo IV seguido de una infusión de 250 mg/hora, o análogos como el octreotide 50 µg en bolo IV seguido de infusión de 50 µg/hora, los cuales se administrarán desde el momento del ingreso y se mantendrán durante 3 a 5 días, sumado a la terapia endoscópica preferiblemente con ligadura variceal realizada en las primeras 12 horas de admisión hospitalaria. Esta terapia será acompañada de profilaxis antibiótica con ceftriaxona 1 g IV cada 24 horas durante 5 a 7 días, o ciprofloxacina 500 mg cada 12 horas por 7 días [34].
Es importante tener en cuenta que la ACLF surge como factor de riesgo independiente aumentando la mortalidad y duplicando el riesgo de sangrado recurrente por várices. Sin embargo, en un estudio reciente se sugiere que una derivación portosistémica transyugular intrahepática (TIPS) preventiva, podría mejorar la supervivencia de los pacientes con hemorragia aguda por várices y ACLF [38]. No obstante, se necesitan más estudios para validar el papel de los TIPS preventivos en estos pacientes [1,13,38].
En estos casos, el manejo de primera línea es con corticoides como prednisolona 40 mg vía oral (VO) por día, o en aquellos pacientes sin disponibilidad de la vía oral se usará metilprednisolona 32 mg IV por día, teniendo en cuenta que debe evitarse su uso en pacientes con hepatitis B, tuberculosis o infección activa, haciendo búsqueda sistemática de estas previo a su uso. La respuesta a los corticoides se puede evaluar con el puntaje de LILLE entre 4 y 7 días después del inicio de la terapia, considerando que puntajes mayores de 0,45 indican poca o nula respuesta terapéutica, por lo cual se suspendería el tratamiento, y en caso de obtener respuesta, se continuaría hasta el día 28 con desmonte paulatino a partir de esa fecha [1,39].
Se debe realizar inicio oportuno de análogos de los nucleótidos/nucleósidos para disminuir rápidamente la carga viral y la consecuente muerte hepatocelular, con mejoría en la supervivencia [1]. El tratamiento consta de entecavir 0,5 mg/día, tenofovir disoproxil fumarato 300 mg/día, o en pacientes con tasa de filtración glomerular <60 mL/min, tenofovir alafenamida 25 mg/día [40].
La lesión renal aguda (LRA) es el compromiso orgánico más comúnmente encontrado en pacientes con ACLF [41]. Para su definición, se recomienda la utilización de los criterios de KDIGO modificados por el Club Internacional de Ascitis (CIA), los cuales se muestran en la tabla 5 [9]. Su severidad será definida por estadios; aquellos con estadios ≥2 son catalogados como falla renal por la EASL-CLIF [3].
Los pacientes que además de ser estadios 2 o 3 de LRA por los criterios del CIA, cumplan otros criterios como no presentar mejoría de creatinina (descenso de ≤0,3 mg/dL de la basal) luego de al menos 48 horas de haber suspendido un diurético, y expansión de volumen con albúmina a 1 g/kg/día por 2 días, ausencia de choque hipovolémico, sin uso reciente de nefrotóxicos, proteinuria <500 mg/día sin microhematuria (<50 glóbulos rojos/mL), y ecografía renal normal, serán clasificados como síndrome hepatorrenal-lesión renal aguda (SHR-LRA), anteriormente denominado como síndrome hepatorrenal tipo 1 [3,42].
El tratamiento de la falla renal consistirá en la administración de albúmina al 20 % a 1 g/kg IV durante 48 horas y luego de 20 g/día a 40 g/día en asociación a terlipresina 2 mg IV cada 24 horas en infusión continua, o bolos de 1 mg cada 6 horas con continuación de tratamiento hasta por dos semanas [43,44], o en caso de no disponibilidad, norepinefrina a dosis titulable con objetivo de presión arterial media (PAM) entre 75 mmHg a 80 mmHg. Se debe evitar el inicio de terapia de reemplazo renal temprana, su uso generalmente está recomendado para aquellos pacientes con SHR-LRA como terapia puente, mientras se está a la espera de trasplante hepático. Se debe suspender y evitar en la medida de lo posible, drogas nefrotóxicas como los AINE y diuréticos [1].
Criterios KDIGO modificados por el Club Internacional de la Ascitis (CIA) para lesión renal aguda (LRA). Tomado y adaptado de [9].

KDIGO: por sus siglas en inglés, Kidney Disease Improving Global Outcomes; TRR: terapia de reemplazo renal.
Inicialmente se puede optar por el uso de lactulosa y enemas para manejo de la encefalopatía hepática [45], sin embargo, en aquellos pacientes con alteración del estado mental marcado, se debe iniciar manejo y aseguramiento de la vía aérea para evitar neumonía por aspiración, usar protocolos de sedación con agentes de acción corta como la dexmedetomidina, y evitar sedación profunda, el uso de fármacos como las benzodiacepinas, opiáceos o los bloqueadores neuromusculares [46].
En estos pacientes es primordial la búsqueda de causas alternativas de la alteración del estado mental, dado que aparte de la hiperamonemia causante de la encefalopatía hepática, también pueden concurrir otras condiciones que podrían explicar la alteración del estado mental, como trastornos hidroelectrolíticos, infecciones, fármacos y eventos cerebrovasculares, entre otros [3].
Se recomienda el uso de ventilación protectora con volumen tidal (corriente) bajo, presiones plateau <30 cmH2O, presión positiva al final de la espiración (PEEP) para pacientes con síndrome de dificultad respiratoria aguda (SDRA) inducido por sepsis con una PEEP óptima superior a 5 mmHg, pronación temprana, protocolos de desmonte ventilatorio y elevación de la cabecera a 30° a 45° [1].
En aquellos pacientes definidos por la EASL-CLIF con falla circulatoria, se recomienda una PAM objetivo ≥65 mmHg (75 mmHg en caso de SHR) con el uso de cristaloides balanceados [47], albúmina al 5 % y vasopresores, siendo el de primera línea la norepinefrina. En caso de requerir la adición de un segundo vasopresor, se pueden considerar la epinefrina o la terlipresina. En casos de choque refractario, se puede utilizar hidrocortisona 200 mg IV al día, especialmente en aquellos pacientes con dosis de norepinefrina >0,5 µg/kg/min [1,47]. Se debe tener precaución con el uso de solución salina en aquellos pacientes con anasarca o ascitis.
Otras consideraciones a tener en cuenta es el uso de albúmina en pacientes a quienes se les realizará paracentesis de grandes volúmenes (más de 5 L) para evitar la disfunción circulatoria, en estos casos se administra albúmina al 20 % a dosis de 6 g/L a 8 g/L de líquido ascítico removido, contando a partir del primer litro [48].
Se recomienda usar una estrategia restrictiva (transfundir solo si la Hb es <7 mg/dL con una meta postransfusión de 7 g/dL a 9 g/dL) para pacientes en estado crítico con ACLF [47,49], exceptuando a los que presentan isquemia miocárdica severa [34,47,50].
Se recomienda tener un nivel de fibrinogenemia por encima de 100 mg/dL, por lo que se deberá administrar fibrinógeno en casos de hipofibrinogenemia severa, y/o transfusión de plaquetas en caso de trombocitopenia crítica <10.000/µL, infección activa con recuento plaquetario <20.000/µL, o en pacientes que serán sometidos a procedimientos y que tienen recuentos <50.000/µL [34,51].
La tromboprofilaxis para enfermedad tromboembólica venosa se realizará preferiblemente con heparinas de bajo peso molecular siempre y cuando no existan contraindicaciones como sangrado reciente y/o trombocitopenia significativa (<50.000/µL o 30.000 a 50.000/µL en casos seleccionados), de lo contrario se optará por medidas mecánicas como tromboprofilaxis [3,47].
Se recomienda la administración de plasma fresco congelado (PFC) a 10 mL/kg solo cuando persista sangrado y el índice internacional normalizado (INR) sea >1,5 o el TPT sea >32 segundos [50], debe tenerse en cuenta que no se recomienda la corrección de alteraciones en el INR en ausencia de sangrado.
El trasplante sigue siendo la terapia definitiva en pacientes con ACLF sin tratamiento exitoso, sin embargo, esto no es factible en muchos casos dado su alto costo y escasez de donantes; por ende, es menester una evaluación crítica de la indicación de este [52].
Los pacientes con ACLF grado 1 y 2 tienen una tasa de supervivencia postrasplante similar a aquellos sin ACLF; en contraposición, aquellos con ACLF grado 3, cuya tasa de supervivencia oscila entre 44 % y 83 %, también pueden experimentar mayor tasa de complicaciones como infecciones, complicaciones neurológicas, complicaciones biliares, de la vasculatura hepática, y una estadía más prolongada en la UCI [53].
Entre los predictores de mal pronóstico postrasplante, se ha documentado la ventilación mecánica, mayor índice de riesgo del donante, trasplante hepático realizado posterior a 30 días de ingresar a la lista de espera y principalmente la terapia de reemplazo renal [53].
Para la toma de decisión de los pacientes que pueden ser candidatos, se debe considerar la reserva del paciente para sobrevivir al periodo preoperatorio, operatorio y posoperatorio, sumado a una calidad de vida significativa postrasplante [3,13].
Actualmente, la elección de los candidatos continúa siendo materia de investigación con estrategias de elección individualizadas y la participación de un equipo multidisciplinar en el área competente.
La falla hepática aguda sobre crónica es una enfermedad sistémica que se asocia a falla orgánica y afecta a pacientes con enfermedad hepática crónica avanzada, confiriéndoles un pronóstico ominoso, a su vez, determinado por el número de sistemas orgánicos comprometidos en su presentación. Es un reto su identificación y diagnóstico, por lo que han surgido múltiples definiciones que tienen como finalidad una identificación temprana, que permita establecer un manejo oportuno basado en la identificación de infecciones y factores precipitantes susceptibles de interrupción, en compañía de medidas de soporte orgánico. Durante el curso y evolución de esta entidad, es imperioso realizar evaluaciones continuas para identificar aquellos pacientes que son candidatos a trasplantes. Aún están en investigación la utilidad de múltiples medidas farmacológicas y no farmacológicas, que permitan enriquecer el arsenal terapéutico y mejorar el pronóstico de estos pacientes.
Comparación de las definiciones disponibles para falla hepática aguda sobre crónica. Tomado y adaptado de [9].

* Disfunción renal definida como una creatinina sérica de 1,5 mg/dL a 1,9 mg/dL.** Encefalopatía hepática definida como grado 1 y 2 de West Haven. APASL: Asociación del Pacífico Asiático para el Estudio del Hígado; EASL-CLIF: Asociación Europea para el Estudio del Hígado-Falla Hepática Crónica; NACSELD: Consorcio de América del Norte para el Estudio de la Enfermedad Hepática en Etapa Terminal; INR: índice internacional normalizado; ACLF: falla hepática aguda sobre crónica; VHA: virus de la hepatitis A; VHB: virus de la hepatitis B; VHD: virus de la hepatitis delta; VHE: virus de la hepatitis E.
Variabilidad en la definición de falla orgánica. Tomado y adaptado de [3].

EASL-CLIF: Asociación Europea para el Estudio del Hígado-Falla Hepática Crónica; NACSELD: Consorcio de América del Norte para el Estudio de la Enfermedad Hepática en Etapa Terminal; TRR: terapia de reemplazo renal; INR: índice internacional normalizado; PAM: presión arterial media; PaO2: presión parcial de oxígeno; FiO2: fracción inspirada de oxígeno; SpO2: saturación de oxígeno en sangre.
Factores precipitantes de falla hepática aguda sobre crónica (ACLF).

DILI: lesión hepática inducida por fármacos; TIPS: derivación portosistémica transyugular intrahepática (por sus siglas en inglés).
Tratamiento empírico en pacientes con falla hepática aguda sobre crónica. Tomado y adaptado de [37].

Criterios KDIGO modificados por el Club Internacional de la Ascitis (CIA) para lesión renal aguda (LRA). Tomado y adaptado de [9].

KDIGO: por sus siglas en inglés, Kidney Disease Improving Global Outcomes; TRR: terapia de reemplazo renal.


