Resumen: El trasplante de hígado es el último recurso para el tratamiento de hepatopatías. Para evitar el rechazo del injerto se requieren esquemas de inmunosupresión que han ido evolucionando a lo largo de los años. Se realizó una revisión bibliográfica en la base de datos PubMed sobre las terapias inmunosupresoras disponibles para evitar el rechazo del injerto en el trasplante hepático, los esquemas utilizados, efectos adversos, interacciones y sus modificaciones desde la fase de inducción hasta el seguimiento posterior. Se encontró que la inducción habitual es con esteroides o terapia inmunológica clonal. En el mantenimiento, los inhibidores de la calcineurina son los más utilizados, las dosis se deben ajustar según sus niveles séricos y la presencia de efectos adversos como nefrotoxicidad o diabetes. Por otra parte, los inhibidores del mTOR han sido considerados como agentes reductores del riesgo de recidiva de cáncer hepatocelular. Las características del paciente y sus comorbilidades (embarazo, insuficiencia renal, diabetes, sepsis, carcinoma hepatocelular) requieren modificar el tratamiento e individualizarlo.
Palabras clave: trasplante de hígado,inmunosupresión,inmunoterapia,rechazo de injerto,inhibidores,calcineurina,rapamicina,esteroides.
Abstract: Liver transplantation is the last option for the treatment of liver disease. Immunosuppression schemes are required to avoid graft rejection, which have evolved over the years. A literature review was carried out in PubMed on the immunosuppressive therapies available to avoid graft rejection in liver transplantation, as well as on the schemes used, adverse effects, interactions and their modifications from the induction phase to subsequent follow-up. The usual induction was found to be with steroids or clonal immune therapy. In maintenance, calcineurin inhibitors are the most widely used, and their doses should be adjusted according to their serum levels and the presence of adverse effects such as nephrotoxicity or diabetes. On the other hand, mTOR inhibitors have been considered to reduce the risk of hepatocellular cancer recurrence. The characteristics of the patient and their comorbidities (pregnancy, kidney failure, diabetes, sepsis, hepatocellular carcinoma) require modification and individualization of the treatment.
Keywords: liver transplant, immunosuppression, immunotherapy, graft rejection, inhibitors, calcineurin, rapamycin, steroids.
Artículos de revisión
Protocolo de inmunosupresión en trasplante hepático: revisión de la literatura
Recepción: 21 Agosto 2021
Aprobación: 22 Noviembre 2021

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
El trasplante hepático está indicado para el tratamiento de la falla hepática aguda, la insuficiencia hepática crónica, la cirrosis hepática y los disturbios metabólicos que son potencialmente corregibles mediante este medio [1,2], por lo tanto, es el único manejo definitivo para pacientes con enfermedad hepática cuyo tratamiento farmacológico no es eficiente, o en el caso del carcinoma hepatocelular (CHC) como coadyuvante de las diferentes opciones o como terapia definitiva. Los medicamentos inmunosupresores modulan la respuesta del sistema inmune y tienen por objetivo prevenir o revertir el rechazo del injerto.
Es de fundamental importancia buscar el equilibrio entre la máxima efectividad para evitar el rechazo y obtener una supresión del sistema inmune que mantenga el control contra infecciones y neoplasias, evitando a la vez la toxicidad directa de los agentes inmunosupresores. Como consecuencia de la evolución de los protocolos de inmunosupresión, la incidencia del rechazo agudo del injerto ha disminuido progresivamente [3]. Actualmente, la mayoría de los casos de rechazo son controlados con el aumento de la dosis de tacrolimus o administración de bolos de corticoides, sin embargo, la inmunosupresión puede estar afectada por distintas comorbilidades, siendo necesario valorar la mejor terapia inmunosupresora de manera individual. El objetivo de esta revisión consiste en indagar sobre las terapias inmunosupresoras disponibles, los efectos adversos, y las modificaciones desde la fase del trasplante hasta el seguimiento posterior.
Se realizó una búsqueda bibliográfica en PubMed sobre inmunosupresión en trasplante hepático según el esquema que se observa en la figura 1. Se utilizaron los siguientes términos MeSH: (inmunosuppression OR therapy, anti-rejection OR antirejection therapy) AND (liver transplantation, OR transplantation, liver OR liver transplantation OR transplantation, liver graftings OR hepatic transplantation OR transplantation, hepatic). Se incluyeron todas las revisiones sistemáticas, los metaanálisis y los estudios clínicos aleatorizados, más 3 artículos de la lista de referencias.
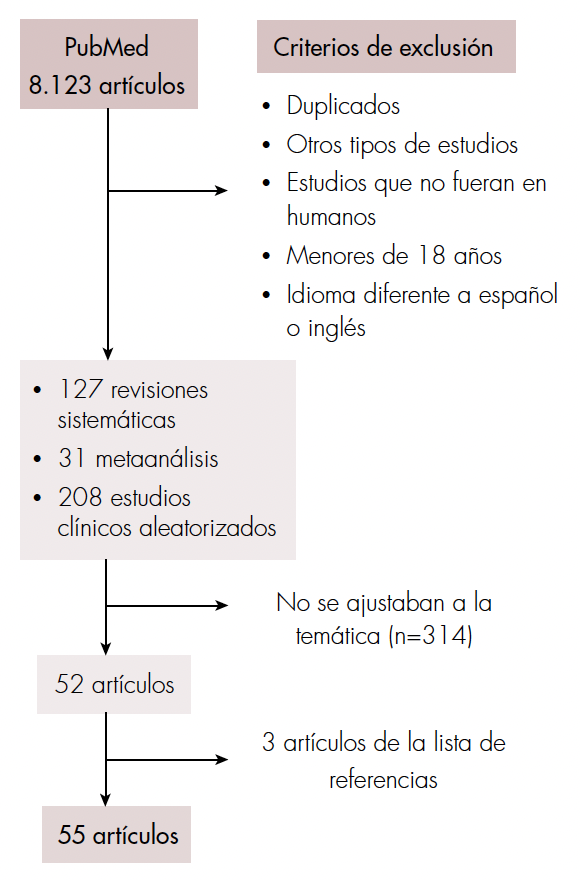
Figura 1.
Diagrama de flujo de búsqueda de la información.
Los avances en la terapia de inmunosupresión han reducido la tasa de rechazo agudo, y a pesar de sus efectos adversos, han aumentado la supervivencia después del trasplante hepático. Uno de los fármacos más importantes son los inhibidores de la calcineurina (ICN), los cuales se convirtieron en la primera línea de tratamiento en la mayoría de los centros de trasplante. Actualmente se reducen gradualmente los glucocorticoides, y tacrolimus se utiliza a largo plazo; no obstante, entre sus efectos menos deseados están la nefrotoxicidad y el desarrollo de neoplasias malignas de novo. A continuación se explican los grupos más importantes de inmunosupresores con sus interacciones y efectos adversos.
Son los principales medicamentos utilizados en la terapia de inmunosupresión para la conservación del trasplante hepático. Corresponden a la ciclosporina y al tacrolimus.
Es un potente inmunosupresor utilizado en trasplantes de órganos sólidos desde la década de los 70 [4]. Su acción depende de la formación de un complejo con su receptor ciclofilina que inhibe la actividad de la fosfatasa calcineurina, resultando en la inhibición de la expresión de genes de proteínas nucleares involucradas en la activación celular y en la formación del linfocito T citotóxico [4]. Como resultado, se inhibe la producción de citocinas como la interleucina-2 (IL-2), la interleucina-4 (IL-4) y el interferón-γ (IFN-γ) [5].
La ciclosporina es absorbida en el yeyuno y ampliamente distribuida por la sangre, con un pico de concentración en el plasma entre 3 a 5 horas posterior a su administración. En la sangre se concentra en los eritrocitos en un 41% a 58%, en el plasma 33% a 47%, en los leucocitos 5% a 12%, y en los linfocitos 9%. En el plasma, aproximadamente el 90% se une a proteínas, principalmente lipoproteínas, teniendo una vida media de 18 horas. La eliminación es predominantemente biliar, y en apenas un 6% es excretada por la orina.
También conocido como FK506, tiene la propiedad de inhibir la actividad de la calcineurina, uniéndose a una proteína inmunofilina, la FK506-binding protein 12 (FKBP12), interfiriendo en la vía de traducción de la señal de inmunoactivación de las células T [6]. Fue introducido como agente inmunosupresor en el inicio de la década de los 90, e inicialmente ideado para trasplante de hígado [4,7]. Su efecto in vitro es 10 a 100 veces mayor que la ciclosporina, y por lo tanto, su nivel sérico terapéutico es aproximadamente 20 veces menor [8]. Su biodisponibilidad oral es variable (5% a 67%), siendo la mejor absorción en condiciones de ayuno. Sin embargo, su eficacia por vía oral (VO) es mayor que la ciclosporina, por lo que se ha convertido en el ICN más utilizado en los protocolos de inmunosupresión, generalmente en combinación con corticoides [9,10]. Su uso ha favorecido la disminución progresiva de la incidencia del rechazo agudo al injerto, así como también ha permitido revertir este rechazo mediante el incremento de su dosis o por la administración de bolos de corticoides [11].
Algunos medicamentos a través de su interacción con el citocromo P450, aumentan los niveles sanguíneos de los ICN, tales como antibióticos (claritromicina, eritromicina, azitromicina), antifúngicos (itraconazol, ketoconazol, voriconazol, clotrimazol), bloqueadores de canales de calcio (verapamilo, diltiazem, nifedipino), y otros como metoclopramida, amiodarona, cimetidina e inhibidores de la bomba de protones (IBP). Por el contrario, otros medicamentos disminuyen los niveles de los ICN, entre ellos, antibióticos (rifambutina, rifampicina) y anticonvulsivantes (carbamazepina, fenobarbital y fenitoína).
Los ICN poseen efectos tóxicos, muchos de ellos dependientes de la dosis. Un importante efecto adverso es la nefrotoxicidad, registrándose insuficiencia renal crónica en cerca del 20% de los trasplantados de hígado en 5 años. Puede presentarse agitación, confusión con alucinaciones o psicosis, hipertensión arterial, dislipidemia, hiperpotasemia, acidosis metabólica y diabetes mellitus, todos ellos efectos adversos bastante comunes. La diabetes es más frecuente con tacrolimus, mientras que la hipertensión y la dislipidemia son más comunes con ciclosporina [4,12]. Otro efecto, aunque menos probable, es la hiperpotasemia.
Un importante aspecto que debe ser resaltado con los ICN es su relación con el factor-ß transformador de crecimiento (TGF-ß), una citocina que estimula la fibrosis y el crecimiento tumoral por aumento de la transcripción, especialmente ante el uso en conjunto de los ICN, con una mayor posibilidad de recurrencia de CHC o surgimiento de enfermedad linfoproliferativa postrasplante.
Es un inhibidor de mTOR (del inglés, Mammalian Target of Rapamycin) ampliamente usado en el trasplante renal, sin embargo, hace pocos años recibió la aprobación de la FDA (del inglés, Food and Drug Administration) para ser usado en la profilaxis del rechazo en el trasplante hepático [4]. Asimismo, es un derivado del 2-hidroxietil del sirolimus que tiene efectos antiproliferativos e inmunosupresores. Al igual que los ICN, también se une a la proteína FKBP12 (reguladora del crecimiento celular), y posteriormente a mTOR para bloquear la traducción de la señal asociada a la quinasa p70S [6], que es clave en la transducción de las señales que llevan a la síntesis del ADN [12]. Este mecanismo resulta en la interrupción del ciclo celular entre las fases G1 a S [12,13]. Asimismo, la inhibición de mTOR bloquea las funciones de los linfocitos T CD4+ y CD8+, la activación de monocitos, y la proliferación y diferenciación de las células B [12]. A diferencia de los ICN, no interfieren con la apoptosis de las células T.
Además de lo mencionado, los ImTOR actúan de manera sinérgica con los ICN, ya que estos últimos actúan en la fase precoz y se complementan con la acción en la fase tardía del EVR [14]; por lo tanto, dosis reducidas de ICN sumadas a EVR pueden ser utilizadas para obtener un efecto inmunosupresor más potente, al permitir la prevención de un rechazo agudo del injerto, reduciendo a la vez sus efectos adversos y posibilitando la preservación de la función renal del paciente trasplantado. El planteamiento de la asociación debe ajustarse de acuerdo a los niveles séricos. EVR debe ser administrado a partir de los 30 a 60 días del postoperatorio, debido a los efectos que tiene en la cicatrización, tasas de hernia incisional y linfocele; sin embargo, estudios recientes reportan que a bajas dosis se minimizan estos efectos [15].
Por otra parte, los ImTOR reducen la expresión del receptor del factor de crecimiento epitelial (EGFR) y su señalización, así como también inhiben la producción del factor de crecimiento del epitelio vascular (VEGF) [16,17], lo que confiere a estos agentes propiedades antineoplásicas.
Estudios clínicos sugieren que la inmunosupresión por ImTOR puede reducir la recidiva de CHC en el postrasplante [18-21]. No obstante, en otro estudio clínico aleatorizado doble ciego, no se encontró una mejora en la sobrevida de los pacientes con CHC avanzado que usaron EVR [22]. A pesar de que varios centros de trasplante ya están utilizando los ImTOR en sus protocolos para los receptores con CHC [13], todavía faltan más estudios clínicos prospectivos controlados y aleatorizados para la comprobación de la efectividad en este subgrupo.
El EVR es rápidamente absorbido por vía oral, alcanzando el pico de concentración entre 1 a 2 horas, pudiendo ser retardada su absorción por alimentos con elevada cantidad de grasa. Cerca del 80% de su eliminación ocurre en la bilis y 5% en la orina, siendo esta útima casi 20% mayor en pacientes de raza negra. Su vida media es aproximadamente de 30±11 h (rango 19-53), teniendo un tiempo de estabilización sanguínea de 4 días. Es metabolizado en el hígado por el citocromo P450, por lo que fármacos que inhiben o compiten con este sistema, por ejemplo, la azitromicina y los IBP, pueden reducir su depuración, ocasionando aumento de sus niveles séricos [23].
Los efectos adversos son dependientes de la dosis e incluyen dislipidemia, trombocitopenia, anemia y leucopenia. No ocasionan neurotoxicidad, nefrotoxicidad o diabetes. El efecto colateral más común es la dislipidemia (hipercolesterolemia y/o hipertrigliceridemia), afectando entre el 23% al 31% de los pacientes, lo cual puede ser controlado con el uso de estatinas. Otros efectos adversos incluyen retardo en la cicatrización, hernias incisionales, úlceras orales, rash cutáneo, proteinuria, edema, dolores articulares, diarrea, náuseas, infecciones urinarias y neumonías. La proteinuria en particular, puede ser motivo para descontinuar el tratamiento por el riesgo de un síndrome nefrótico, en especial en pacientes con proteinuria basal con valores >800 mg/día previa al tratamiento, en quienes no se aconseja su uso [15,24,25].
Los esteriodes se han utilizado de forma permanente en el trasplante hepático con el fin de prevenir el rechazo agudo, y son comúnmente administrados como terapia de inducción, no obstante, con la introducción de otros agentes inmunosupresores como los ICN, su uso ha venido disminuyendo [26].
Para el tratamiento del rechazo agudo del injerto son administrados en altas dosis en bolos. Los más utilizados son metilprednisolona, prednisolona y prednisona [26,27]. Su amplio uso es determinado por sus efectos antiinflamatorios e inmunomoduladores, al unirse a los receptores de glucocorticoides, que influyen en la transcripción genética y producción de citocinas proinflamatorias, resultando en una disminución de la respuesta inflamatoria por la reducción de IL-1, IL-2, IL-6, IFN-γ y factor de necrosis tumoral alfa (TNF-α) [5]. Sin embargo, estos efectos traen consigo toxicidad severa y numerosos efectos adversos, lo cual ha tenido como resultado variaciones en la forma de administración. Entre ellas, se ha reducido drásticamente la dosis inicial de esteroides durante las primeras semanas postrasplante, e incluso muchos centros evitan su uso después de los primeros 6 meses. Adicionalmente, se considera que la utilidad de los esteroides es mayor para evitar el rechazo agudo que para los casos de rechazo tardío o crónico, y aún se consideran como la primera línea de tratamiento en la mayoría de los centros de trasplante para el rechazo agudo [26,27].
Como meta en el esquema inmunosupresor, idealmente se deben dejar de utilizar después de 3 a 6 meses postrasplante debido a la severidad de los efectos adversos, sin embargo, en los casos de pacientes trasplantados por hepatitis autoinmune o en aquellos con historia previa de rechazo severo, se considera que puede ser útil sostener el uso indefinido de prednisona a dosis bajas [26].
Presentan efectos secundarios indeseables, tales como hipertensión, retención de agua y sodio, diabetes, dislipidemia, retraso del crecimiento, osteoporosis, acné, alteraciones del comportamiento, inestabilidad del humor, cuadros psicóticos, cataratas o glaucoma. Por ello, en la mayoría de los esquemas son utilizados únicamente en los primeros meses del postoperatorio.
Fue incorporada en los esquemas de inmunosupresión en la década de 1960 [28]. La azatioprina es un derivado imidazólico de la 6-mercaptopurina, que como análogo de las purinas y al ser incorporado en la replicación del ADN, bloquea su ruta sintética, lo que afecta directamente el ciclo celular de los linfocitos [29].
Posterior a su administración es bien absorbida por el tracto gastrointestinal. Tiene una vida media reducida (cerca de 3 horas), sin embargo, sus metabolitos permanecen activos por largo tiempo, permitiendo ser administrada cada 12 a 24 horas.
Entre los principales fármacos que interactúan con la azatioprina se incluyen el alopurinol, el cual inhibe la xantina oxidasa y aumenta el riesgo de mielotoxicidad, y los inhibidores de la enzima convertidora de angiotensina (IECA).
La mielosupresión dependiente de la dosis es el efecto tóxico más grave, causa leucopenia y trombocitopenia [4]. Otros efectos son colestasis, pancreatitis, enfermedad hepática venooclusiva, alopecia y fragilidad dérmica. Otros menos frecuentes son el carcinoma espinocelular y hepatotoxicidad.
El micofenolato de mofetilo (MMF) y el micofenolato de sodio (MFS) son profármacos del ácido micofenólico (MPA). Actúan como inhibidores de la enzima inosina monofosfato deshidrogenasa (IMPDH), necesaria para sintetizar la guanosina, un nucleótido imprescindible para los leucocitos y la proliferación de las células T y B [2,27]. El mecanismo de acción es semejante al de la azatioprina. En la sangre circulan en el 90% unidos a proteínas, sin embargo, la concentración activa del medicamento es la porción no ligada a las proteínas, la cual es eliminada por la vía biliar, seguida de desconjugación intestinal por bacterias y posterior reabsorción, constituyendo un ciclo entero-hepático. Cerca del 90% de la dosis oral del medicamento es eliminado por la orina como glucurónido de ácido micofenólico.
El MPA ha venido sustituyendo a la azatioprina por ser más potente y presentar menos efectos adversos. Sin embargo, el MPA ha demostrado efectos teratogénicos en animales, por lo tanto, la azatioprina es la primera línea de elección en los casos de mujeres embarazadas [30].
Por otro lado, existe evidencia que sugiere que en la mayoría de los casos no es lo suficientemente potente y rápido para ser utilizado como monoterapia. Por lo tanto, los derivados del MPA son ampliamente usados en combinación con los ICN a dosis reducida, contribuyendo a la disminución de los efectos nefrotóxicos de los ICN [31].
La administración concomitante con ganciclovir y aciclovir puede potencializar la supresión medular. Existe riesgo de una reducción de la eficacia ante el uso simultáneo de antiácidos que contengan magnesio y aluminio.
Los principales efectos adversos son leucopenia, anemia, trombocitopenia, dolor abdominal y diarrea, afectando del 20% al 40% de los pacientes. También se describe neutropenia grave (neutrófilos <500/mm3), que es más común con dosis altas de MMF entre los 31 a 180 días postrasplante. Estos efectos adversos son frecuentemente resueltos con la disminución de la dosis [32].
Los fármacos descritos en la literatura son los anticuerpos monoclonales como muromonab-CD3, anti-CD2 o alemtuzumab, los anticuerpos policlonales como la globulina antitimocito de conejo o de caballo (ATG) o la globulina antilinfocitos, y los antagonistas del receptor de la IL-2 como el daclizumab, el basiliximab, el BT563 (anticuerpos IgG1 murino anti IL-2R) y el anticuerpo monoclonal anti-Tac (anticuerpos IgG2a murino anti IL-2R) [33-35].
Los preparados anticélulas T han sido usados con el propósito de evitar los eventos adversos de los primeros medicamentos utilizados en el periodo de inducción y en el postoperatorio inmediato [10]. Representan una alternativa apropiada para reducir dosis en fase postoperatoria inicial, puesto que existe un riesgo actual asociado al uso habitual de dosis elevadas de esteroides en la recidiva de hepatitis C e infección por citomegalovirus (CMV). La mayoría de los centros de trasplante están utilizando el preparado policlonal y la ATG con la intención de retrasar la exposición a los ICN.
La globulina antitimocítica (ATG) es un anticuerpo policlonal de origen de conejo o de caballo contra linfocitos T, efectiva para la prevención del rechazo al trasplante. El efecto inmunosupresor se da por la depleción de los linfocitos T, al promover su lisis [31,36]. Carece de acción nefrotóxica, por eso es indicada para pacientes que presentan disfunción renal en el momento del trasplante. Generalmente es administrada en el periodo intraoperatorio, como opción para la terapia de inducción con inmunosupresores o para el tratamiento del rechazo en pacientes corticorresistentes [11,36].
Basiliximab, un anticuerpo monoclonal antirreceptor de IL-2, es muy utilizado en la terapia de inducción para trasplante renal, además, diversos estudios encontrados en la literatura comprueban su eficacia en la terapia de inducción postrasplante hepático [29,34,36].
Rituximab es un anticuerpo monoclonal quimérico murino-humano, que se une específicamente al antígeno de membrana CD20, expresado en los linfocitos pre-B hasta los linfocitos B maduros, más no en células progenitoras, células pro-B, ni plasmocitos. Este fármaco permite iniciar reacciones inmunológicas que median la lisis de células B. Los posibles mecanismos para la lisis celular son la citotoxicidad dependiente del complemento, la citotoxicidad celular dependiente de anticuerpos y la inducción de apoptosis. Rituximab viene siendo utilizado para el tratamiento del rechazo hiperagudo y agudo mediados por anticuerpos en trasplantes renales y hepáticos [37,38].
Es necesario que exista un equilibrio entre el régimen ideal de inmunosupresión para prevenir el rechazo y la necesidad de minimizar la dosis de los fármacos, con el fin de prevenir los efectos adversos. También se han creado estrategias dirigidas a la protección renal que muestran beneficios si se introducen temprano en el primer año después del trasplante. Los esquemas de tratamiento se dividen en dos fases; la de inducción, que generalmente es administrada en los primeros meses postrasplante, y la de mantenimiento, que suele durar toda la vida [26]. Lo que se espera de la terapia inmunosupresora es evitar episodios de rechazo, mejorar la sobrevida, así como también, la calidad de vida. Las dosis de los principales fármacos de los esquemas inmunosupresores se especifican en la tabla 1.
La terapia doble con esteroides e ICN es considerada la terapéutica inicial en el trasplante hepático, con incidencia de rechazo del 35% al 50%, y sobrevida de los pacientes del 80% al 90% en el primer año postrasplante. Sin embargo, los efectos secundarios de la inmunosupresión (riesgo de infección oportunista y neoplasias de novo), la posibilidad de recidiva de hepatitis B y hepatitis C, y los efectos adversos a largo plazo, determinan una elevada morbilidad y son causas frecuentes de mortalidad [39,40].
Los esteroides utilizados en el intraoperatorio con dosis basal (tabla 1), se recomiendan reducir progresivamente hasta alcanzar un retiro completo entre los 3 meses y 1 año postrasplante. En los pacientes trasplantados por cirrosis debida a hepatitis C, se puede considerar la opción de mantener el esteroide solo por los primeros 6 meses, con la intención de minimizar los daños de la recidiva de la hepatitis C.
Para la prevención del rechazo agudo del injerto, en los casos de insuficiencia renal donde se desea retardar el inicio de los ICN debido a que inducen una mayor inmunosupresión por desencadenar una reducción de los linfocitos T, una alternativa sería la administración de ATG. En el caso de basiliximab como terapia de inducción, este ha demostrado una menor proporción de episodios de rechazo agudo a los 6 y 9 meses postrasplante [34]. Existe evidencia de que la adición de basiliximab a la triple inmunosupresión de mantenimiento, mejora la eficacia de la terapia, reduciendo la incidencia de episodios de rechazo agudo, sin aumentar los efectos adversos [33]. Puede ser la alternativa más apropiada para pacientes con insuficiencia renal previa o alta posibilidad de desarrollarla en el postoperatorio del trasplante.
Una revisión sistemática que comparó la terapia de inducción entre ATG y corticoterapia, no identificó diferencias significativas en cuanto a mortalidad, rechazo, recidiva de infecciones y complicaciones [41]. Por otra parte, otro estudio realizó un análisis comparativo entre los tipos de anticuerpos, y no se identificaron diferencias significativas. Sin embargo, hubo menor tasa de eventos adversos entre los antagonistas de IL-2, comparados con ATG policlonales (RR 0,23; IC95% 0,09-0,93). Los autores alertan de la baja calidad de los estudios clínicos aleatorizados, con un elevado riesgo de sesgo, debido al pequeño número de estudios disponibles, pobre calidad metodológica y muestra limitada [42].
Dosis de fármacos inmunosupresores en trasplante hepático.
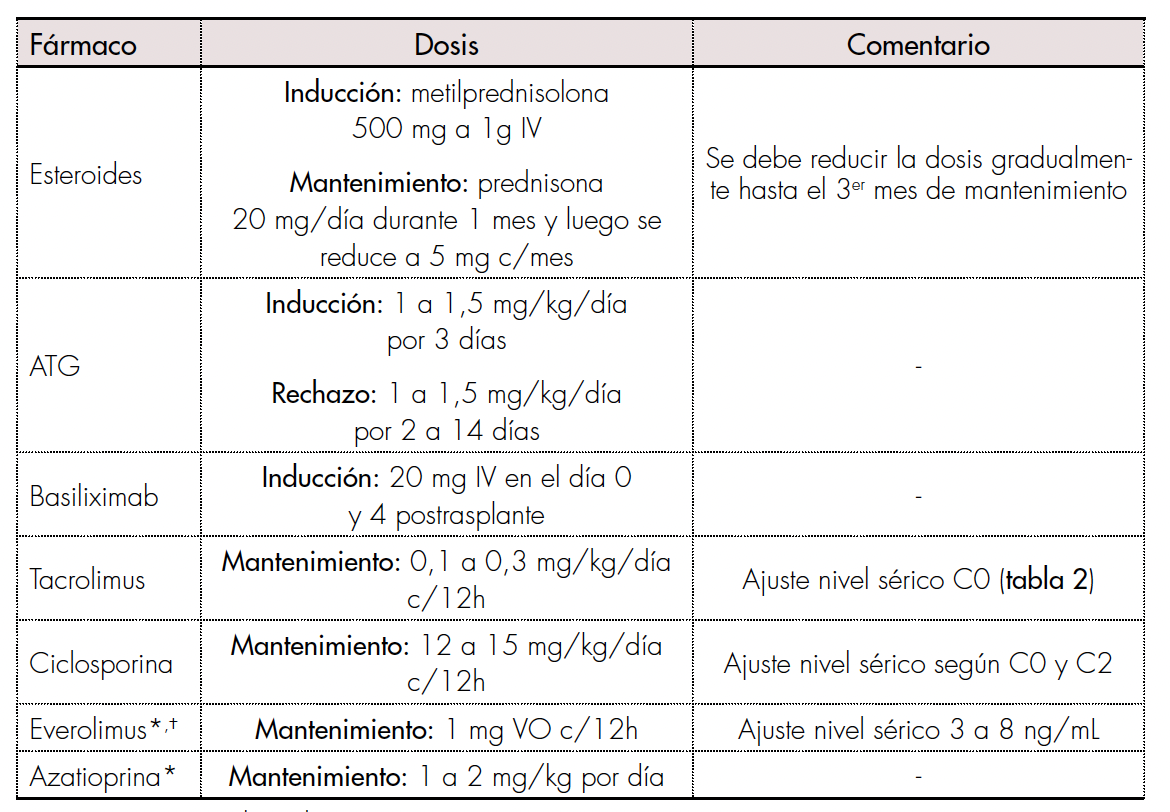
* Tratamiento combinado.Ϯ Iniciar terapia 30 a 60 días postrasplante. C0: concentración predosis; C2: concentración a las 2 horas después de la administración; ATG: globulina antitimocítica.
Los ICN, ciclosporina y tacrolimus, continúan siendo los principales fármacos en el esquema de inmunosupresión eficaz para evitar el rechazo. Para minimizar el efecto adverso de su uso crónico, se busca asociar y reducir la dosis de estos agentes con otros inmunosupresores de diferentes clases, tales como MMF o MFS, EVR y/o esteroides [43,44]. La justificación para la adición de los derivados del MPA es permitir una reducción de la exposición a los ICN, preservando así la función renal [32,45].
Un metaanálisis determinó que el tacrolimus es superior a la ciclosporina en mejorar la sobrevida del paciente y del injerto, y en prevenir el rechazo agudo después del trasplante de hígado. No obstante, el tacrolimus aumentó el riesgo de diabetes [46].
Algunos centros de trasplante utilizan esquemas de inmunosupresión libre de esteroides, mediante una monoterapia con tacrolimus [47]. En una revisión de 2014 se concluyó que la sustitución de esteroides por otros agentes inmunosupresores o monoterapia con tacrolimus después de dos semanas de esteroides, son alternativas propuestas para minimizar los efectos adversos de los esteroides [48].
Las evidencias de tres estudios aletorizados indican que el uso de everolimus, asociado a dosis reducida de tacrolimus, tiene un beneficio en la función renal de pacientes trasplantados de hígado después del primer al tercer año de seguimiento [49-51]. El inicio de esta medicación se recomienda aproximadamente 4 semanas posterior al trasplante [49]. El nivel sérico de EVR es de fundamental importancia para la eficacia del fármaco, más que la dosis ingerida por el paciente trasplantado; por lo tanto, la monitorización terapéutica es necesaria. Estudios en trasplantados de riñón indican que niveles séricos de EVR mantenidos alrededor de 8 ng/mL, combinados con ICN a dosis reducidas, preservan la eficacia para prevenir el rechazo del injerto.
En cuanto a los pacientes con CHC, se pueden utilizar los ImTOR, los cuales han demostrado que disminuyen el riesgo de recidiva y complicaciones. El riesgo de recidiva del CHC en pacientes trasplantados demostró ser dependiente de la dosis de los ICN [52-54], ya que estos tienen efectos proliferativos de células malignas por un aumento de la angiogénesis y la invasión de células cancerígenas [55].
El orden terapéutico para el control del postrasplante hepático inicia con tacrolimus como terapia de elección, a dosis de 0,1 a 0,3 mg/kg/día cada 12 horas VO o vía sonda nasogástrica (VSN), siendo necesario monitorear sus niveles séricos dependiendo del tiempo (tabla 2). Las alternativas al tacrolimus son la ciclosporina y la corticoterapia. La administración oral de ciclosporina debe regularse según la evaluación C0 o C2 (tabla 2) antes de la administración del medicamento, de acuerdo a los niveles séricos.
La terapia puede ser individualizada dependiendo del tipo de paciente, ya sea tipo alfa, alfa autoinmune, no alfa y beta (tabla 3), con la intención de maximizar el beneficio y disminuir los efectos adversos en el paciente.
Niveles sanguíneos de tacrolimus y ciclosporina de acuerdo al tiempo postrasplante.
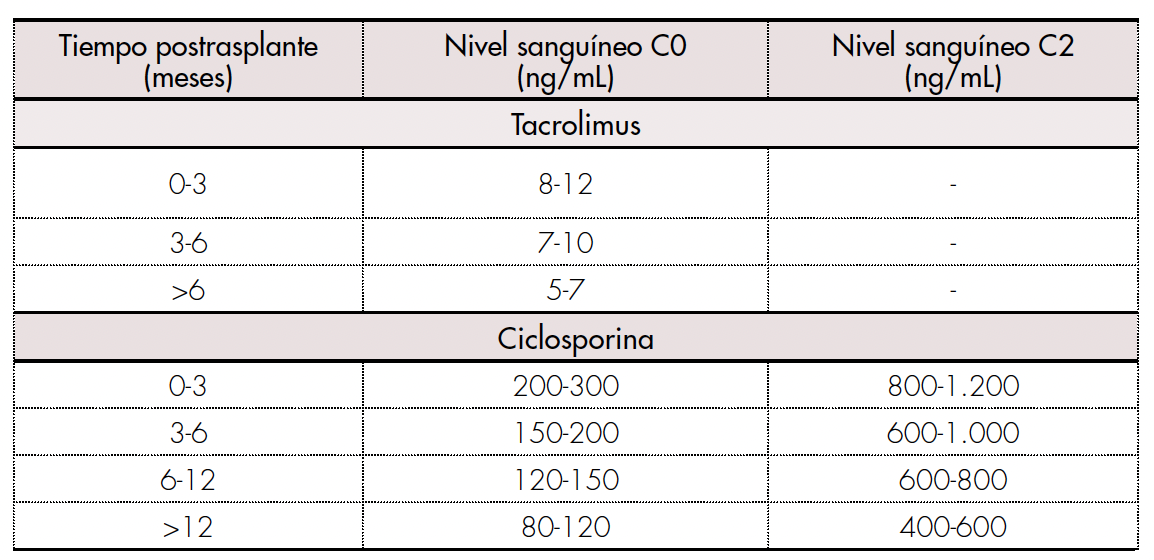
C0: concentración predosis; C2: concentración a las 2 horas después de la administración.
Terapia inmunosupresora completa en paciente postrasplante hepático.
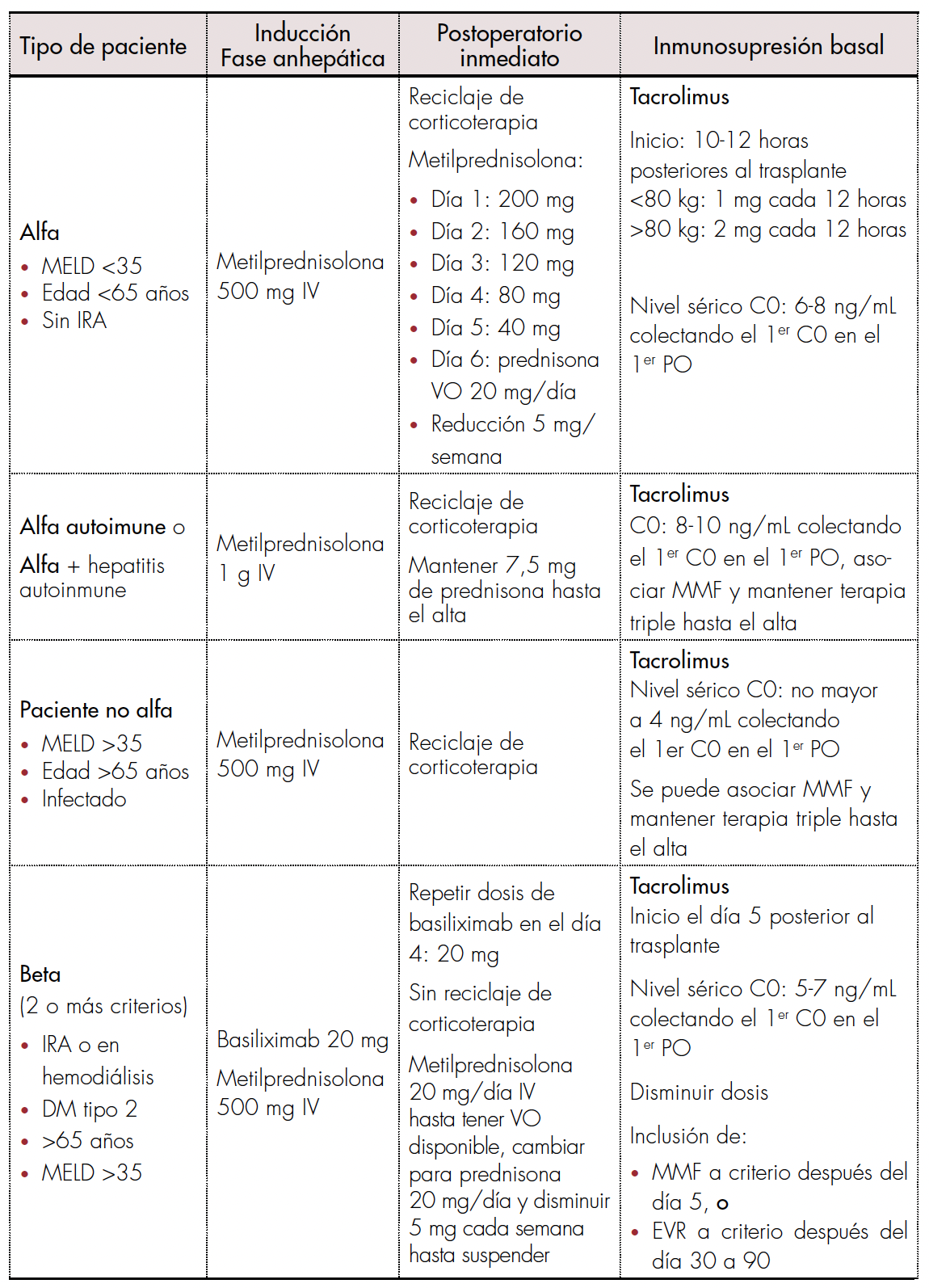
MELD: Model for End-stage Liver Disease ; IRA: insuficiencia renal aguda; IV: endovenoso; VO: vía oral; PO: postoperatorio; C0: concentración predosis; MMF: micofenolato de mofetilo; EVR: everolimus; DM: diabetes mellitus.
Consiste en terapias alternativas a la tradicional, recomendadas ante comorbilidades o efectos secundarios especiales del paciente inmunosuprimido tras el trasplante hepático (tabla 4). Estas buscan reducir la dosis de ICN, para disminuir sus efectos adversos.
Terapia inmunosupresora postrasplante hepático en presencia de comorbilidades.
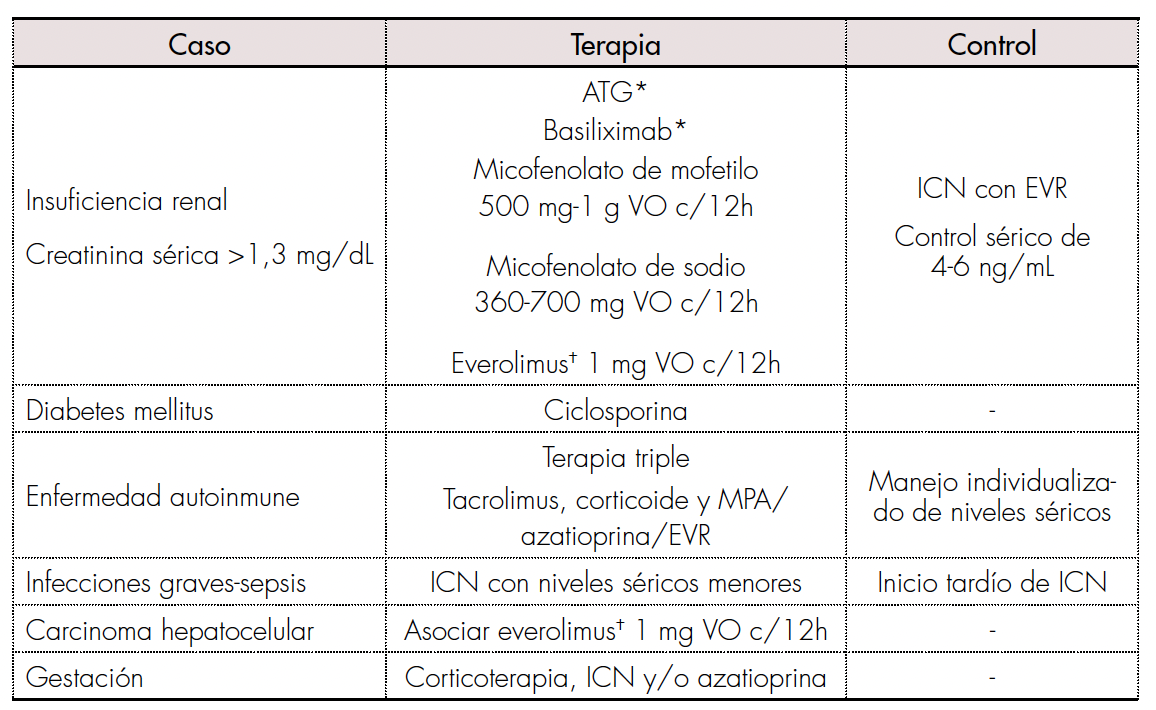
* Retardar el inicio de inhibidores de calcineurina.Ϯ Después de 60 días postoperatorio. ATG: globulina antitimocítica; VO: vía oral; ICN: inhibidores de la calcineurina; EVR: everolimus; MPA: ácido micofenólico.
La primera medida terapéutica a ser adoptada es aumentar el inmunosupresor de base hasta obtener una respuesta favorable, con el objetivo de reducir las enzimas hepáticas o mejorar los hallazgos histológicos de rechazo agudo. Se recomienda la siguiente secuencia de alternativas:
1. Bolo de 500 mg a 1 g de metilprenisolona, que puede ser o no repetido.
2. Cuando es posible, aumentar la dosis de los ICN, con la finalidad de alcanzar niveles sanguíneos en el límite superior.
3. Para mantenimiento posrechazo, se tiene como opción MPA o ImTOR. En caso de resistencia se recomienda timoglobulina 1,5/ng/kg/día durante 3 a 14 días.
4. En casos de rechazo hiperagudo/agudo mediado por anticuerpos, existe la opción de rituximab (hasta 375 mg/m2), asociado a inmunosupresión triple.
Es difícil revertir un cuadro de rechazo que ya evolucionó con ductopenia. En caso de no presentarse mejoría clínica ni de la bioquímica, o en ausencia de ductos biliares en la biopsia hepática, se debe indicar retrasplante hepático lo más precozmente posible para evitar el deterioro clínico progresivo. Los resultados del retrasplante hepático en el rechazo crónico son aceptables en comparación a otras etiologías.
La terapia de inmunosupresión es continua para todos los pacientes trasplantados de hígado [56]. La intensidad de la inmunosupresión y los medicamentos utilizados serán definidos conforme a la evolución y a la reacción inmunológica al injerto. Una de las complicaciones postrasplante es el surgimiento de neoplasias, y en casos de enfermedad linfoproliferativa, el inmunosupresor será reducido en algunos pacientes hasta suspenderlo. La reducción de la dosis deberá ser individualizada, considerando la gravedad, estadio de la neoplasia y riesgo de rechazo [57,58].
El trasplante hepático exitoso requiere un esquema de atención y cuidado que involucre un equipo médico, en conjunto con los pacientes y familiares, para toda la vida. Se debe mantener apoyo y vigilancia de la adherencia al tratamiento de los pacientes trasplantados, principalmente aquellos de la tercera edad.
Los pacientes son vigilados mensualmente en el primer año postrasplante para la evaluación de los niveles séricos de los inmunosupresores, la verificación de efectos adversos o infecciosos, y los exámenes para diagnóstico precoz. En el caso del paciente sin complicaciones clínicas y de laboratorio, las visitas médicas y los exámenes deberán ser progresivamente espaciados. En el segundo año postrasplante, el acompañamiento ambulatorio puede pasar a ser trimestral. La evaluación de los niveles séricos de los inmunosupresores y eventuales ajustes de las dosis, y el control de exámenes de sangre y orina para analizar la función renal, glicemia y perfil lipídico, deben ser mantenidos bajo vigilancia y documentados en la historia clínica del paciente. La tamización y búsqueda de aparición de neoplasias inicia con el examen físico, para investigar lesiones sugestivas de melanomas. Todos los eventos adversos deben ser documentados en la historia clínica.
El adecuado manejo de la inmunidad en el paciente con trasplante de cualquier órgano sólido es de suma importancia para evitar la reacción inmune contra el injerto, que lleva al declive del procedimiento, y por ende, al fallo terapéutico, pudiendo terminar en la muerte del paciente. Específicamente, valorando el trasplante hepático, existen varios fármacos útiles para reducir la inmunidad y garantizar la efectividad de la intervención quirúrgica. En cuanto a los fármacos utilizados, se han mantenido como primera opción los inhibidores de la calcineurina, correspondientes a tacrolimus y ciclosporina; el tacrolimus es principalmente utilizado en la inducción y mantenimiento de la inmunosupresión eficaz para evitar el rechazo. Otros fármacos cuyo uso varía según la necesidad del paciente o según la consideración del centro de trasplante, son los agentes antimetabolitos, los ImTOR, los esteroides, los derivados del ácido micofenólico y anticuerpos de diferentes tipos, destacándose cada uno de ellos por tener características significativas. Algunas de las alternativas terapeúticas implementadas, no han demostrado ser lo suficientemente efectivas para ser prescritas como monoterapia, por lo que se sugiere su combinación con los inhibidores de la calcineurina a dosis reducida. Los fármacos de terapia inmunológica son eficaces tanto para la fase de inducción, como para la del postoperatorio inmediato. Es importante reconocer que los efectos adversos de la terapia inmunosupresora son frecuentes, por lo tanto, es óptimo llevar a cabo una monitorización regular postrasplante, con el objetivo de identificarlos de forma temprana y poder realizar los ajustes necesarios a la terapia inmunosupresora, en pro de evitar un empeoramiento del paciente. La opción terapéutica será individualizada, mediante un análisis exacto de las comorbilidades y condiciones presentes en cada caso.

Figura 1.
Diagrama de flujo de búsqueda de la información.
Dosis de fármacos inmunosupresores en trasplante hepático.

* Tratamiento combinado.Ϯ Iniciar terapia 30 a 60 días postrasplante. C0: concentración predosis; C2: concentración a las 2 horas después de la administración; ATG: globulina antitimocítica.
Niveles sanguíneos de tacrolimus y ciclosporina de acuerdo al tiempo postrasplante.

C0: concentración predosis; C2: concentración a las 2 horas después de la administración.
Terapia inmunosupresora completa en paciente postrasplante hepático.

MELD: Model for End-stage Liver Disease ; IRA: insuficiencia renal aguda; IV: endovenoso; VO: vía oral; PO: postoperatorio; C0: concentración predosis; MMF: micofenolato de mofetilo; EVR: everolimus; DM: diabetes mellitus.
Terapia inmunosupresora postrasplante hepático en presencia de comorbilidades.

* Retardar el inicio de inhibidores de calcineurina.Ϯ Después de 60 días postoperatorio. ATG: globulina antitimocítica; VO: vía oral; ICN: inhibidores de la calcineurina; EVR: everolimus; MPA: ácido micofenólico.


