



Jornadas
Jornadas del Comité de Nefropatía de la Sociedad Argentina de Diabetes Actualización de cirugía bariátrica en paciente con diabetes y enfermedad renal. Parte 1. Apartado 3
Conference of the Nephropathy Committee of the Argentine Society of Diabetes Bariatric surgery update in a patient with diabetes and kidney disease. Part 1. Section 3
Revista de la Sociedad Argentina de Diabetes
Sociedad Argentina de Diabetes, Argentina
ISSN: 0325-5247
ISSN-e: 2346-9420
Periodicidad: Cuatrimestral
vol. 55, núm. 2, 2021
Recepción: 18 Febrero 2021
Aprobación: 03 Mayo 2021

Palabras clave: microbiota intestinal, obesidad
Keywords: gut microbiota, obesity
Microbiota intestinal, obesidad, síndrome metabólico, diabetes mellitus tipo 2 y enfermedad renal crónica
Gut microbiota, obesity, metabolic syndrome, type 2 diabetes mellitus, and chronic kidney disease
La microbiota intestinal es la comunidad de microorganismos vivos residentes en el intestino y sus alteraciones podrían contribuir en parte con el desarrollo de algunas patologías como la obesidad y la DM2. La población en colon asciende a 1,012-1,014, siendo esta cifra mayor que el de las células humanas1. Cumple funciones sobre la nutrición ya que interviene en el procesamiento de componentes indigeribles de la dieta como polisacáridos vegetales, la síntesis de aminoácidos esenciales y vitaminas, la homeostasis metabólica y la regulación inmunológica1.
La microbiota intestinal es diferente para cada individuo y existe un balance saludable entre huésped-microorganismos que posibilita que las funciones anteriormente mencionadas se desarrollen de manera óptima 2.
La microbiota intestinal incluye especies nativas que colonizan permanentemente el tracto gastrointestinal (TGI) y microorganismos que lo colonizan transitoriamente.
Las alteraciones de la microbiota intestinal y la respuesta adversa del huésped se denominan disbiosis y se asocia con diferentes patologías como obesidad, SM y DM2.
Las bacterias son trillones de microorganismos que constituyen ~50% de la masa fecal. Los filos microbianos intestinales dominantes son firmicutes (GRAM+), bacteroidetes (GRAM-), actinobacteria, proteobacteria, fusobacteria y verrucomicrobia. Los filos firmicutes y bacteroidetes representan el 90% de la microbiota intestinal. El filo firmicutes está compuesto por más de 200 géneros diferentes como Lactobacillus, Clostridium, Enterococcus y Ruminicoccus. El género Clostridium representa el 95% del filo firmicutes. El filo bacteroidetes se constituye de géneros predominantes como Bacteroides y Prevotella. El filo actinobacteria es proporcionalmente menos abundante, representado principalmente por el género Bifidobacterium2.
El ser humano intraútero carece de microbiota y el TGI se coloniza inmediatamente al nacer. A lo largo de la vida, la composición microbiana dependerá de la genética, edad, tipos de fuentes nutricionales, enfermedades, uso de antibióticos, etc.1,2,3.
En este texto nos referiremos fundamentalmente a la relación entre la microbiota y la homeostasis metabólica.
Efectos metabólicos de la microbiota intestinal
La microbiota intestinal cumple algunos de los siguientes efectos metabólicos:
• Efectos por su actividad enzimática fermentativa sobre polisacáridos complejos no digeribles con la consecuente generación de monosacáridos (MS) y ácidos de cadena corta (AGCC).
• Efectos por sus endotoxinas: endotoxemia metabólica.
• Efectos por su actividad enzimática sobre las proteínas.
Microbiota en condiciones fisiológicas
1. Bacterias y monosacáridos en condiciones fisiológicas normales
Los MS provenientes de la fermentación bacteriana activan la ChREBP (proteína de unión a elemento de respuesta a carbohidratos), el mayor factor de transcripción activado por la glucosa que se encuentra altamente expresado en hígado, células β pancreáticas, tejido adiposo blanco y pardo y músculo, que tiene capacidad de regular el metabolismo de la glucosa y los lípidos a través de la regulación de la expresión genética de las vías de la glucólisis, gluconeogénesis y lipogénesis4.
2. Bacterias y AGCC en condiciones fisiológicas normales
a) Los AGCC, fundamentalmente propiónico, butírico y acético (proporción habitual 1-1-3), son efectores de las actividades de la microbiota relacionadas con:
• El metabolismo de la glucosa y de los lípidos.
• El apetito y la homeostasis de la energía.
• Las actividades anticancerígenas, antioxidantes e inmunomoduladoras.
A nivel del hígado, tejido adiposo blanco y pardo y músculo esquelético regulan la expresión genética de las vías de la glucólisis, gluconeogénesis y lipogénesis5.
El propionato y el acetato son producidos principalmente por bacteroidetes, mientras que el butirato es dominantemente producido por firmicutes. Sin embargo cada AGCC no es de síntesis exclusiva de cada filo bacteriano3,6.
Si bien la luz intestinal es el principal sitio de producción de los AGCC, el gradiente de concentración cae desde la luz hacia la periferia con una captación preferencial de butirato por el epitelio intestinal, propionato por el hígado y acetato por los tejidos periféricos7.
En el hígado, el propionato puede activar la gluconeogénesis e inhibir la lipogénesis mientras que el acetato es el principal AGCC sustrato para la lipogénesis hepática y promueve la lipogénesis en tejido adiposo blanco. El butirato estimula la lipólisis en tejido adiposo y la β oxidación de los AGL3.
El acetato parece ser “predominantemente” obesogénico, mientras butirato y propionato “predominantemente” antiobesogénicos”, pero ninguno de los tres cumple esta función de manera pura ya que se pueden comportar en uno u otro sentido.
El butirato es la principal fuente de energía de los colonocitos, incrementa la actividad mitocondrial, previene la endotoxemia metabólica, mejora la sensibilidad insulínica, tiene actividad antiinflamatoria y anticancerígena, protege la integridad de la barrera intestinal y favorece la hipofagia.
El propionato inhibe la síntesis de colesterol antagonizando el efecto del acetato e inhibe la expresión de resistina en los adipocitos. El propionato y el acetato regulan el peso al actuar sobre hormonas anorexígenas intestinales. El acetato es potencialmente obesogénico por actuar como sustrato para la lipogénesis hepática y adipocitaria6.
El acetato ha sido vinculado con la supresión de la lipólisis adipocitaria periférica, por lo tanto, reduce el flujo de AGL hacia el hígado mitigando el deterioro inducido por el hígado graso sobre la homeostasis de la glucosa. Por otro lado, su elevación en plasma está inversamente relacionada con los niveles de insulina plasmática. Un mecanismo para explicar este efecto involucra una mejor respuesta de la insulina en las células β pancreáticas mediada por los GPR-43 (receptores acoplados a la proteína G-43) lo que induce un mejor control glucémico7.
Como se menciona en el párrafo anterior, parte de los efectos metabólicos de los AGCC se realiza a través de su actividad sobre los GPR-41 también llamado FFAR-3 (receptor de ácidos grasos libres-2) y GPR-43 también llamado FFAR-2. Ambos GPRs están presentes también en adipocitos, células epiteliales y enteroendocrinas. Su estímulo produce aumento de la síntesis de PYY y GLP-1 (péptido YY y péptido símil al glucagon-1: ambos de efecto anorexígeno) por lo que modulan el eje intestino-hipotálamo, favorecen el aumento de la motilidad intestinal y disminuyen la cosecha de energía de los alimentos. El estímulo del GPR-43 reduce la liberación de AGL a la circulación al mejorar la sensibilidad a la insulina. El GPR-41 aumenta la expresión de leptina en adipocitos6.
Por otra parte, algunos componentes microbianos por sí mismos, como la proteína chaperona ClpB, mimetizan al POMC (propiomelanocortina) precursor de la α-MSH (melanocortina) de efecto anorexígeno, lo cual se suma al efecto de los AGCC sobre el control del apetito5.
En las Tablas 1, 2 y 3 se describen algunos de los mecanismos por los cuales actúan los AGCC y las vías efectoras hasta ahora conocidas.
b) Los AGCC en condiciones fisiológicas normales aumentarían la expresión intestinal del FIAF (fasting-induced adipose factor o factor adiposo inducido por el ayuno) también llamado ANGPTL4 (angiopoietin-like 4).
La microbiota regula la expresión del FIAF intestinal, que es un inhibidor circulante de la lipoproteinlipasa (LPL) que favorece la captura de los ácidos grasos y el aumento del tejido adiposo. Algunos trabajos demostraron que AGCC como el butirato pueden aumentar la expresión del FIAF intestinal de manera PPAR-γ independiente. Sin embargo, la co-estimulación con ligandos del PPAR-γ conjuntamente con AGCC produce un aumento de los niveles del FIAF. Estudios sobre líneas celulares de adenocarcinoma de colon señalaron que concentraciones fisiológicas de AGCC indujeron la expresión del FIAF por activación del PPAR-γ. Sin embargo, el mecanismo definitivo por el cual los AGCC modifican la expresión del FIAF queda aún por dilucidarse8,9,10.
c) Los AGCC y mucosa intestinal: función de barrera y angiogénesis en condiciones fisiológicas normales.
La microbiota promueve la función de barrera intestinal a través de la acción de los AGCC. El butirato favorece las uniones intercelulares de la mucosa intestinal por estimular la expresión genética de las proteínas de unión estrecha zonulina y ocludina que mantienen la adecuada función de barrera-permeabilidad intestinal. También inhibe la angiogénesis de la mucosa intestinal y favorece la apoptosis de células neoplásicas, contribuyendo en la prevención del cáncer colorrectal (CCR)6,11.
3. Bacterias y termogénesis: sistema endocannabinoide (SEC) y empardamiento en condiciones fisiológicas normales
El SEC juega un rol clave en la homeostasis de la energía dado que regula el apetito, la distribución y expendio de energía, la expansión del tejido adiposo, la homeostasis de la glucosa y la regulación de la inflamación. En estudios con animales, la microbiota intestinal y el SEC se modulan mutuamente. Por ejemplo, la presencia de Lactobacillus acidophilus (filo firmicutes) ha mostrado que induce la expresión de receptores cannabinoides en las células intestinales, generando cambios en la permeabilidad. Desafortunadamente, los datos se basan predominantemente en estudios animales. En humanos, la relación directa entre los cambios en la microbiota intestinal y el tono del SEC todavía debe demostrarse concluyentemente 5.
Por otra parte, estudios que revisaron el vínculo entre la exposición al frío y la microbiota resaltan que una cepa bacteriana específica, la Akkermansia muciniphyla (filo verrucomicrobia) cuya presencia o ausencia parece modular la eficiencia energética en función del estado nutricional del huésped o de la temperatura ambiente, actuaría como un sensor de energía5.
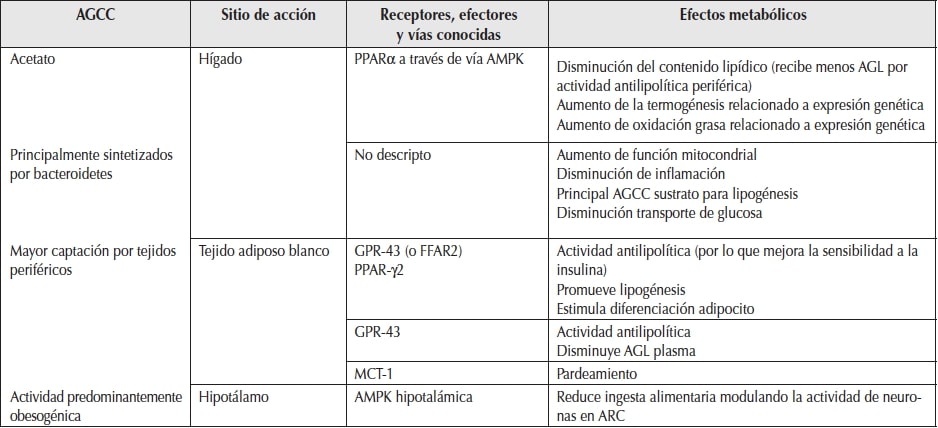
PPAR: receptor del proliferador activado de peroxisoma; AMPK: adenosina monofosfato kinasa; MCT-1: transportador de monocarboxilato-1; AGL: ácidos grasos libres; ARC: núcleo arcuato.
Modificado de: Cani et al.5.
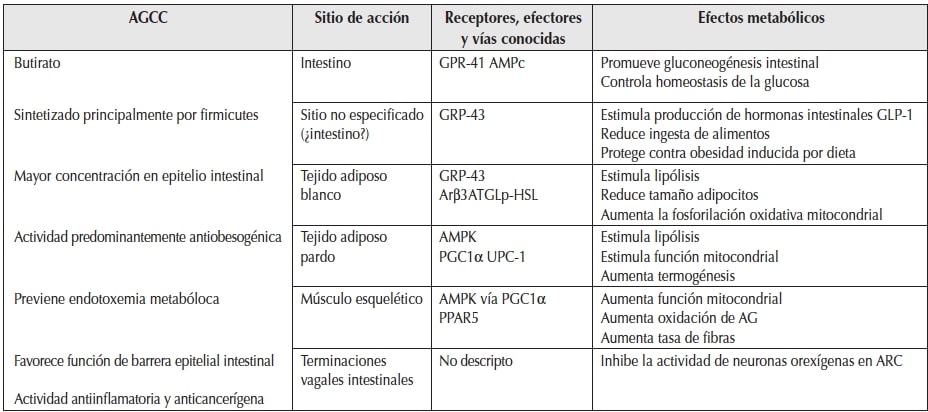
ARβ 3: receptor β adrenérgico 3; ATGL: adiposo-triglicéridos lipasa; p-HSL: lipasa hormono sensible fosforilada; PGC-1α: proteína coactivadora del receptor activado por el proliferador de peroxisomas1α; UCP-1: proteína desacoplante-1.
Modificado de: Cani et al.5.Microbiota, obesidad y DM2
La disbiosis puede contribuir al desarrollo de distintas enfermedades. Estudios realizados tanto en ratones como en humanos demostraron que la microbiota intestinal difiere en su composición entre obesos y delgados. En un modelo de ratones ob/ob deficientes en leptina, Ley et al. encontraron un aumento de la relación firmicutes/bacteroidetes, los dos filos bacterianos intestinales dominantes. Los ratones obesos mostraron un aumento de firmicutes y disminución de bacteroidetes, comparados con los magros12. Cuando Ley et al. evaluaron lo mismo en humanos delgados vs obesos, encontraron diferencias similares 13.
En el estado de obesidad existe un cambio pronunciado en la ecología microbiana asociada a la patología del huésped. La convivencia de bacteroidetes y firmicutes en el intestino implica una minimización de la competencia por los recursos a través de la cooperación o la especialización. Por lo tanto, el colon de sujetos obesos tiene propiedades que inclinan el equilibrio hacia el aumento de firmicutes: “microbiota obesa”13.
La misma alteración (aumento de firmicutes y disminución de bacteroidetes) está asociada y/o predice el desarrollo de resistencia insulínica/DM2 de tal forma que se la considera como un futuro potencial marcador clínico de DM214.
Múltiples estudios confirmaron que las alteraciones de la microbiota de los sujetos obesos pueden relacionarse con una mayor capacidad para extraer o “cosechar” energía de los alimentos, comparados con sujetos delgados14.
Si comparamos lo expuesto anteriormente durante una condición fisiológica normal vs sujetos obesos-DM2, en este último grupo hay un aumento de la capacidad para cosechar la energía de los alimentos, lo cual puede explicarse por varios mecanismos relacionados con la disbiosis descripta.
En sujetos con obesidad-DM2 se ha encontrado:
• Incremento de MS circulantes y por lo tanto de la captura de los mismos a nivel hepático, lo cual activa la ChREBP al favorecer la lipogénesis, y alterar la glucólisis y gluconeogénesis1,15,16.
• Todas las funciones que los AGCC cumplen sobre el metabolismo de los H de C y los lípidos se ven alteradas, ya que al variar la microbiota varía la concentración de cada AGCC y sus funciones (el desequilibrio en la síntesis de butirato puede provocar disminución de la lipólisis, de la oxidación de los AGL y la termogénesis). En la disbiosis se observa una disminución de la expresión del FIAF, lo cual favorecerá la actividad de la LPL aumentando los AGL circulantes provenientes de los triglicéridos y su posterior captura con expansión del tejido adiposo1,16,17. También se altera el eje intestino-hipotálamo y los niveles de péptidos anorexígenos5.
• La disbiosis aumenta la vascularización y el flujo sanguíneo dentro de la mucosa intestinal , facilitando la absorción de nutrientes1,18.
Todos los mecanismos conducen a un aumento de la cosecha de energía de los alimentos.
Endotoxemia metabólica
Las bacterias Gram (-) (70% del total de bacterias en el intestino) tienen en su membrana externa un componente glicolipídico principal: un lipopolisacárido (LPS) con acción de endotoxina19.
La microbiota obesa y sus cambios en las concentraciones de AGCC, fundamentalmente del butirato, se relacionan con la reducción de la expresión de los genes para las proteínas de unión estrecha intestinal que se muestran menos abundantes y desorganizadas en el colon, favoreciendo el pasaje de endotoxinas a través de la barrera alterada. El ingreso de las endotoxinas de las bacterias exógenas puede ser por vía local o por una infección sistémica, y el de las endógenas a través del intestino luego de la lisis de la célula bacteriana por absorción paracelular o por transporte transcelular6,19.
La endotoxemia puede originar un cuadro de infección/sepsis o un cuadro metabólico denominado “endotoxemia metabólica”.
Cani et al. describieron la “endotoxemia metabólica” como una condición del LPS plasmático crónicamente elevado en niveles 10 a 50 veces más bajos que durante las condiciones sépticas. La endotoxemia metabólica se observó en ratones genéticamente obesos (ob/ob) que consumían dieta normocalórica y se pudo inducir en ratones magros con una dieta obesogénica. Esto se relacionó con un aumento del depósito de grasa, activación de las vías inflamatorias y oxidativas y un incremento de la resistencia insulínica20.
Estudios en humanos también mostraron una elevación del LPS circulante en individuos obesos vs delgados21.
El componente lipídico del LPS (lípido A) inicia una cascada de señalizaciones al unirse al receptor tipo Toll 4 (TLR4) presente en células inmunológicas, músculo esquelético, hígado y tejido adiposo, activando al factor de transcripción NFκB (factor nuclear κB) lo cual resulta en un aumento de la expresión de proteínas proinflamatorias (por ejemplo, PAI-1, TNFα, IL6, IL-1) y ROS generando un estado inflamatorio de bajo grado, que también caracteriza a la obesidad, la DM2, la enfermedad cardiovascular y la aterosclerosis. Este estado inflamatorio generado por la endotoxemia juega un rol importante en la regulación de la homeostasis de la glucosa y los lípidos19.
Microbiota en la enfermedad renal
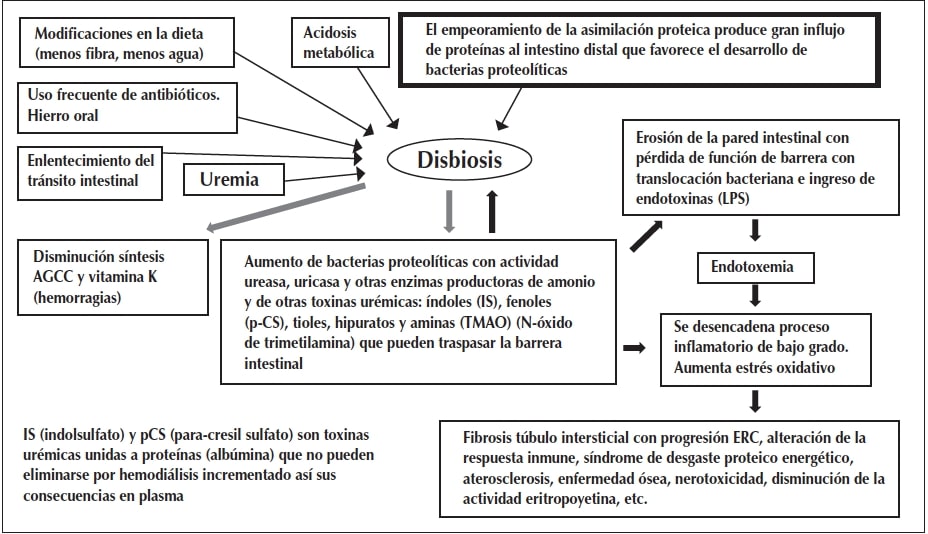
Los pacientes con ERC y ERCT tienen alteraciones cuantitativas y cualitativas en la microbiota intestinal. Esta disbiosis puede producirse por la uremia per se o relacionarse con modificaciones de la dieta, como disminución de la ingesta de fibra y líquidos y situaciones de tratamiento (como el uso recurrente de antibióticos o hierro oral), acidosis metabólica, empeoramiento de la asimilación proteica y enlentecimiento del tránsito intestinal22,23.
Las alteraciones de la microbiota intestinal incluyen un aumento de bacterias aerobias y anaerobias en duodeno y yeyuno y una disminución en todo el intestino delgado de lactobacillaceae y prevotellaceae. En colon hay un sobrecrecimiento de bacterias aerobias 100 veces mayor, con aumento de proteobacterias, enterobacterias, clostridium perfringens y disminución de lactobacilos y bifidobacterias, con alto riesgo de diarreas por clostridium difficile22,23.
Esta microbiota intestinal disbiótica no solo produce toxinas urémicas y una variedad de metabolitos nocivos, sino también puede potencialmente disminuir la producción de metabolitos beneficiosos como los AGCC.
La pérdida de la función renal produce un mayor ingreso de urea dentro del tracto gastrointestinal lo cual, junto con el empeoramiento de la asimilación proteica de la dieta, produce gran influjo de proteínas al intestino distal y favorece el desarrollo de bacterias proteolíticas. A través de la ureasa expresada por algunas bacterias intestinales (especialmente Clostridium spp, Enterococcus, Shigella, Escherichia coli), se generan altos niveles de amonio y otros tóxicos que afectan el crecimiento de las bacterias comensales y alteran la permeabilidad de la barrera intestinal, permitiendo la translocación bacteriana y el ingreso de endotoxinas (LPS), desencadenando un estado inflamatorio de bajo grado que colabora con la progresión de la ERC, la enfermedad cardiovascular, la resistencia insulínica, la pérdida de la energía proteica y la alteración del sistema inmune, etc.22-25.
En los pacientes en hemodiálisis, el estrés circulatorio sistémico y la isquemia regional recurrente también pueden dañar la barrera intestinal22-25.
En la Figura 2 se muestra un esquema de la relación “disbiosis-enfermedad renal”.
BIBIOGRAFÍA
1. Icaza-Chávez ME. Microbiota intestinal en la salud y la enfermedad. Revista de Gastroenterología de México 2013; 78(4):240-248.
2. Rinninella E, Raoul P, Cintoni M, et al. What is the healthy gut microbiota composition? A changing ecosystem across age, environment, diet, and diseases. Microorganisms 2019; 7(1):14 1-22.
3. Thursby E, Juge N. Introduction to the human gut microbiota. Biochem J 2017; 474(11):1823-1836.
4. Iizuka K. Recent progress on the role of ChREBP in glucose and lipid metabolism. Endocrine Journal 2013; 60 (5): 543-555.
5. Cani PD, Van Hul M, Lefort C, et al. Microbial regulation of organismal energy Homeostasis. Nature Metabolism 2019; 34 (1):34-46.
6. Chakraborti CK. New found link between microbiota and obesity. World J Gastrointest Pathophysiol 2015; 6 (4):110-119.
7. Morrison DJ, Preston T. Formation of short chain fatty acids by the gut microbiota and their impact on human metabolism. Gut Microbes 2016; 7(3):189-200.
8. Alex S, Lange K, Amolo T, et al. Short-chain fatty acids stimulate angiopoietin-Like 4 synthesis in human colon adenocarcinoma cells by activating peroxisome proliferator-activated receptor γ. Mol Cell Biol 2013; 33(7):1303-1316.
9. Korecka A, De Wouters T, Cultrone A, et al. ANGPTL4 expression induced by butyrate and rosiglitazone in human intestinal epithelial cells utilizes independent pathways. Am J Physiol Gastrointest Liver Physiol 2013; 304: G1025-G1037.
10. Musso G, Gambino R, Cassader M. Obesity, diabetes, and gut microbiota the hygiene hypothesis expanded. Diabetes Care 2010; 33:2277-2284.
11. Wu X, Wu Y, He L, et al. Effects of the intestinal microbial metabolite butyrate on the development of colorectal cancer. Journal of Cancer 2018; 9 (14):2510-2517.
12. Ley RE, Backhed F, Turnbaugh P, et al. Obesity alters gut microbial ecology. Proc Natl Acad Sci U S A 2005; 102:11070-11075.
13. Ley RE, Turnbaugh PJ, Klein S, Gordon JI. Microbial ecology: human gut microbes associated with obesity. Nature 2006; 444:1022-1023.
14. Hartstra A, Bouter K, Bäckhed F, et al. Insights into the role of the microbiome in obesity and type 2 diabetes. Diabetes Care 2015; 38:159-165.
15. Poupeau A, Postic C. Cross-regulation of hepatic glucose metabolism via ChREBP and nuclear receptors. Biochimica et Biophysica Acta 2011; 1812:995-1006.
16. Al-Assal K, Martínez A, Torrinhas R, et al. Gut microbiota and obesity. Clinical Nutrition Experimental 2018; 20:60-64.
17. Kootte R, Vrieze A, Holleman F. The therapeutic potential of manipulating gut microbiota in obesity and type 2 diabetes mellitus. Diabetes, Obesity and Metabolism 2012; 14:112-120.
18. Ding S, Chi MM, Scull BP, et al. High-fat diet: bacteria interactions promote intestinal inflammation, which precedes and correlates with obesity and insulin resistance in mouse. PloS One 2010; 5: e12191.
19. Boutagy N, McMillan R, Frisard M, et al. Metabolic endotoxemia with obesity: ¿is it real and is it relevant? Biochimie 2016; 124:11-20.
20. Cani P, Amar J, Iglesias M, et al. Metabolic endotoxemia initiates obesity and insulin resistance. Diabetes 2007; 56:1761-1772.
21. Kallio KAE, Hätönen KA, Lehto M, et al. Endotoxemia, nutrition, and cardiometabolic disorders. Acta Diabetol 2015; 52 (2):395-404.
22. Castillo-Rodríguez E, Fernández R, Esteras R, et al. Impact of altered intestinal microbiota on chronic kidney disease progression. Toxins (Basel) 2018; 10(7):300:1-21.
23. Ramezani A, Raj D. The gut microbiome, kidney disease, and targeted interventions. J Am Soc Nephrol 2014; 25:657-670.
24. Osuna-Padilla IA, Leal-Escobar G. Alteraciones en el eje intestino-riñón durante la enfermedad renal crónica: causas, consecuencias y propuestas de tratamiento. Rev Esp Nutr Hum Diet 2017; 21(2):174-83.
25. Ramezani A, Massy Z, Meijers B, et al. Role of the gut microbiome in uremia: a potential therapeutic target. Am J Kidney Dis 2016; 67(3):483-498
Información adicional
Conflictos de interés: La
Dra. Susana Gutt declara haber recibido honorarios por consultoría, disertación
y/o entrenamiento de disertantes de los laboratorios Novo Nordisk, Raffo y Bagó.
La Dra. Fabiana Vázquez manifiesta haber recibido honorarios por consultoría,
disertación y/o entrenamiento de disertantes de los laboratorios Novo Nordisk,
Boehringer Ingelheim, AstraZeneca, Servier, Lilly y Merck. La Gloria Viñez declara
haber recibido honorarios por consultoría, disertación y/o entrenamiento de
disertantes de los laboratorios Servier, Boehringer Ingelheim, Novartis, Merck
Sharp & Dohme, Sanofi Aventis, Bayer y Novo Nordisk. El resto de los
autores declara que no existe conflicto de interés.

