Introducción
El café (Coffea spp.) es un cultivo de suma relevancia a nivel mundial por su alto valor como bebida de consumo (Alemayehu, 2017) y por ser uno de los productos agrícolas más importantes, ocupando el segundo puesto en el comercio internacional luego del petróleo (Labouisse et al., 2008). Las regiones tropicales y subtropicales del mundo son los lugares donde se cultiva mayormente, derivándose, directa o indirectamente de su producción, los ingresos de más de 125 millones de personas (Tran et al., 2016).
El género Coffea L., comprende más de 130 especies, de las cuales las más cultivadas comercialmente son C. arabica L., C. canephora P. y C. liberica Bull. Fernández et al., (2010).Coffea arabica L. es la especie más importante y la preferida en el mercado, teniendo una participación promedio entre las cosechas 2014-2015 y 2015-2016 de 58,1 % en la producción mundial (ICAFE, 2016).
Todas las especies de café, a excepción de Coffea arabica L., Coffea heterocalyx L. y Coffea anthonyi L., son autoincompatibles y además C. arabica L. es la única especie no diploide. La especie Arábica es un alotetraploide autofértil (2n=4x=44), producto de la hibridación espontánea entre Coffea canephora Pierre (progenitor paterno) y Coffea eugenoides L (progenitor materno) (Lashermes et al., 1999), con un tamaño de genoma de 1300 Mpb (Lashermes et al., 2008).
Las diferentes ploidías en el género Coffea obstaculizan la introducción de características agronómicas de las especies diploides hacia las tetraploides y por esto, es tan importante el uso de técnicas que puedan romper estas barreras entre especies y que sirvan para complementar los programas tradicionales de mejoramiento genético y, a la vez la base genética disponible.
El mejoramiento del café y la obtención de un nuevo cultivar con base en las metodologías tradicionales, es un proceso que requiere alrededor de treinta años (Melese, 2016) y esfuerzos, ya que comprende varios pasos como la selección de las especies o variedades a utilizar, su consiguiente hibridación y evaluación de la progenie resultante, en algunos casos retrocruces, y cruces interespecíficos (Orozco y Schieder, 1982).
El cultivo in vitro de células y tejidos vegetales desempeña un papel importante en la biotecnología agrícola. La embriogénesis somática como método de regeneración de plantas se ha logrado en un gran número de familias y especies y se ha usado para los estudios básicos de fisiología vegetal y en aplicaciones más prácticas, como la micropropagación y la transformación genética.
En este sentido la embriogénesis somática es el método más estable, y consiste en el desarrollo de los procesos por el cual células somáticas dan origen a un embrión somático sin intervención de gametos (Mesén y Jiménez 2016). La embriogénesis somática fue descrita por primera vez en Coffea canephora (var. Robusta) por Staritsky (1970) y Coffea arabica en 1977 por Sondahl y Sharp, quienes describieron la inducción de embriones a partir de callo.
La aplicación de la embriogénesis somática para la multiplicación acelerada de plantas de café se ha desarrollado a partir de numerosas técnicas que simplifican este proceso que busca establecer la producción de plantas de gran potencial y reducir los costos de producción de posturas. Existen diversos trabajos que han descrito la embriogénesis somática directa en café, esta vía de regeneración de plantas permite reducir el tiempo de cultivo, disminuye los costos de producción y reduce la frecuencia de variación somaclonal respecto a la vía indirecta. Por otro lado, la embriogénesis somática directa con frecuencia es descrita como de baja frecuencia y la vía indirecta como un método de alta frecuencia (Etienne et al., 2016).
La gran cantidad de protocolos disponibles en la literatura, reflejan que el café no es una especie con problemas para la embriogénesis somática. Sin embargo, se ha descrito una gran variabilidad en la eficiencia de regeneración, esto ha sido debido a las diferencias que muestran los genotipos incluso con empleo de un mismo protocolo.
Al respecto la literatura consultada plantea que los porcentajes de germinación de los embriones somáticos no superan el 60% y no siempre se logra una germinación completa (Barbón et al., 2014). Generalmente, es posible inducir embriogénesis somática en Coffea canephora variedad Robusta, sólo con la presencia de la Citocinina 6-Benzilaminopurina (BAP) en el medio de inducción.
Sin embargo, en algunos clones no se obtienen buenos resultados con este medio y en ciertos casos el desarrollo de callo embriogénico es un proceso largo, que va de seis a diez meses dependiendo del genotipo (López-Gómez et al., 2010; López-Gómez et al., 2011).
Teniendo en cuenta que el Velazco 5 es un híbrido interespecífico que solamente puede ser propagado vegetativamente o con el empleo de técnicas biotecnológicas, se hace necesario investigar combinaciones de Auxinas y Citoquininas que permitan establecer un protocolo eficiente para obtener embriones somáticos y regenerar plantas de este híbrido
Objetivo: Evaluar el efecto de diferentes combinaciones de Auxinas y Citoquininas en la embriogénesis somática del híbrido de café Velazco-5.
Materiales y métodos
La investigación
se realizó en el laboratorio de biotecnología del Instituto de Investigaciones Agroforestales, Tercer Frente, Santiago de
Cuba, durante el período comprendido entre diciembre del 2020 a septiembre del 2021.
Obtención de las vitroplantas
Como explante se tomaron hojas tiernas de plantas madres del híbrido de café Velazco -5, que crecerán en aisladores biológicos. Las hojas se lavaron con agua estéril y se sumergieron en una solución de etanol 70% por 30 segundos, luego se les adicionó una solución al 2% NaOCl durante 30 min. Al finalizar las hojas se enjuagaron tres veces con agua destilada estéril con Cisteína, luego fueron cortadas en segmentos de 1cm2, colocadas en pomos de cristal con los medios de cultivo.
El medio de cultivo utilizado fue Murashige y Skoog (1962) (MS), suplementado con Mioinositol 100 mg.L-1, sacarosa 30 g.L-1 y solidificado con Agar Planta 8 g.L-1. En la fase de multiplicación se suplementó el medio de cultivo con Bencilaminopurina (BAP) 4 mg.L-1 y ácido indolacético (AIA) 0,65 mg.L-1. En la fase de enraizamiento se suplementó con AIA 1 mg.L-1 y AIB 1 mg.L-1. El pH del medio de cultivo fue ajustado a 5,7.
Los cultivos in vitro se mantuvieron en cámaras de crecimiento a temperatura de 25 1°C, humedad relativa 60%, iluminación de 23 mol m-2s-1 (flujo de fotones fotosintéticos) con lámparas de luz fluorescente, fotoperíodo 16 h luz y 8 h oscuridad. Estas serán ubicadas en cámaras de crecimiento con un diseño completamente aleatorizado en condiciones controladas de laboratorio y los datos se procesarán con el programa Statistic 8.0, se utilizará la prueba de Duncan para comparar las medias, previa transformación de los datos X’ = (arcsen √x).
Efecto de la concentración de Auxina 2,4-D y la Citoquinina 6-BAP en la inducción de callos potencialmente embriogénicos del híbrido café Velazco-5.
Este experimento tuvo como objetivo determinar la influencia de concentraciones de la Auxina 2,4-D y la Citoquinina 6-BAP en la inducción de callos potencialmente embriogénicos del híbrido de café Velazco-5. Para la inducción callogénica se utilizaron segmentos de hojas procedentes del híbrido de café Velazco-5, los mismos fueron colocados con el haz sobre el medio de cultivo, durante cuatro semanas en condiciones de oscuridad a 25 ºC.
Se empleó el medio de cultivo propuesto por Hermoso y Menéndez (2000), constituido por sales Murashige y Skoog (MS) 50%, 100 mg/l Mioinositol, 35 mg/l Cisteína, 10 mg/l Tiamina, 1 mg/l de Piridoxina, 1 mg/l de Ácido Nicotínico, 30 g/l Sacarosa y 2.4 g/l Gelrite, a pH de 5,8. Este medio de cultivo fue enriquecido con diferentes concentraciones y reguladores de crecimiento: 2,4-ácido Diclorofenoxiacético y Kinetina.
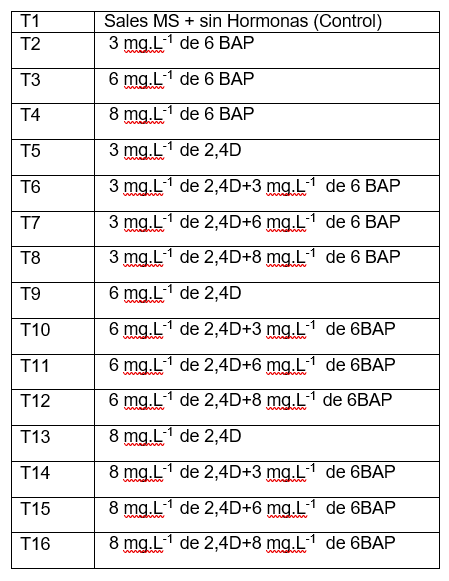
Tratamientos
Se evaluó el número de explantes con formación
de callo (%); color y textura de callo, clasificados en friable o no friable, según lo
planteado por (Ortiz et al., 2017).
Análisis estadístico
A partir de los
datos obtenidos se realizó un análisis de varianza, para el modelo matemático correspondiente a un diseño de bloques al
azar. Se utilizó el Test de Comparación de Rangos
Múltiples de Duncan para un 95 %) para separar las medias (Duncan, 1995). Con vista a llevar a cabo este procesamiento y análisis estadístico se utilizó el paquete STATGRAPHICS PLUS versión 5.0.
Resultados y discusión
Efecto de la concentración de Auxina 2,4-D y la Citoquinina 6-BAP en la inducción de callos potencialmente embriogénicos del híbrido café Velazco-5.
Con relación a la variable se muestra en la figura 1 que hubo diferencias significativas entre los tratamientos donde destacan en la formación de callos los tratamientos T11, T10 y T12 respectivamente con un valor de inducción de callos que alcanza con el tratamiento T11 de 94,13% en el híbrido de café Velazco-5. Estos resultados pudieran estar causados por la presencia de estimulante y su interacción con otras hormonas que regulan numerosas funciones específicas de las células, así como la capacidad que tiene este producto de provocar efectos beneficiosos atribuidos a la presencia de hormonas naturales y otros compuestos que influyen en el crecimiento de las plantas.
Este comportamiento (figura 2) del incremento del crecimiento puede estar dado por la acción del estimulante en la zona del punto de crecimiento de las plantas, donde es capaz de activarse la división y el alargamiento celular mediante la actividad de sustancias de crecimiento presente en las plantas, como las Auxinas, Giberelinas, Citoquininas, entre otras (Vázquez y Torres, 2001).
No se observó explantes oxidados y con relación a ello, por su parte López-Gómez et al. (2010) obtuvieron más del 50% de explantes oxidados al usar 3,5% NaOCl; Paredes et al. (2013), realizaron la desinfección de hojas de café con 1,5% de NaOCl por 20 minutos y el 10% de los explantes presentaron oxidación. Estos resultados favorables se deben a la baja concentración de NaOCl y tiempo de inmersión utilizados en el experimento. Además, se tuvo en cuenta otras estrategias descritas por Azofeifa (2009) como el estado juvenil de las hojas, las sales del medio de cultivo a la mitad de concentración y la incubación en oscuridad.
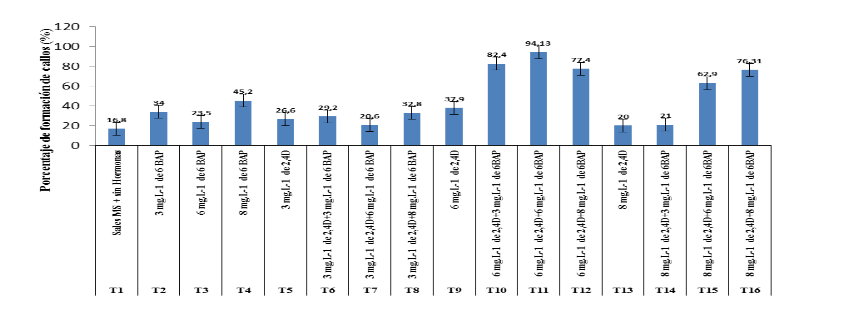 Figura 1.
Efecto de la concentración de Auxina 2,4-D y la Citoquinina 6-BAP en la inducción de callos potencialmente embriogénicos del híbrido de café Velazco-5
Figura 1.
Efecto de la concentración de Auxina 2,4-D y la Citoquinina 6-BAP en la inducción de callos potencialmente embriogénicos del híbrido de café Velazco-5
En investigaciones
los tratamientos que indujo alta tasa de callogénesis
fue T1 (88%), T3 (66%) y T2 (100%)
para la variedad Castillo, Catuaí y Costa Rica 95, respectivamente; sin embargo, no hubo diferencias estadísticas
con los otros niveles de BAP pero sí con los tratamientos con KIN (T4, T5 y T6). La
embriogénesis somática directa no se caracteriza por una formación de callos previa a la formación de embriones; a
pesar de ello, se observaron callos
pequeños y no diferenciados con el borde del explante,
por lo que se les denominaron callos de cicatrización, reportado también por López-Gómez et al. (2016).
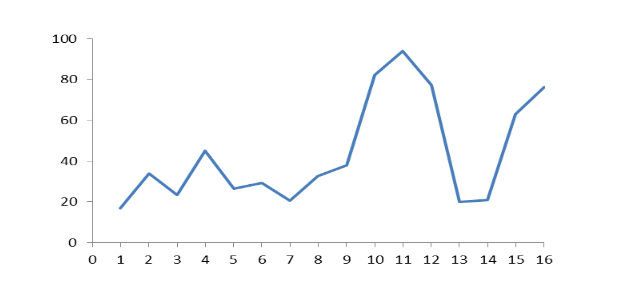 Figura 2.
Progresión lineal de las
diferentes concentraciones de Auxina 2,4-D y la Citoquinina 6-BAP en la inducción de callos potencialmente embriogénicos del híbrido de café Velazco-5
Figura 2.
Progresión lineal de las
diferentes concentraciones de Auxina 2,4-D y la Citoquinina 6-BAP en la inducción de callos potencialmente embriogénicos del híbrido de café Velazco-5
Respecto a la
evaluación de callogénesis, todos los tratamientos
(T7-T12) presentaron alta tasa de
formación de callos (92-100%), en las tres variedades, sin diferencias
estadísticas significativas. Autores
afirman que la adición de la Auxina 2,4-D permite la inducción de callo, así lo reportaron Paredes et al. (2013),
López-Gómez et al. (2016), Montes-Cruz et
al. (2017) y Avila-Victor et al. (2018), al usar diferentes concentraciones de 2,4-D, solo o con una Citoquinina,
para obtener 100% de explantes con callogénesis en diferentes variedades de café.
Conclusiones
Los tratamientos T11; T10; T12 respectivamente los cuales se les aplicó diferentes concentraciones de Auxina 2,4-D y la Citoquinina 6-BAP inducen callos potencialmente embriogénicos en el híbrido de
café Velazco-5
Referencias bibliográficas
Alemayehu, D. 2017. Review on genetic diversity of coffee (Coffea arabica L) in Ethiopia. Int. J. Forest. Hort. 3(2):18-27.
Avila-Victor, C.M.; Martínez-Infante, Á.; Ordaz-Chaparro, V.M.; Arjona-Suárez, E.J.; Iracheta- DonJuan, L.; Gómez-Merino, F.C. Robledo-Paz, A. 2018. Embriogénesis somática directa e indirecta en Coffea arabica var. Colombia. Agroproductividad 11(4): 30-35.
Azofeifa, Á. 2009. Problemas de oxidación y oscurecimiento de explantes cultivados in vitro.
Agronomía Mesomeamericana 20(1): 153-175.
Barbón R, Nguyen H, Capote A, de Feria M, Pérez A, Rivero L, Leiva M, O Hurtado (2014) Efecto de mezclas de sustratos en la fase de conversión de plantas de Coffea arabica L. cv. ‘Caturra rojo’ obtenidas por embriogénesis somática. Biotecnología Vegetal 14(4): 205-213
Etienne, H.; Bertrand, B.; Dechamp, E.; Maurel, P.; Georget, F.; Guyot, R.; Breitler, J.C. 2016. Are genetics and epigenetic instabilities of plant embryogenic cells a fatality? The experience of coffee somatic embryogenesis. Human Genetics and Embryology 6(1): 136-140.
Fernández, R., Z. De-Guglielmo, and A. Menéndez. 2010. Cultivo de tejidos y transformación genética de café. Rev. Invest. 34(71):57-84.
ICAFE (Instituto Del Café de Costa Rica). 2016. Informe sobre la actividad cafetalera de Costa Rica. ICAFE, Heredia, CRI. http://www.icafe.cr/wp-content/uploads/informacion_mercado/informes_actividad/anteriores/2016.pdf (consultado 10 ene. 2018).
Labouisse, J.P., B. Bellachew, S. Kotecha, and B. Bertrand. 2008. Current status of coffee (Coffea arabica L.) genetic resources in Ethiopia: implications for conservarion. Genet. Resour. Crop Evol. 55:1079-1093.
Lashermes, P., A. Carvalho, and H. Etienne. 2008. Genomics of coffee, one of the world’s largest traded commodities. In: P.H. Moore, and R. Ming, editors, Genomics of tropical crop plants. Vol. 1. Plants genetics and genomics: Crops and models. Springer, NY, USA. p. 203-226. doi:10.1007/978-0-387-71219-2_9
Lashermes, P., MC. Combes, J. Robert, P. Trouslot, AD. Hont, F. Anthony, and A. Charrier. 1999. Molecular characterization and origin of the Coffea arabica L. genome. Mol. Gen. Genet. 261:259-266. doi:10.1007/s004380050
López-Gómez, P.; Iracheta-Donjuan, L.; Castellanos-Juaréz, M.; Méndez-López, I.; Sandoval- Esquivez, A.; Aguirre-Medina, J.; Ojeda-Zacarías, Gutiérrez-Díez, A. 2010. Influencia del explante y medio de cultivo en la embriogénesis somática en hojas de café. Revista Fitotecnia Mexicana 33(3): 205-213.
López-Gómez, P.; Iracheta-Donjuan, L.; Ojeda-Zacarías, M.; Ducos, J. Medio de cultivo e inhibidores de etileno en la embriogénesis somatica de café. 2016. Revista Mexicana de Ciencias Agrícolas 7(7): 1749-1757.
Melese, K. 2016. The role of biotechnology on coffee plant propagation: A current topics paper.
J. Biol. Agric. Healthcare 6(5):13-19.
Mesén, F; Jiménez, LD. 2016. Producción de clones de café por miniestacas. Turrialba, Costa Rica, CATIE. Serie Técnica, Manual Técnico Nº. 130. 28 p.
Montes-Cruz, S.; Lalama-Aguirre, J.; Echeverría-Féiz, J.; Toromoreno-Arévalo, L.; Salazar- Torres, S.; Benavides-Burgos, E.; Atiaja-Llamba, J. 2017. Obtención de embriones somáticos de cafeto a partir de explantes de hojas de las variedades Bourbón Cidra, Caturra Rojo y SL-28 de plantaciones establecidas en la Provincia del Carchi, Zona 1, Ecuador. Dominio de las Ciencias 3(2): 918-942.
Murashige, T.; Skoog, F. 1962. A revised medium for rapid growth and bioassays with tobacco tissue culture. Physiol Plant 15: 473-497.
Orozco, F.J., y D. Schieder. 1982. Aislamiento y cultivo de protoplastos a partir de hojas de café. Cenicafé 33(4):129-136.
Ortiz N, Barbón R, Capote A, Pérez A, Robaina M (2017) Caracterización morfológica en vivero de plantas de Coffea arabica L. cv. Caturra rojo J-884 obtenidas por embriogénesis somática. Biotecnología Vegetal 17(4): 251-257
Paredes, G.; Peña, C.; Jadán, M. 2013. Obtención de embriones en fase cotiledonar de Café Robusta (Coffea canephora) con el empleo de un sistema de inmersión temporal, mediante la técnica de embriogénesis somática a partir de segmentos foliares. ESPE. Sansolquí, Ecuador. 21 pp.
Staritsky G (1970) Embryo formation in callus tissues of coffee. Acta Bot. Neerlandica 19:509– 514.
Tran, H.T., L. Slade, A. Furtado, H. Smyth, and R. Henry. 2016. Advances in genomics for the improvement of quality in coffee. J. Sci. Food Agric. 96:3300-3312.