



DIVERSIDAD Y DISTRIBUCIÓN ESPACIAL DE LOS ANFIBIOS DEL RIO SIRAÍN EN EL BOSQUE MUY HÚMEDO TROPICAL, KANKINTÚ, BOCAS DEL TORO, 2022
Diversity and spatial distribution of the amphibians of the Siraín River in the Very Humid Tropical Forest, Kankintú, Bocas del Toro, 2022
Revista Colegiada de Ciencia
Universidad de Panamá, Panamá
ISSN-e: 2710-7434
Periodicidad: Semestral
vol. 5, núm. 1, 2023
Recepción: 07 Abril 2023
Aprobación: 03 Julio 2023
Resumen: En el río Siraín, distrito de Kankintú, comarca Ngäbe Buglé se determinó la distribución espacial de los anfibios utilizando tecnologías SIG. Se encontraron 11 especies pertenecientes a seis familias en seis muestreos durante los años 2016, 2018 y 2022. A diferencia de la estructura de las comunidades de anfibios para tipos de bosque similares en América Central, se obtuvo una baja riqueza específica, con pocos individuos y con diversidad de Shannon (H= 2.02), lo que puede estar relacionado con el impacto antrópico a los bosques y a los ríos de Kankintú. De las especies encontradas D. auratus y O. pumilio, presentaron estado de conservación con medida de vulnerabilidad según ley nacional.
Palabras clave: Distribución espacial, diversidad de anfibios, tecnologías SIG.
Abstract: In the Siraín river, Kankintú district, Ngäbe Buglé region, the spatial distribution of amphibians was determined using GIS technologies. 11 species belonging to six families were found in six samplings during the years 2016, 2018 and 2022. Unlike the structure of amphibian communities for similar forest types in Central America, a low specific richness was obtained, with few individuals and with diversity Shannon (H= 2.02), which may be related to the anthropogenic impact on the forests and rivers of Kankintú. Of the species found, D. auratus and O. pumilio presented conservation status with a vulnerability measure according to national law.
Keywords: Amphibian diversity, GIS technologies, spatial distribution.
Introducción
Panamá cuenta con un 3% de la herpetofauna total mundial. Se estima que la herpetofauna panameña está compuesta por 207 especies de anfibios (Jaramillo et al. 2010). Los estudios de herpetofauna en Panamá han aumentado, gracias a los trabajos de (Carrizo, 2010; Crawford et al., 2010; Huq, S., 2014; Batista et al., 2014), a pesar de esto, son pocos los antecedentes para la comarca Ngäbe Buglé.
En la comarca Ngäbe-Buglé se han deforestado 817.83 hectáreas, con una tasa anual de 102.24 hectáreas. Principalmente para las actividades agropecuarias, en los distritos de Kankintú y Kusapín, reduciendo su cobertura vegetal primaria a un ritmo de 10% en las últimas décadas (ANAM, 2003). En la actualidad, se encuentra cubierta por 35% de bosques maduros o bosques primarios y el desarrollo incontrolado de sus usos, las prácticas agrarias inapropiadas, la tala indiscriminada, la contaminación de los ríos y quebradas con basura y detergentes, son los problemas ambientales que amenazan la conservación de los recursos en la comarca (Hidalgo et al., 2020). Esto podría estar implicando una disminución de la biodiversidad de algunos taxones susceptibles e indicadores de la calidad ambiental, como lo son los anfibios.
Por este motivo, el objetivo de la siguiente investigación es determinar la diversidad y la distribución de los anfibios del río Siraín en el Bosque Muy Húmedo Tropical del distrito de Kankintú, comarca Ngäbe Buglé, Bocas del Toro.
MATERIALES Y MÉTODOS
Área de Estudio
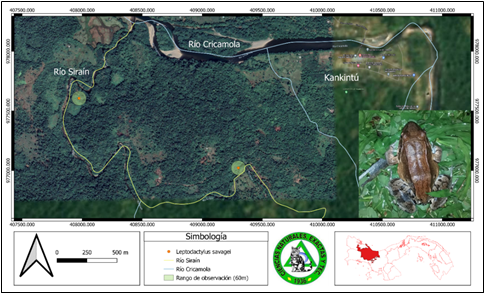
El estudio se realizó en Bosque Muy Húmedo Tropical, que rodea el cauce del río Siraín, ubicado en el corregimiento de Kankintú, distrito de Kankintú, Comarca Ngäbe Buglé, provincia de Bocas del Toro. La longitud del área de muestreo es de aproximadamente 2.5 km y se georreferencia en el punto 8° 50' 56" N y 81° 49' 58" W. Presenta clima tropical, del tipo Afi de acuerdo con el sistema de clasificación Köppen-Geiger, con precipitaciones de ± 2557 mm al año.

El río Siraín se encuentra a una altitud de 25 m.s.n.m. en el Bosque Muy Húmedo Tropical de Kankintú, donde el mes con el promedio de temperatura más alta es abril con (28.8°C). El mes más frío es enero con (17.8°C). El mes con la humedad relativa más alta es octubre, con (85%). El mes con la humedad relativa más baja es marzo, con (72%). El área de muestreo cuenta con una longitud aproximada de 2.5 Km entre los tres transectos, en la vegetación adyacente al río Siraín, la cual se ve limitada con pocos árboles y arbustos, con pequeñas pendientes y áreas planas poco intervenidas. Algunos lugareños han modificado la vegetación improvisando caminos, casas y siembras, lo que ha modificado el tipo de bosque. En la parte más alta del río, existe el bosque primario, hay pocos arbustos y encontramos pendientes sinuosas.

Categorías de microhábitats
Para este estudio se consideraron algunos microhábitats, solo para referenciar el sitio donde un organismo realiza alguna actividad, ya sea cerca del agua o en áreas circundantes (Alfonso et al., 2009). Se integraron diferentes tipos de microhábitats, siendo estos: suelo desnudo, planta/ herbácea, tronco/arbusto, pasto/agua, agua, roca, hojarasca y pastos.
Recolección de datos
El muestreo se llevó a cabo entre los meses de (mayo-junio) de 2016; (marzo-abril) de 2018 y (agosto-septiembre) de 2022, completando doce visitas e invirtiendo seis horas por día. El inventario se realizó usando la técnica regular de registro visual. El principal método de muestreo utilizado fue el registro por encuentros visuales (VES, Visual Encounter Survey) (Heyer et al., 1994). Este método es muy práctico cuando se realizan evaluaciones ecológicas rápidas (Cañizales, 2020). Además, son muy buenos para determinar la riqueza de especies del área y la composición de las especies del ensamble local (Crump y Scott, 1994).
Los recorridos se efectuaron entre las 10:00 a 15:00 h cubriendo aproximadamente 500 m en cada transecto y 500 metros de separación entre cada uno y se utilizaron dos personas. Una vez encontradas, las especies se fotografiaban y se tomaba un punto de georreferenciación utilizando un GPS Garmin eTrex 20.
Análisis de la Información
En cada muestreo se contaban y fotografiaban las especies. Se midieron los índices de Riqueza de Especies (S), Diversidad de Shannon-Wiener(H’), Equidad de Pielou (J’) y el de Abundancia Relativa; empleando los programas estadísticos Past 3.17, SigmaPlot 12.0 y Excel 2016 de Microsoft Office 2016.
Se elaboraron curvas de acumulación para estimar la completitud del muestreo de anfibios con el estimador de riqueza Chao1. Los cálculos se realizaron con el Software EstimateS 9.0 (Colwell et al., 2012).
Para identificar las especies de anfibios, se empleó la Clave de anfibios y reptiles de Costa Rica de Savage, J. (2002) y Guía de campo de Anfibios de Costa Rica de Leenders, T. (2017). Para el estado de conservación de las especies, se utilizó: El Informe sobre el Estado del Conocimiento y Conservación de la Biodiversidad y de las Especies de Vertebrados de Panamá, 2007 y la Lista Roja de la UICN (López y Morales, 2020).
Para los mapas de distribución espacial para cada especie de anfibios en la cobertura boscosa aledaña al río Siraín, se consideró el punto GPS tomado para cada uno de los individuos encontrados. Éstos fueron tomados con el datum WGS84 / UTM zone 17N y colocados luego en el programa QGIS 3.26.2. Se hizo un buffer con una distancia de 60 m, establecida por el rango aproximado en que se podía observar una especie en un transecto.
RESULTADOS
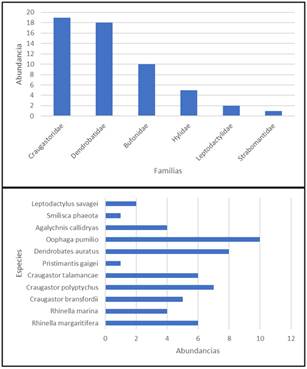
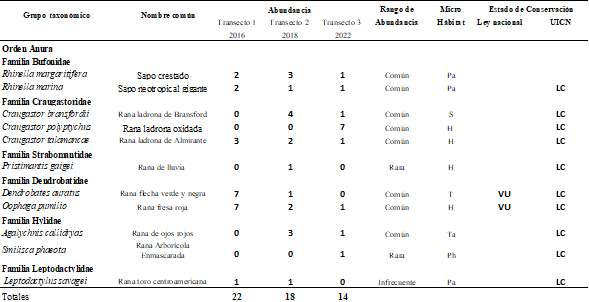
En total, se encontraron once especies de anuros para los transectos establecidos en el río Siraín (Tabla 1). La familia más abundante fue Craugastoridae con 18 individuos y la especie más abundante fue Oophaga pumilio con 10 individuos (Figura 3). Oophaga pumilio y Dendrobates auratus se consideran vulnerables según Ley Nacional y todas las restantes de preocupación menor, según la lista roja de la UICN (Tabla 1).
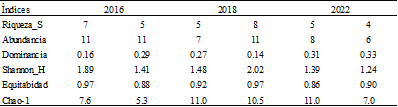
Distribución espacial de los anfibios en río Siraín Kankintú
Familia Bufonidae
Rhinella margaritifera (Laurenti, 1768) Sapo crestado (Figura 6).
Ampliamente distribuido por la mayor parte de la cuenca amazónica y por el este de Panamá. Generalista de una amplia variedad de hábitats, incluyendo ecosistemas alterados por el hombre. En este estudio,
En el río Siraín, es una especie bastante común, fue colectado en el transecto 2, donde hay impacto antrópico del hábitat, pero este parece ser muy tolerante al ambiente degradado. En este estudio, fue una especie muy activa durante la estación lluviosa, concentrándose muy cercana a la zona ribereña, lo cual coincide con el trabajo de (Gentry y Dodson, 1987).
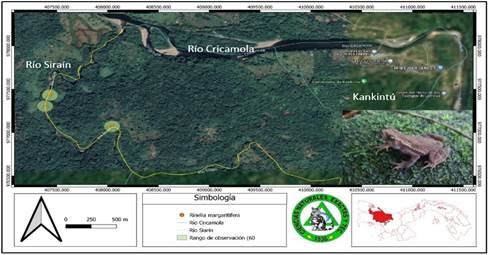
Rhinella marina (Linnaeus 1758) Sapo neotropical gigante (Fig. 7).
Esta especie está ampliamente distribuida, desde Estados Unidos hasta el sur de Bolivia y Brasil. Parece ser una especie que se adapta muy bien a la intervención antrópica, adquiriendo una aparente tolerancia. En el estudio, fue común verlo por la tarde y noche que durante el día y se puede encontrar en áreas abiertas, naturales o con impacto antrópico, como lo describe en su trabajo (Toft y Duellman, 1979, Székely et al., 2016). En el río Siraín, muestra una aparente preferencia por sitios impactados donde alcanza grupos muy numerosos. Esta especie es más activa durante la estación seca, y aprovecha los microhábitats suelo, pasto/agua que estén muy cerca de las fuentes de agua, igual como lo explica (Cogger, 2018).
Familia Craugastoridae
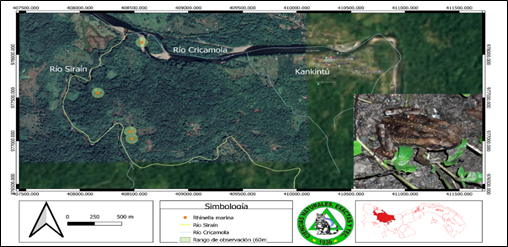
Craugastor bransfordii (Cope, 1886) Rana ladrona de Bransford (Fig. 8).
Esta especie se encuentra en Costa Rica, Nicaragua y Panamá abarcando bosques húmedos subtropicales o tropicales y es una de las más abundantes especies de anfibios en el Bosque Tropical Montano Bajo en la Cordillera de Talamanca (Savage, 2002; Acosta et al., 2015).
Está amenazado por la pérdida de hábitat. Su estado de conservación en términos del estado de la UICN (Lista Roja) es de Preocupación Menor (LC). Esto se correlaciona con el estudio en río Siraín, pues resultó muy común en el transecto 2, por el cual pasa una trocha que utilizan los lugareños para trasladarse de una comunidad a otra, demostrando su tolerancia a la presencia de las personas.
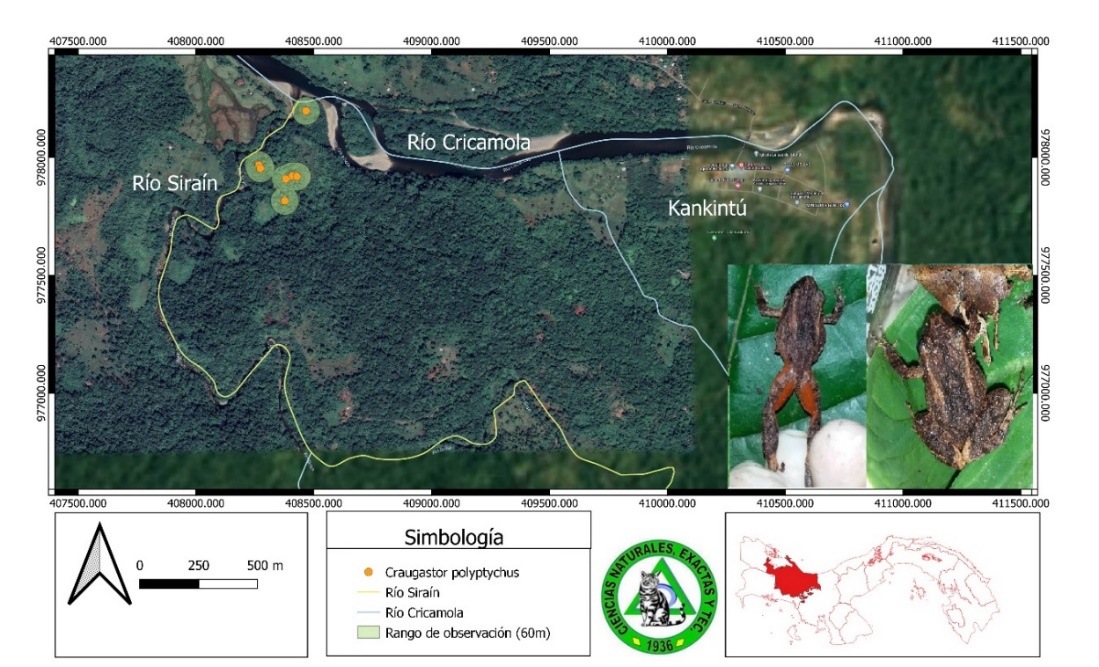
Craugastor polyptychus (Cope, 1886) Rana ladrona oxidada (Fig. 9).
Esta especie se puede encontrar en las tierras bajas húmedas de Nicaragua hasta Panamá, donde es común en bosques húmedos subtropicales o tropicales de tierras bajas, plantaciones y bosques muy impactados (Folt y Reider, 2013). En este estudio, figura como una especie adaptable y es poco probable que enfrente amenazas significativas, solo la pérdida de hábitat. Esto se demuestra, pues su población se encuentra en el transecto 3, cercano a una finca agropecuaria.
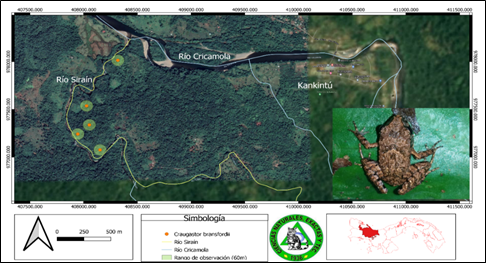
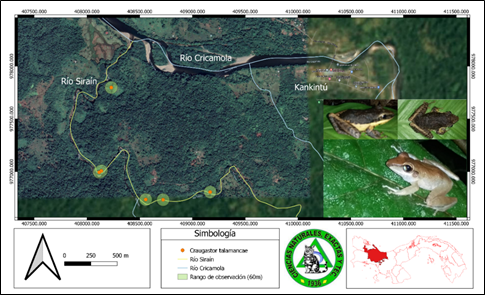
Craugastor talamancae (Dunn, 1931) Rana ladrona de Almirante (Fig. 10).
Presenta una barra oscura atravesando el ojo y barrando los brazos y las piernas, la cual es una característica distintiva en esta especie. Se encuentra en tierras bajas húmedas y bosques primarios y secundarios montanos a una altitud de 15 a 646 m sobre el nivel del mar. En este estudio, se observó al final del día en hojas de ramas y hojarasca. Está aparentemente amenazado por la deforestación del sitio, demostrando ser una especie común, pero que se mantiene alejada de las zonas con impacto agropecuario, su población fue mayor en el transecto 1.
Familia Strabomantidae
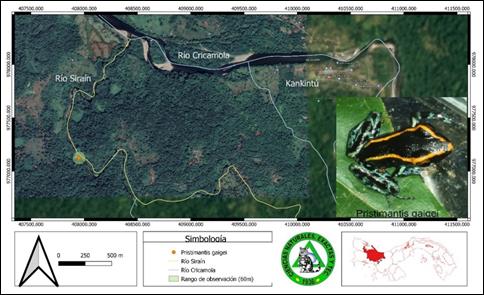
Pristimantis gaigei (Dunn, 1931) Rana de lluvia de Gaige (Fig. 11).
Se encuentra en las tierras bajas del Atlántico desde Costa Rica hasta el centro de Colombia. En este estudio, se encontró solitaria en la hojarasca y asociado a coberturas boscosas más densas en el transecto 2. Estas ranas representan un caso de mimetismo batesiano (Bayazit, 2010; Leenders, 2017), donde imitan la coloración de las ranas venenosas (Dendrobatidae). La especie presenta dos rayas dorsolaterales doradas, que las hace lucir como Phyllobates aurotaenia y Phyllobates lugubris las cuales son muy tóxicas.
Familia Dendrobatidae
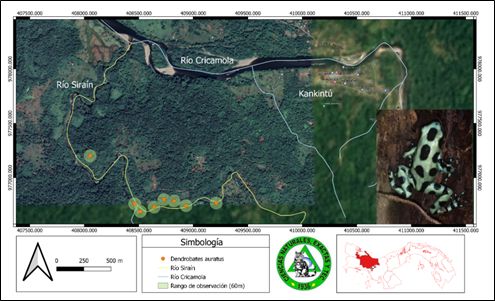
endrobates auratus (Girard, 1855) Rana flecha verde y negra (Fig. 12).
Es una especie de anfibio anuro muy común en el suelo de los bosques de Centroamérica desde el sur de Nicaragua hasta el noroeste de Colombia (Acosta y Cuentas, 2016). Fueron observados durante el día. Tiene una coloración muy variable con coloraciones verdes a azulado o crema. Se alimenta de insectos venenosos y no venenosos como escarabajos y hormigas que habitan en su localidad, de los que consigue su veneno; que contiene unos 90 alcaloides (Myers y Daly, 1976). Algo particular en el río Siraín, fue que solo se encontró en el transecto 2 asociada a la hojarasca y troncos de árboles caídos, siendo tan común.
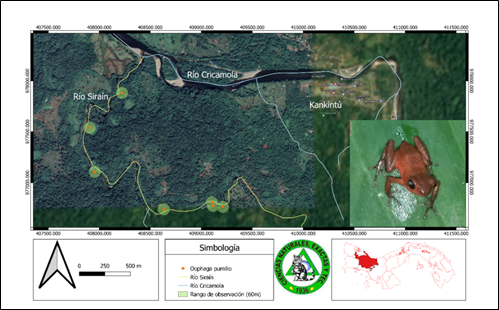
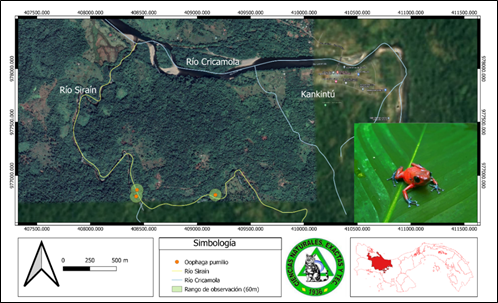
Oophaga pumilio (Schmidt, 1857) Rana fresa venenosa (Fig. 13 a y b).
La rana fresa o rana venenosa de blue jeans (Oophaga pumilio, antes Dendrobates pumilio) es una especie de tamaño pequeño distribuida en América Central, donde es muy común, extendiéndose desde el centro este de Nicaragua a través de Costa Rica y el noroeste de Panamá (Frost, 2023).
Este estudio resultó común en los tres transectos, en la parte más alta del río relacionada a bosques premontanos muy poco intervenidos, y en la parte más baja asociada a troncos, suelo y hojarasca; pues esta especie aprovecha, troncos, arbustos, bromelias y hojarasca para su ciclo de vida (Strynoski, 2012). En río Siraín, se registraron dos subespecies de esta rana venenosa, una asociada a hojarasca en todos los transectos (Figura 13 a) y otra solo en el primer transecto (Figura 13 b), tal vez, porque estos microhábitats contienen las hormigas que componen su dieta (Bolton et al., 2017).
Familia Hylidae
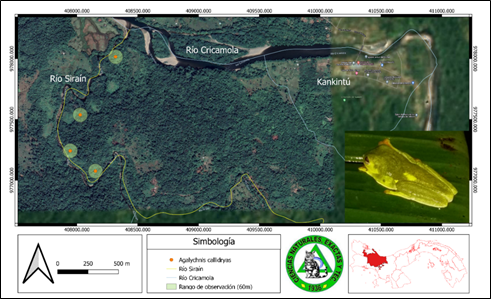
Agalychnis callidryas (Cope, 1862) Rana de ojos rojos (Fig. 14).
Agalychnis callidryas es nativa de Belice y su distribución continua en las montañas del Caribe hasta Panamá (Gómez et al., 2018; McCranie, 2006). Las diferencias morfológicas intraespecíficas sugieren la existencia de tres poblaciones diferentes, en América Central y Panamá (Duellman, 2001). Para este estudio se encontró en el transecto 2, en arbustos cercanos al bosque premontano, donde destacan las formaciones de charcas temporales importantes para su reproducción y donde parecen tolerantes a los bosques secundarios, siempre que no estén tan degradados (Gómez et al., 2018).
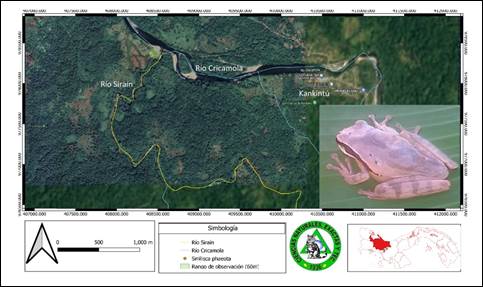
Smilisca phaeota (Cope, 1862) Rana Arborícola enmascarada (Fig. 15).
Se distribuye en Colombia, Costa Rica, Ecuador, Honduras, Nicaragua y Panamá, hasta los 1, 600 msnm (Gómez et al., 2018), también algunos registros en hábitats premontanos demuestran la presencia de ella (Hernández et al., 2015). Esta rana arborícola es fácil de reconocer debido a la presencia de una máscara oscura (Savage, 2002). En el río, Siraín es una especie muy poco extendida o abundante. Estudios demuestran que es una especie adaptable a zonas perturbadas (Savage, 2002; Gómez et al., 2018). Fue observada en un área bastante intervenida por la construcción de viviendas, la expansión de tierras para cultivos y por el ruido de los motores de los botes que transitan el río.
Familia Leptodactylidae
Leptodactylus savagei (Heyer, 2005) Rana Toro Centroamericana (Fig. 16).
Es una especie de rana que se extiende desde el este de Honduras, a través de Nicaragua, Costa Rica y Panamá hasta Colombia. Puede medir de 106 a 156 mm para los machos y de 110 a 164 mm para las hembras. Los adultos de esta especie son depredadores de prácticamente cualquier cosa que puedan comer. Es una especie común sin amenazas reales conocidas (Leenders, 2017). En este estudio, se observó y se escuchó su llamado es muy fuerte y repitente en la zona de pastos muy cercanos a cuerpos de agua estancada en los transectos 1 y 2 los cuales aprovecha, posiblemente, para atraer y fecundar a las hembras.
DISCUSIÓN
Diversidad y distribución espacial de los anfibios de río Siraín, Kankintú, comarca Ngäbe Bugle.
Se reportaron en el área del río Siraín, un total de 11 especies de anfibios, agrupadas en 8 géneros, seis familias (Tabla 1). Esta riqueza representa el 4.7% de las especies de anfibios reportados para Panamá (Quiroz, 2020).
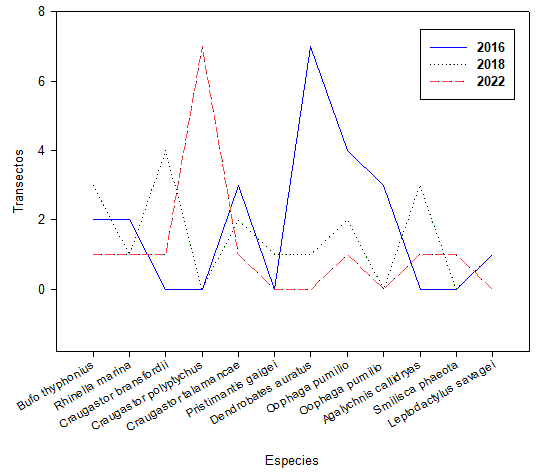
La riqueza de anfibios encontrada es más baja que la descrita por Medina et al., (2019) para bosque tropical de tierras bajas adyacentes a zonas ribereñas en el trópico; lo que puede estar relacionado con el impacto al ecosistema en Kankintú, comarca Ngäbe Buglé. La abundancia demostró ser mayor en el 2016, en el primer transecto, encontrado en la parte más distante a la población y su impacto (Figura 4).
Respecto a la distribución espacial de las especies en los mapas diseñados con tecnología SIG, no se dispone de antecedentes para establecer comparación y analizar, pero los resultados obtenidos indican, que no hay una sola especie que no comparta un espacio dentro del área estudiada, con al menos una especie diferente. Todos los anfibios habitan coexistiendo con otros, lo que se debe probablemente a competencia o que la limitación principal es la necesidad de estar cerca del agua. Para poder determinar la razón de esta convivencia, serán necesarios más estudios sobre usos de los microhábitats y la relación con el impacto antrópico, transición de cobertura vegetal y caracterización fisicoquímica del agua y el suelo. Pues, se observó que en su mayoría las especies se encontraban en áreas de transición de cobertura vegetal, tal vez, impulsados por la tala y el tránsito de personas por las trochas improvisadas.
La familia Craugastoridae presentó la mayor riqueza, debido a que son el grupo de vertebrados terrestres más diversificado, incluyen ranas con desarrollo directo sin requerimientos de cuerpos de agua (Acosta y Cuentas, 2016), pudiendo ocupar diferentes ambientes en los transectos seleccionados, haciendo mejor uso de sus recursos. Las especies menos abundantes fueron P. gaigei y S. phaeota (Tabla1), a pesar de sus rangos de adaptabilidad y tolerancia en bosques poco intervenidos (Palacios et al., 2018) su baja diversidad y abundancia durante los tres años de muestreo indican una aparente preocupación.
Otros estudios en Panamá señalan a Strabomantidae entre las más diversas en las áreas boscosas de montaña (Cedeño et al., 2006; Sosa y Guerrel, 2013), pero para este estudio, solo se observó la especie P. gaigei posiblemente por la deforestación experimentada en estos últimos años. De igual forma O. pumilio y D. auratus encuentran en río Siraín un sitio muy bueno para su supervivencia, aunque mantienen un estado de conservación de vulnerabilidad por ley nacional.
La dominancia en los tres transectos, son para las especies: R. margaritifera, C. talamancae y O. pumilio, las cuales se encontraban en los tres transectos, dominando igualmente los microhábitats pasto/agua y hojarasca. Esta situación guarda relación con las especies reportadas por Bonilla (2019) en su trabajo: Anfibios asociados a áreas degradadas por minería en Jigualito, Chocó-Colombia 2020.
El índice de diversidad de Shannon-Wiener (H’=2.02), y el índice de equitatividad (J’= 0.97), obtenidos durante la estación lluviosa del 2018 en el segundo transecto, sugieren una distribución bastante homogénea de los individuos reportados (Tabla 2). Posiblemente atribuible a la precipitación que modifica el clima beneficiando a los anfibios los cuales son los vertebrados que pierden agua más rápido, desplazando a las especies menos tolerantes. De la misma forma, e esperaba encontrar mayor abundancia y diversidad en el tercer transecto, pues durante la pandemia se esperaba que los organismos aumentaran su abundancia, pero sucedió lo contrario.
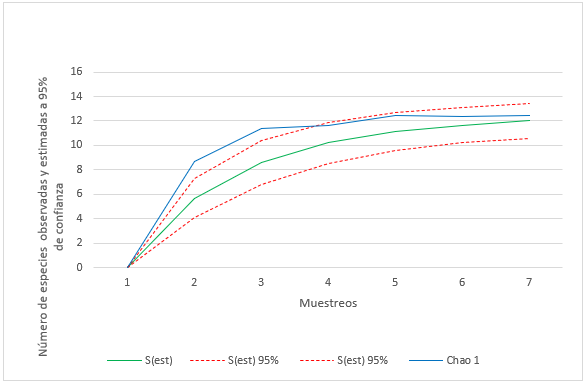
La riqueza de especies registrada en el área de estudio y analizada por el estimador de Chao 1, muestra que la curva de acumulación de especies aun no alcanza la asíntota, demostrando así, que faltarían por añadir algunas especies al inventario (Fig. 5). En este sentido, Chao et al. (2005) señalan que la completitud aproximada de los inventarios puede deberse a los valores de las diversidades casi proporcionales entre los transectos. Esto produce que algunas especies de la familia Hylidae y Strabomantidae podrían estar ocultas en la vegetación secundaria por las modificaciones del hábitat, debido a las actividades antrópicas (Palacios et al., 2018), tal como se observó en este trabajo.
Entre la gran variedad de anfibios que podemos encontrar en el Bosque Tropical de Panamá, solo algunas especies se encuentran en las zonas aledañas al río Siraín, lo cual puede ser atribuido a dos situaciones: el impacto humano sobre el río por las actividades de lavado doméstico y las fuertes temporadas de sequias que se hacen perceptibles a finales e inicio del año.
CONCLUSIÓN
Se determinó la distribución de los anfibios en el río Siraín y se categorizaron especies como raras, infrecuentes y comunes. Se registraron 11 especies de anfibios, de las cuales O. pumilio fue la más común y la más rara fue P. gaigei.
La estructura de la herpetofauna observada durante los tres años de observación no representó gran variedad de especies, pero las que se encuentran, utilizan diferentes microhábitats, aprovechando la hojarasca, los pastos o cuerpos de agua. Esto permite la coexistencia de los anfibios y el establecimiento de patrones de distribución espacio temporales.
En general, la riqueza y la diversidad calculada son tan solo una aproximación de la realidad e indican que la proporción de la diversidad es apenas regular, pero lo suficientemente equitativa para mantener la supervivencia de las especies encontradas aun cuando el sitio se encuentra impactado aparentemente por las poblaciones humanas que habitan cerca del río. Se necesita realizar más investigaciones, en el futuro, para tener certeza de la posible causalidad del impacto antrópico en la diversidad de anfibios.
Agradecimientos
Deseo agradecer muy especialmente a la comunidad de Kankintú por haberme permitido realizar este tipo de investigaciones en su población. Además, un especial agradecimiento a los estudiantes del grupo de segundo año de la Licenciatura en Educación del Centro Regional Universitario de Bocas del Toro, Anexo de Kankintú por su ayuda en el muestreo de los anfibios.
REFERENCIAS
Acosta-Chaves, V. J., Chaves, G., Abarca, J. G., García-Rodríguez, A. y Bolaños, F. (2015). A checklist of the amphibians and reptiles of Río Macho Biological Station, Provincia de Cartago, Costa Rica. Check List, 11(6). https://repositorio.una.ac.cr/bitstream/handle/11056/17698/document%20%2812%29.pdf?sequence=1&isAllowed=y
Acosta-Galvis, A.R. y Cuentas, D. (2016). Lista de los anfibios de Colombia: referencia en línea, version 05.2015.0. Batrachia, Villa de Leyva, Boyacá, Colombia. https://www.batrachia.com/orden-anura/craugastoridae-6-spp/
Alfonso, C. A. D., Tessaro, S. A. G., Alberto, C., y González, L. (2009). El hábitat: definición, dimensiones y escalas de evaluación para la fauna silvestre. Manual de Técnicas para el estudio de la Fauna, 317. https://www.researchgate.net/publication/310425829_Manual_de_Tecnicas_para_el_estudio_de_la_Fauna_silvestre
ANAM. (2003). Informe final de la cobertura boscosa y uso de suelo de la República de Panamá, 1992-2000. Autoridad Nacional del Ambiente. https://books.google.com.pa/books?id=ApHcNAEACAAJ&hl=es&source=gbs_navlinks_s
Batista, A., Jaramillo, C. A., Ponce, M. y Crawford, A. J. (2014). A new species of Andinobates (Amphibia: Anura: Dendrobatidae) from west central Panama. Zootaxa, 3866(3), 333-352. https://d1wqtxts1xzle7.cloudfront.net/50175265/Batista_l_14_Andinobates_geminisae_PA-libre.pdf?1478569847=&response-content-disposition=inline%3B+filename%3DA_new_species_of_Andinobates_Amphibia_An.pdf&Expires=1687200880&Signature=bkelnJxs~Fc8oK7h6hm3RR0BT7RNkvqgnodPgW8AMYQLGBoHMnXVNkflM-INia~djizbpsrtg8ql3bfPUDNwn1mP1pbFL-vPM2jmihG1ANBocLLyzXpUQN77LxIdHv-7~1pMm6CEWBxowsAIcE7deUn8zo4p3dvlBHXZ9hN5L4EJEAElwzWGymygXFGV2ySyzr4gHx3VJq~TLhfhL8UL5fyFD4~9HMRhIJWbrJiM2I4jrsgp45Jti9y5txkf7rPkkuSfmda90-eUj9hJBX75G9WrxdhoA~myWhLBs1vTICtA9VBHu0A2ixUZ33yk~py1LpXpI4UhQ8dMcDze-eI~dg__&Key-Pair-Id=APKAJLOHF5GGSLRBV4ZA
Bayazit, V. (2010). Biological activities of nanomaterials (bufadienolides, peptides and alkoloids) in the skin of amphibian on Gammarus pulex L. Digest Journal of Nanomaterials and Biostructures, 5(2), 347-354. https://chalcogen.ro/347_Bayazit.pdf
Bolton, S. K., Dickerson, K. y Saporito, R. A. (2017). Variable alkaloid defenses in the dendrobatid poison Frog Oophaga pumilio are perceived as differences in palatability to arthropods. Journal of Chemical Ecology, 43(3), 273–289. https://doi.org/10.1007/s10886-017-0827-y
Bonilla, N. S. (2019). Anfibios asociados a áreas degradadas por minería en Jigualito, Chocó-Colombia. IIAP. https://www.gbif.org/es/dataset/6704a0e5-71e9-474a-8b0a-e897e3670141
Cañizales, I. (2020). Comunidad de anuros en ambiente de sabana de la cordillera de la costa de Venezuela. Acta biológica venezuelica, 39(1), 107-123. http://saber.ucv.ve/ojs/index.php/revista_abv/article/view/19384
Carrizo Díaz, A. R. (2010). Riqueza y abundancia de la herpetofauna de la cuenca alta del río Santa María, Santa Fé, Veraguas (Tesis Doctoral). Universidad Autónoma de Chiriquí). https://jadimike.unachi.ac.pa/handle/123456789/337
Cedeño, J., Martínez Cortés, V. y Fossatti, H. (2006). Anfibios en la Reserva Forestal la Tronosa: Diversidad y estado de conservación. Tecnociencia, 8(2), 101-114. https://revistas.up.ac.pa/index.php/tecnociencia/article/view/751/640
Chao, A., Chazdon, R. L., Colwell, R. K., & Shen, T. J. (2005). A new statistical approach for assessing similarity of species composition with incidence and abundance data. Ecology letters, 8(2), 148-159. https://doi.org/10.1111/j.1461-0248.2004.00707.x
Cogger, H. G. (2018). Reptiles and amphibians of Australia. (7a ed.). CSIRO Publishing. https://www.amazon.com/-/es/Harold-G-Cogger-ebook/dp/B07JRFQ36K
Colwell, R. K, Chao, A., Gotelli, N. J., Lin, SY, Mao, CX, Chazdon, R.L. y Longino, J. T. (2012). Modelos y estimadores que vinculan rarefacción, extrapolación y comparación de conjuntos basadas en individuos y muestras. Revista de ecología vegetal, 5(1), 3-21. doi: 10.1093/jpe/rtr044
Crawford, A. J., Lips, K. R. y Bermingham, E. (2010). Epidemic disease decimates amphibian abundance, species diversity, and evolutionary history in the highlands of central Panama. Proceedings of the National Academy of Sciences, 107(31), 13777-13782. https://www.pnas.org/doi/pdf/10.1073/pnas.0914115107
Crump, M. L., & Scott, N. J. (1994). Standard techniques for inventory and monitoring. Measuring and monitoring biological diversity: standard methods for amphibians (WR Heyer, MA Donnelly, RW Mc Diarmid, LC Hayek & MS Foster, eds). Smithsonian Institution Press, Washington, 76-141. https://repository.si.edu/handle/10088/19095
Delfín-Alfonso, Ch. A., Gallina-Tessaro, S. A. y López-González, C. A. (2014). El hábitat: definición, dimensiones y escalas de evaluación para la fauna silvestre. En S. Gallina y C. López-González. (Eds.). Manual de Técnicas para el estudio de la fauna. (pp. 283-312). Universidad Autónoma de Querétaro. https://www.researchgate.net/publication/271849889_El_habitat_definicion_dimensiones_y_escalas_de_evaluacion_para_la_fauna_silvestre
Duellman, W. E. (2001). The hylid frogs of Middle America, Volume 1. Society for the Study of Amphibians and Reptiles. Natural History Museum of the University of Kansas. https://books.google.com.pa/books/about/The_Hylid_Frogs_of_Middle_America.html?id=vdj_vQAACAAJ&redir_esc=y
Folt, B. y Reider, K. E. (2013). Leaf-litter herpetofaunal richness, abundance, and community assembly in mono-dominant plantations and primary forest of northeastern Costa Rica. Biodiversity and Conservation, (22), 2057-2070. https://www.researchgate.net/publication/257538505_Leaf-litter_herpetofaunal_richness_abundance_and_community_assembly_in_mono-dominant_plantations_and_primary_forest_of_northeastern_Costa_Rica
Frost, D. R. (2023). Amphibian Species of the World: an Online Reference. Version 6.2. Electronic Database accessible at https://amphibiansoftheworld.amnh.org/index.php. American Museum of Natural History, New York, USA. doi.org/10.5531/db.vz.0001
Gentry, A. H. y Dodson, C. H. (1987). Diversity and biogeography of neotropical vascular epiphytes. Annals of the Missouri Botanical Garden, 74(2), 205-233. https://www.jstor.org/stable/2399395
Gómez-Hoyos, D., Méndez-Arrieta, R., Méndez-Arrieta, A., Seisdedos-de-Vergara, R., Abarca, J., Barrio-Amorós, C. y González-Maya, J. (2018). Anuran inventory in a locality of the buffer area of La Amistad International Park, Costa Rica: pilot study for citizen science application. Anales de biología, (40), 57-64. https://www.um.es/analesdebiologia/numeros/40/PDF/40_2018_07.pdf
Hernández‐Ordóñez, O., Urbina‐Cardona, N. y Martínez‐Ramos, M. (2015). Recovery of amphibian and reptile assemblages during old‐field succession of tropical rain forests. Biotropica, 47(3), 377-388. https://onlinelibrary.wiley.com/doi/abs/10.1111/btp.12207
Heyer, W. R., Donnelly, M. A., McDiarmid, R. W., Hayek, L-A. C. y Foster, M. (Eds.). (1994). Measuring and monitoring biological diversity: standard methods for amphibians. Smithsonian Institution Press. https://pubs.er.usgs.gov/publication/5200175
Hidalgo, J., De León, J., González, C., Gibeaux, S., Batista, A., Samudio, M., ... y Vega, R. (2020). Informe de ejecución del proyecto: Sostenibilidad en el uso de recursos naturales y conservación de la biodiversidad de la región occidental de Panamá. DOI: 10.5281/zenodo.7629233
Huq, S. (2014). Andinobates geminisae. AmphibiaWeb: Información respecto a biología anfibia y conservación. https://es.mongabay.com/2015/01/nueva-rana-venenosa-de-dardo-necesita-un-plan-de-conservacion-inmediato/
Jaramillo, C., Wilson, L.D., Ibáñez, R., Jaramillo, F. (2010) The herpetofauna of Panama: distribution and conservation status. In: Wilson LD, Townsend JH, Johnson JD. (Eds) Conservation of Mesoamerican Amphibians and Reptiles.Eagle Mountain Publishing, LC, Eagle Mountain, Utah, 604–671
Leenders, T. (2017). Amphibians of Costa Rica: a field guide. Cornell University Press.
López-Gallego, C. y Morales M, P. (2020) Cavanillesia chicamochae. The IUCN Red List of Threatened Species 2020: e.T134501353A153330605. https://dx.doi.org/10.2305/IUCN.UK.2020-2.RLTS.T134501353A153330605.es
McCranie, J. R. (2006). Specimen locality data & museum numbers for "Guía de Campo de los anfibios de Honduras". Ubicación y números de museo de los especímenes, información complementaria a la "Guía de campo de los anfibios de Honduras". Smithsonian Herpetological Information Service. https://repository.si.edu/handle/10088/852
Medina-Rangel, G. F., Ruiz-Valderrama, D. H. y Thompson, M. E. (2019). Anfibios y reptiles. Colombia: Bajo Caguán-Caquetá. Universidad Nacional de Colombia. https://fieldguides.fieldmuseum.org/sites/default/files/rapid-color-guides-pdfs/1059_colombia_amphibians_and_reptiles_of_bajo_caguan-caqueta.pdf
Myers, C. W. y Daly, J. W. (1976). Preliminary evaluation of skin toxins and vocalizations in taxonomic and evolutionary studies of poison-dart frogs (Dendrobatidae). Bulletin of the AMNH, 157, 175-262. https://digitallibrary.amnh.org/handle/2246/622
Palacios-Rodriguez, L., y Rengifo-Mosquera, J., Roa Panesso, M. y Palacios Asprilla, Y. (2018). Riqueza y distribución de Hílidos (Hylidae: Anura) en zona de bosques pluvial tropical en el departamento del Chocó, Colombia. Revista colombiana de ciencia animal, 10(2), 154-166. http://www.scielo.org.co/pdf/recia/v10n2/2027-4297-recia-10-02-154.pdf
Quiroz-Espinosa, M., Miranda, M. y Batista, A. (2020). Plan de educación ambiental para los anfibios de Panamá. Los Naturalistas. http://www.unachi.ac.pa/assets/descargas/vip/Plan-de-Educacion-Ambiental-1324unachi2021.pdf
Savage, J. M. (2002). The amphibians and reptiles of Costa Rica: a herpetofauna between two continents, between two seas. University of Chicago Press.
Scott, N. J., Crump, M. L., Zimmerman, B. L., Jaeger, R. G., Inger, R. F., Corn, P. S., Woodward, B. D., Dodd, C. K., Scott, D. E., Shaffer, H. B., Alford, R. A., Richards, S. J., y Altig, R. (1994). Standard techniques for inventory and monitoring. En R. Heyer W. Measuring and monitoring biological diversity. Standard methods for amphibians. (74–141). Smithsonian Institution Press. https://repository.si.edu/handle/10088/19095
Sosa, Á. y Guerrel, J. (2013). Riqueza, diversidad y abundancia de anfibios en el bosque nuboso de Cerro Azul, sector Alto Chagres, Parque Nacional Chagres, Panamá. Tecnociencia, 15(1), 57-75. https://revistas.up.ac.pa/index.php/tecnociencia/article/view/1034
Stynoski, J. L. (2012). Behavioral ecology of parental care in a dendrobatid frog (Oophaga pumilio). University of Miami.
Székely, P., Székely, D., Armijos-Ojeda, D., Jara-Guerrero, A. y Cogălniceanu, D. (2016). Anfibios de un bosque seco tropical: Reserva Ecológica Arenillas, Ecuador. Ecosistemas, 25(2), 24-34. https://doi.org/10.7818/ECOS.2016.25-2.04
Toft, C. A. y Duellman, W. E. (1979). Anurans of the lower Rio Llullapichis, Amazonian Peru: a preliminary analysis of community structure. Herpetologica, 35(1), 71-77. https://www.academia.edu/364849/Anurans_of_the_Lower_Rio_Llullapichis_Amazonian_Peru_a_Preliminary_Analysis_of_Community_Structure
Vega, A., Gibeaux, S., Gónzalez, C. J., De León, J. y Hidalgo, J. (2020). Informe de ejecución del proyecto: Sostenibilidad en el uso de recursos naturales y conservación de la biodiversidad de la región occidental de Panamá. CENPEN. https://www.researchgate.net/publication/341656662_INFORME_DE_EJECUCION_DEL_PROYECTO_Sostenibilidad_en_el_Uso_los_Recursos_Naturales_y_Conservacion_de_la_Biodiversidad_de_la_Region_Occidental_de_Panama_CENPEN-18-012_PRIMERA_ETAPA_30_DE_MARZO_DE_2020

