



INTERACCIÓN DE PROROCENTRUM LIMA CON LAS MACROALGAS AGAROPHYTON CHILENSIS, ULVA SPP. Y CODIUM FRAGILE Y SU EFECTO EN LA ESTIMULACIÓN DEL EPIFITISMO
INTERACTION OF PROROCENTRUM LIMA WITH THE MACROALGAE AGAROPHYTON CHILENSIS, ULVA SPP. AND CODIUM FRAGILE AND ITS EFFECT ON THE STIMULATION OF EPIPHYTISM
Tecnociencia
Universidad de Panamá, Panamá
ISSN: 1609-8102
ISSN-e: 2415-0940
Periodicidad: Semestral
vol. 26, núm. 1, 2024
Recepción: 10 Julio 2023
Aprobación: 05 Octubre 2023

Resumen:
Prorocentrum lima ha presentado frecuentes estudios en el área acuícola, dentro del control de seguridad de moluscos bivalvos. Este dinoflagelado no ha sido cultivado a gran escala en un marco autotrófico con medios de cultivo inorgánicos. El presente estudio busca comprender su carácter epífito-bentónico y sus interacciones con algunas macroalgas para desarrollar nuevas tecnologías y cultivarlo a gran escala. La cepa de P. lima se aisló de Codium fragile, y en cultivo con medio inorgánico se obtuvo su máxima densidad celular (20 317 células mL-1) el día 24, con una tasa de crecimiento promedio de 0.0815 ± 0.2027 div día-1. En una simulación de cultivo de mesocosmos en condiciones ambientales naturales y controladas, P. lima epifitó a las macroalgas Agarophyton chilensis, Ulva spp. y C. fragile, además de todas las estructuras inertes presentes en los estanques de cultivo. Sin embargo, presentó la mayor densidad (80 053 células g-1FW) sobre A. chilensis, en condiciones controladas a los 13 días de cultivo. Las macroalgas estarían aportando nutrientes orgánicos específicos que estimularían el crecimiento de
P. lima.
Palabras clave: Prorocentrum lima, mesocosmos, macroalgas, nutrientes.
Abstract: Prorocentrum lima has presented frequent studies in the aquaculture area, within security control of bivalve mollusks. This dinoflagellate has not been cultivated on a large scale in an autotrophic framework with inorganic culture media. The present study seeks to understand its epiphyte-benthic character and its interactions with some macroalgae to develop new technologies and cultivate it on a large scale. The P. lima strain was isolated from Codium fragile, and in culture with inorganic medium its maximum cell density (20 317 cells mL-1) was obtained on day 24, with an average growth rate of 0.0815 ± 0.2027 div day-1. In a mesocosm culture simulation under natural and controlled environmental conditions, P. lima epiphyted the macroalgae Agarophyton chilensis, Ulva spp. and C. fragile, in addition to all the inert structures present in the culture ponds. However, it presented the highest density (80 053 cells g-1 FW) on A. chilensis, under controlled conditions at 13 days of culture. The macroalgae would be providing specific organic nutrients that would stimulate the growth of P. lima.
Keywords: Prorocentrum lima, mesocosmos, macroalgae, nutrient.
INTRODUCCIÓN
Se han registrado floraciones algales nocivas (FAN) de dinoflagelados epífitos- bentónicos en todos los océanos, especialmente en aguas tropicales y subtropicales asociadas a la presencia de especies correspondientes a los géneros Gambierdiscus, Ostreopsis, Prorocentrum, Coolia y Amphidinium (Aligizaki & Nikolaidis, 2006; Alikasi & Nikolaidis, 2008; David et al., 2018; Faust, 1991; Fukuyo, 1981; Fukuyo, 1995; Karafas et al., 2015; Laza-Martinez et al., 2011; Lewis et al., 2018; Mangialajo et al., 2011; Nagahama et al, 2011;Penna et al., 2005;Tawong et al., 2014). Algunas especies de Prorocentrum, que son asociadas a la síntesis de ácido okadaico (AO) y sus Dinophysistoxinas derivadas (DTXs) (Koike et al., 1998; Foden et al., 2005; Murakami et al., 1982 ; Nascimento et al., 2005; Paz et al., 2006), a menudo constituyen una parte importante de esta comunidad de microalgas (Carlson & Tindall, 1985).
Los programas de vigilancia para el registro de estos dinoflagelados epibentónicos tóxicos son altamente complejos y requieren un procedimiento de obtención de muestras diferente al de los organismos planctónicos causantes de las FAN (Berdalet et al., 2016; GEOHAB, 2012; . El método más utilizado consiste en la recolección de sustratos naturales, para luego separar y cuantificar la comunidad epibentónica presente (Litaker et al., 2010) obteniendo un gran número de muestras (Lobel et al., 1988), lo que dificulta su análisis (Tester et al., 2014).
Los dinoflagelados bentónicos pueden variar en composición y abundancia de células, lo cual depende de variables ambientales como la temperatura, salinidad, luz y nutrientes (Arbeláez et al., 2020 ; Bomber et al.,1988; Carlson & Tindall, 1985; Chinain et al., 1999;Hales et al., 1999; Kibler et al., 2015; Lartigue et al., 2009; Okolodrov et al., 2014; Pearce et al., 2001). Además su ocurrencia y abundancia depende de los sustratos, que pueden estar constituidos por diferentes especies de macroalgas, pastos marinos y corales (Fukuyo, 1981; Irola-Sansores et al., 2018; Lobel et al., 1988; Nakahara et al., 1996;Parsons & Preskitt, 2007;Parsons et al., 2011).
Actualmente, existe poco conocimiento sobre la relación de los dinoflagelados epífitos y los productos extracelulares liberados o exudados por las macroalgas, que pueden incrementar o inhibir su crecimiento (Bomber et al., 1989; Carlson et al., 1984;Rains & Parsons, 2015). Estos compuestos serían utilizados por los dinoflagelados en estrategias nutricionales como la mixotrofía y la heterotrofia, adquiriéndolos no sólo de las aguas circundantes, sino también de los sedimentos o de las superficies sobre las que viven (Litaker et al., 2010).
Algunas especies de dinoflagelados, como P. lima (Ehrenberg) F. Stein 1878, son especies epibentónicas que se extienden a aguas templadas no subtropicales (Lassus et al., 2016), tal aguas costeras del centro norte de Chile (Uribe et al., 2018). Durante las últimas décadas, esta especie han sido ampliamente estudiada por su capacidad para producir toxinas diarreicas, incluidas AO, DTX y otros análogos (Marr et al., 1992; Torgensen et al., 2008;Uchida et al., 2014; Lee et al., 2015; Hu et al., 2017; Yang et al., 2017;Wu et al., 2020), aunque la toxicidad de algunos aún es incierta (Hu et al., 2010).
Hasta la fecha, el cultivo masivo de P. lima se ha explorado con poco éxito con el uso de medios de cultivo inorgánicos (Bravo et al., 2001; Foden et al., 2005; Heredia-Tapia, 2005; Hou et al., 2015; Nascimento et al., 2016; Nascimento et al., 2005; Praptiwi, 2014;Vale et al., 2009; Vanucci et al., 2010; Varkitzi et al., 2010; Varkitzi et al., 2017;
Gu et al., 2019; Tarazona, 2019; Wang et al., 2015; Wu et al., 2020), enfocado principalmente al estudio de metabolitos tóxicos en laboratorio (Hu et al., 1992; Murakami et al., 1982). Además, se han utilizado dos sistemas para la producción de biomasa de P. lima, el cultivo semicontinuo (Varkitzi et al., 2017) y los fotobiorreactores (Wang et al., 2015), ambos casos están restringidos a condiciones autotróficas.
En el norte de Chile, se registra por primera vez un pequeño florecimiento de P. lima en Bahía Calderilla, que es una bahía semicerrada de aguas poco profundas, ubicada aproximadamente 5 km al norte de Bahía Inglesa, donde el cultivo industrial de vieiras (Argopecten purpuratus) mediante acuicultura, se lleva a cabo. Durante este florecimiento se encontraron células distribuidas en la columna de agua, arena, rocas y macroalgas (C. fragile, A. chilensis y Ulva spp.) del entorno (Uribe et al., 2018). Con
P. lima se brinda la oportunidad de realizar un estudio para entender la interacción residente-huésped. Por lo tanto, se utilizan sustratos vivos (macroalgas) dentro de un sistema de cultivo de mesocosmos en un ambiente controlado y natural, con el propósito de conocer si los sustratos brindan estimulación o inhibición al crecimiento de P. lima.
MATERIALES Y MÉTODOS
Colecta, aislamiento y cultivo de cepas de P. lima
Las muestras biológicas fueron recolectadas en diciembre de 2017 en el sector costero de Bahía Calderilla, Región de Atacama, Chile (27º5’16.25” S y 70º51’21.07” O). Estas muestras tomadas entre 0.2 a
0.4 m de profundidad estuvieron conformadas por las macroalgas dominantes
Agarophyton chilensis, Ulva spp. y Codium fragile.
De cada una de ellas se tomaron seis muestras de 300 g, las cuales se pusieron en una bolsa plástica con 500 mL de agua de mar. Posteriormente, se almacenaron en una caja térmica y se trasladaron al Laboratorio de Producción Primaria y Fitoplancton de la Universidad Católica del Norte para su análisis.
En el laboratorio, las muestras fueron agitadas vigorosamente para desprender los epifitos. Posteriormente, el agua fue filtrada utilizando un filtro de 20 µm, para concentrar las microalgas y retener el perifiton. Cada célula microalgal fue observada utilizando un microscopio fotónico invertido Olympus CKX41 en búsqueda del dinoflagelado P. lima.
Una vez identificado y con el propósito de establecer cultivos clonales, células de P. lima fueron aisladas utilizando la técnica de micropipeteo y lavado consecutivo (Stein, 1973).
Los cultivos fueron desarrollados en placas de cultivo celular estériles de 24 pocillos, por lo que cada célula aislada fue depositada individualmente en un pocillo de 2 mL con 1 mL de medio de cultivo L1 sin silicato (L1-Si) (Guillard & Hargraves, 1993). Cada placa de cultivo se incubó en ambiente controlado a una temperatura de 20 °C, bajo una irradiación de 80 µmol de fotones m-2s-1 y con un fotoperiodo de 12 h: 12 h (luz/oscuridad).
Luego de 60 días, cuando el cultivo alcanzó una densidad aproximada de 1 000 células mL-1 se inoculó por triplicado 30 mL en matraces de vidrio de 250 mL con 100 mL del medio (L1-Si) con densidades celulares entre 500 y 1 000 células mL-1, y se cultivaron en ambiente controlado con las condiciones previamente señaladas, luego se determinó el crecimiento poblacional de los cultivos registrando las densidades celulares cada tres días con una cámara de recuento celular Sedgwick-Rafter y expresando los resultados en células mL-1, siguiendo la metodología establecida por LeGresley & McDermott, 2010.
También de cada cultivo se estimaron las tasas de crecimiento diario experimentales (día-1), según el protocolo señalado por Levasseur et al., (1993).
Adicionalmente, con los valores de las densidades celulares experimentales se estimaron las tasas de crecimiento máximas y las concentraciones celulares máximas, mediante un modelo matemático de crecimiento exponencial con saturación, a partir de la observación inicial (día 0), para estandarizar las tasas de crecimiento y las respectivas curvas de crecimiento de la cepa.
El modelado numérico de los datos de crecimiento se realizó con el método de mínimos cuadrados no lineales del macro "Solver" de la hoja de cálculo de Microsoft Excel y el error asociado a las estimaciones de los parámetros (como intervalos de confianza) se calculó y evaluó mediante la prueba t de Student y se determinó la curva de crecimiento.
Preparación de mesocosmos marino
Se prepararon dos estanques cilíndricos de fibra de vidrio transparente con capacidad de 500 L. El estanque Nº 1 para realizar un cultivo mesocosmos en ambiente natural y el Nº 2 para un cultivo en ambiente controlado.
A ambos estanques, se les agregó arena limpia de playa, cuatro rocas pequeñas, lisas, planas y limpias de la zona intermareal. Además, se agregaron 400 gramos de cada macroalga (A. chilensis, Ulva spp. y C. fragile), ancladas en la arena. Finalmente, se agregaron 100 L de agua de mar microfiltrada (1 µm) sin nutrientes y se les suministró aire a través de mangueras transparentes y piedras difusoras.
Posteriormente, cada estanque fue inoculado con dos litros de cultivo de la cepa de P. lima, alcanzando una densidad de 880 células mL-1 para el estanque Nº 1 y 651 células mL-1 para el estanque Nº 2. El estanque Nº 1 fue ubicado en un patio de luz exterior con un fotoperiodo estival, donde la irradiancia (µmol fotones m-2s-1) fue registrada cada hora durante 19 días, con un sensor LiCor Li200X y la temperatura del agua (ºC), diariamente y cada dos horas durante el día, con un termómetro electrónico Checktemp 1 Hanna. El estanque Nº 2 se ubicó en un laboratorio de ambiente controlado a 16 ºC, con un fotoperiodo de 12 h: 12 h (luz/oscuridad) y con una intensidad de irradiación (Io) de 80 µmol fotones m-2s-1, para los 19 días.
En ambos estanques, cada tres días se recolectaron muestras de 20 g de las tres macroalgas por triplicado. Estas muestras fueron colocadas en bolsas plásticas con 100 mL de agua de mar microfiltrada (0.45 µm) y se agitaron vigorosamente durante tres minutos para separar las células de P. lima de la superficie de las algas. Este procedimiento se repitió tres veces con el propósito de asegurar el completo desprendimiento de las células. Posteriormente, se determinó la densidad celular usando una cámara de recuento Sedgwick-Rafter. Para expresar la cantidad de células g-1 respecto al peso húmedo (Pm) de cada macroalga, se usó el procedimiento descrito por Reguera et al., (2011).
Los valores obtenidos fueron empleados para generar las curvas de crecimiento en el programa Excel, comparando las densidades celulares obtenidas sobre las tres especies macroalgales. Los resultados experimentales se analizaron estadísticamente con un análisis de varianza unidireccional ANOVA y realizando la prueba post-hoc de Fisher, para evaluar la variabilidad del máximo número de células de P. lima en ambos mesocosmos y entre las mismas macroalgas en los dos estanques. Todos los análisis se desarrollaron utilizando el programa estadístico Statistic 7 (V.7).
RESULTADOS
Colecta, aislamiento y cultivo de cepas de P. lima
De las tres especies de macroalgas muestreadas, sólo en C. fragile se encontraron
células del dinoflagelado P. lima. Al cultivarla, esta cepa creció rápidamente, alcanzando la densidad celular máxima experimental de 20 317 ± 1 377 células mL-1 el día 24, mientras que la densidad celular máxima teórica fue de 19 422 ± 382 células mL-1 (R2 > 0.9723). Posteriormente la densidad empezó a disminuir, llegando a los valores (18 117 ± 2 153 células mL-1) el día 39 (Figura 1).
Esta cepa obtuvo una tasa de duplicación experimental de 0.2115 ± 0.2975 día-1 hasta los 15 días de cultivo. Además, su tasa de crecimiento máxima teórica fue de 0.1544 ± 0.0253 día-1.
Mesocosmos marino
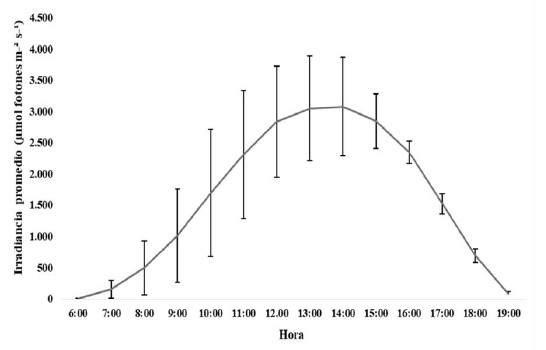
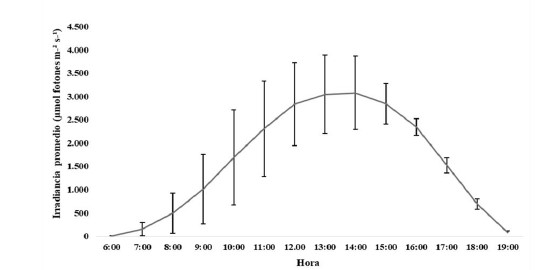
El mesocosmos en el patio de luz exterior (ambiente estival) recibió una irradiancia de entre 31 - 420 µmol fotones m-2 s-1 a las 7:00 horas, alcanzando la irradiación más alta a las 14:00 horas con 1 508 – 3 638 µmol fotones m-2s-1, mientras que a las 19:00 horas se obtuvo entre 27 y 741 µmol de fotones m-2 s-1 (Figura 2), observándose mayor estabilidad en la irradiación después de las 16:00 horas.
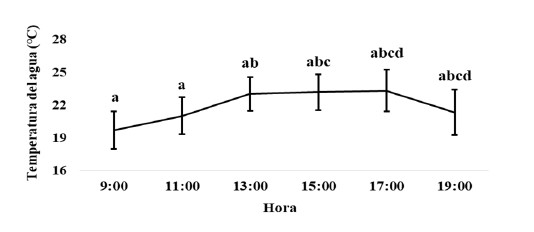
El registro de la temperatura del agua del estanque en los 19 días del estudio presentó durante el día una temperatura promedio diaria de 21.9 ± 1.4 °C, estabilizándose entre las 13 y 17 horas con variaciones promedio entre 23.0 y 23.3 °C (Figura 3.). Esta temperatura estuvo por debajo de 21.3 ± 2.0 °C en las noches y luego del amanecer volvía a aumentar. El máximo promedio obtenido fue de 23.5 ± 0.7 °C, mientras que el mínimo fue de 19.8 ± 1.3 °C.
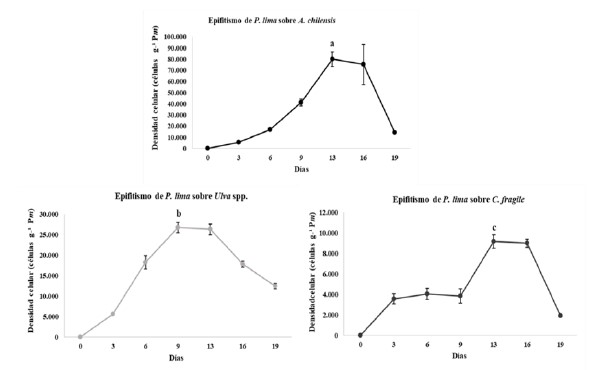
En este estanque con ambiente estival la mayor densidad celular de P. lima correspondiente a 30 267 ± 2 203 células g-1 Pm (peso húmedo) se registró el día 16 sobre A. chilensis. Las máximas densidades sobre A. chilensis durante el estudio fueron significativamente mayores a las de las otras dos macroalgas (p < 0.05). Sobre C. fragile la máxima densidad celular correspondiente a 17 700 ± 2 100 células g-1 Pm fue registrada a los 13 días, mientras que en Ulva spp., fue de 15 733 ± 7 943 células g-1 Pm en el mismo periodo de tiempo (Figura 4; Tabla 1). A partir de los 13 días empezaron a disminuir las densidades celulares sobre Ulva spp. y C. fragile, mientras que sobre A. chilensis ocurrió desde el día 16. Sobre todas las macroalgas hubo un perfil de epifitación errático durante todas las curvas, pero en Ulva spp. y C. fragile se observó de manera más pronunciada al final de sus curvas de crecimiento.
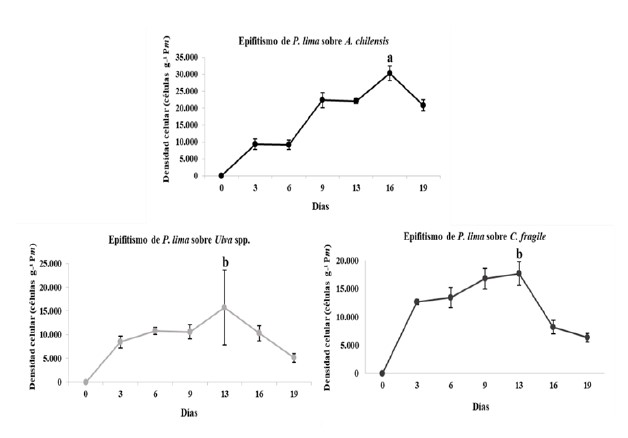
![Máximas densidades celulares de P. lima [células g-1 Pm (peso húmedo)] epifitando a
A. chilensis, C. fragile y Ulva spp., dentro del mesocosmos bajo condiciones naturales (temporada estival) y condicionales controladas de laboratorio. Las
letras diferentes indican diferencias entre las máximas densidades celulares sobre las otras macroalgas (p < 0,05)](../2244880004_gt2.png)
En el mesocosmos en ambiente controlado, el día 13 se registró una alta densidad celular de P. lima correspondiente a 80 053 ± 6 617 células g-1 Pm epifitando a A. chilensis. En Ulva spp. se cuantificaron 26 760 ± 1 224 células g-1 Pm en el día 9, mientras que en C. fragile se registraron 9 165 ± 665 células g-1 Pm también el día 13 del estudio. Las densidades celulares empezaron a disminuir desde el día 13 sobre todos los sustratos macroalgales. Después del tercer día de la prueba, C fragile tuvo un perfil de epifitación muy errático en su curva de crecimiento.
Los datos estadísticos mostraron diferencias significativas (p < 0.05), entre las máximas densidades sobre las tres macroalgas durante el estudio (Figura 5; Tabla 1), obteniendo A. chilensis la mayor epifitación de P. lima, y C. fragile, la menor.
Las máximas densidades celulares de P. lima obtenidas sobre C. fragile durante todo el estudio presentaron diferencias (p < 0.05) entre sí, entre ambos mesocosmos, obteniéndose las mayores densidades celulares en el estanque en ambiente estival. De igual forma ocurrió entre las máximas densidades celulares obtenidas sobre A. chilensis, aunque las mayores densidades celulares se obtuvieron en el estanque en ambiente controlado. Sobre Ulva spp. también se obtuvo diferencias (p < 0.05) entre las mayores densidades celulares entre ambos estanques, pero en el estanque en ambiente controlado se reportó mayor densidad (Tabla 1).
DISCUSIÓN
Colecta, aislamiento y cultivo de cepas de P. lima
En diciembre de 2017, durante una floración detectada en el sector costero de Bahía Calderilla, en el Norte de Chile, se encontró la cepa D008-2 de P. lima epifitando a la macroalga C. fragile. Este evento fue similar al reportado por Uribe et al., (2018) en
ese mismo lugar, quienes en febrero de 2016 encontraron a P. lima sobre la superficie de diferentes macroalgas como C. fragile, A. chilensis y Ulva spp. Estos resultados señalan la selectividad de este dinoflagelado sobre varios sustratos macroalgales, y aunque en el presente estudio se encontró sólo sobre C. fragile, estas células pueden ser halladas en otras macroalgas que sean similares en su preferencia (Tester et al., 2014).
La capacidad de P. lima de crecer sobre estos sustratos vivos ha sido descrita por Parsons & Preskitt, (2007);Tester et al., (2014); Nishimura et al., (2020), asociados a macroalgas como Ulva, Gracilaria, Enteromorpha flexuosa y Gelidium pusillum. Del mismo modo, otros dinoflagelados bentónicos pueden coexistir con macroalgas, como ha sido reportado por Bomber & Aikman, (1989), Faust, (1991) o Moreira-González et al., (2018), quienes señalan que diversos dinoflagelados como Amphidinium, Gambierdiscus, Coolia, Ostreopsis y Prorocentrum habitan comúnmente en macroalgas como Ulva, Heterosiphonia y Codium en diversos hábitats marinos costeros, aunque también puede habitar sobre sustratos inertes y/o epifitando moluscos bivalvos.
Los valores de las mayores densidades celulares de P. lima al ser cultivada (20 317 ± 1 377 células mL-1), fueron similares a los reportados por Wang et al., (2015) (16 000
– 25 000 células mL-1) y a los de Varkitzi et al., (2017) (20 690 células mL-1). No obstante, fueron superiores a los reportados por Bravo et al., (2001) (7 000 – 15 000 células mL-1) y a los de Aquino-Cruz et al, (2018) (600 – 11 500 células mL-1) en similares condiciones de cultivo, lo cual demuestra que este dinoflagelado suele desarrollar variabilidades en su crecimiento (Bravo et al., 2001). Por otra parte, la extensa fase estacionaria de 24 días obtenida, es señalada como muy característica de esta especie bentónica, ya que Nascimento et al., (2005) registraron un tiempo similar de 20 días, con una fase exponencial de 25 días y una densidad celular máxima de
48.300 células mL-1.
Mesocosmos marino
En el mesocosmos en ambiente natural, que registró altas variaciones en las irradiaciones (0 a 3 000 µmol fotones m-2s-1) y temperatura del agua (18.3 a 25.0ºC), obtuvo un crecimiento limitado de P. lima en las tres macroalgas (A. chilensis, Ulva spp y C. fragile), no superando las 31 000 células g-1 Pm. En cambio, en el estanque con ambiente controlado la irradiación (80 µmol fotones m-2s-1) y la temperatura (16 ± 1 ºC), se mantuvieron constantes durante todo el estudio, permitiendo un mayor epifitismo de 26 760 y 80 053 células g-1 Pm sobre Ulva spp. y A. chilensis, respectivamente.
La estabilidad ambiental en el estanque con condiciones controladas fue favorable para el crecimiento de esta especie epífita. El desarrollo de esta especie de dinoflagelado en similares condiciones ha sido reportado por David et al., (2018), quienes al cultivar en matraces con 50 mL de f/2 a irradiaciones de 80 y 100 µmol fotones m-2s-1, lograron una alta tasa de crecimiento (0.23 día-1) en su cepa de P. lima. La alta irradiación que recibe el cultivo en mesocosmos en ambiente natural a medio día, pudo fotoinhibir el aparato fotosintético de estas células, reduciendo las densidades celulares de P. lima, al no estar aclimatadas a la alta irradiación (David et al., 2018; López-Rosales et al., 2013; Praptiwi, 2014).
Por otra parte, P. lima logró desarrollarse entre los 16 a 25 ºC de temperatura, sugiriendo una amplia tolerancia térmica de este dinoflagelado. En efecto, estas cepas en condiciones naturales han sido reportadas en áreas tropicales y subtropicales con temperaturas entre 19 y 33 ºC (Aligizaki et al., 2009; Nagahama et al., 2011), 21 ºC en este estudio, e incluso en regiones templadas o frías creciendo con temperaturas entre 5 y 25 ºC (Morton et al., 1992). Estos resultados son también consistentes con las observaciones en laboratorio hechas por (Aquino-Cruz et al., 2018; López-Rosales et al., 2013;McLachlan et al., 1994; Varkitzi et al., 2017), quienes desarrollaron cultivos de esta especie y lograron crecimientos a temperaturas entre 20 y 30 ºC. Del mismo modo, (Aquino-Cruz et al., 2018; McLachlan et al., 1994), demostraron que P. lima puede ser cultivada a temperaturas más bajas (15 ºC), similar al cultivo desarrollado en ambiente controlado para la cepa (D008-2). Estos resultados indican que, para conseguir una alta densidad celular de esta especie, se debe cultivar bajo condiciones ambientales controladas, eligiendo las variables ambientales de acuerdo con el origen de la cepa a cultivar.
Sin embargo, también hay que considerar el sustrato para esta especie epifita, ya que el mesocosmos en ambiente natural, como en ambiente controlado presentó una preferencia al epifitismo sobre A. chilensis, seguido de Ulva spp. y finalmente en C. fragile.
En general, algunas investigaciones señalan que las relaciones simbióticas entre P. lima con macroalgas rodófitas en ambiente natural suelen ser comunes, reportando su interacción con Acanthophora spicifera (Morton & Faust, 1997), Gelidiella spp., Gelidiopsis variabilis, G. salicornia (Parsons & Preskitt, 2007), Gracilaria gracilis (Hachani et al., 2018), Amphiroa spp. (Irola-Sansores et al., 2018), Gracilariopsis spp. y Gracilaria spp. (Catuto-Magallan, 2019) y Laurencia spp. (Tarazona-Janampa et al., 2020), entre otras. Bravo et al., (2020) también reportaron la preferencia de
Prorocentrum spp. en diferentes macroalgas ramificadas como las rodofíceas Spyridea, Lophocladia y Asparagopsis, y en la feófita Halopteris, observándose que las arquitecturas filamentosas y enredadas de estos talos, tienen una influencia en la abundancia de estos dinoflagelados. En el presente estudio ocurrió de manera similar con la estructura filamentosa y ramificada de A. chilensis.
Las rodófitas como A. chilensis, se caracterizan por tener polisacáridos estructurales conformados por agarosa, galactosa o ácido pirúvico (Matsuhiro & Urzúa 1990; Chandia, 2020). En este contexto, es posible que P. lima en su condición de mixótrofo (Faust, 1998) tenga la capacidad de nutrirse de estos azúcares mediante una simple difusión, desdoblándolos a través de una rápida acción enzimática o utilizándolos como moléculas más pequeñas producidas por la acción enzimática bacteriana, incrementando su densidad celular.
El epifitismo de P. lima sobre A. chilensis tanto en ambiente natural, como controlado fue mayor que en Ulva spp. y C. fragile. Estas dos últimas macroalgas sintetizan polisacáridos altamente sulfatados que poseen un amplio espectro de actividad biológica, incluyendo la actividad antiproliferativa (Wang et al., 2014; Aumeerun et al., 2019) e inhibición de crecimiento, combatiendo a microalgas marinas como Rhodosorus magnei, Neorhodella cyanea y Prymnesium calathiferum (Águila- Ramírez et al., 2012), por lo que esta actividad biológica pudo influir en la proliferación de P. lima sobre Ulva spp. y C. fragile.
CONCLUSIONES
Del perifiton obtenido, P. lima fue aislado únicamente en C. fragile, aunque puede ser encontrado en otras macroalgas. Este dinoflagelado suele desarrollar amplia tolerancia a diferentes irradiaciones y temperaturas, facilitando su proliferación sobre diversos hábitats. Al cultivarse en los mesocosmos, tanto en ambiente natural como controlado, epifitó a todas las macroalgas, pero presentando una mayor afinidad con A. chilensis. Además, también logró crecer sobre todas las estructuras inertes presentes en ambos estanques. El crecimiento de este dinoflagelado en un sistema de cultivo sin adición de nutrientes podría indicar que se estaría alimentando de los componentes liberados por los sustratos macroalgales.
CONFLICTOS DE INTERÉS
Los autores declaran no tener conflicto de intereses.
REFERENCIAS
Águila-Ramírez, R., Arenas-González, A., Hernández-Guerrero, C., González-Acosta, B., Borges-Souza, J., Véron, B., & Hellio, C. (2012). Antimicrobial and antifouling activities achieved by extracts of seaweeds from Gulf of California, Mexico. Hidrobiologica, 22(1), 8–15.
Aligizaki, K., & Nikolaidis, G. (2006). The presence of the potentially toxic genera Ostreopsis and Coolia (Dinophyceae) in the North Aegean Sea, Greece. Harmful Algae, 5(6), 717–730 https://doi.org/10.1016/j.hal.2006.02.005
Aligizaki, K., & Nikolaidis, G. (2008). Morphological identification of two tropical dinoflagellates of the genera Gambierdiscus and Sinophysis in the Mediterranean Sea. Journal of Biological Research, 9, 75–82.
Aligizaki, K., Nikolaidis, G., Katikou, P., Baxevanis, A., & Abatzopoulos, T. (2009). Potentially toxic epiphytic Prorocentrum (Dinophyceae) species in Greek coastal waters. Harmful Algae, 8(2), 299– 311.https://doi.org/10.1016/j.hal.2008.07.002
Aquino-Cruz, A., Purdie, D., & Morris, S. (2018). Effect of increasing sea water temperature on the growth and toxin production of the benthic dinoflagellate Prorocentrum lima. Hydrobiologia, 813(1), 103–122. https://doi.org/10.1007/s10750-018-3512-4
Arbeláez, N., Mancera-Pineda, J., & Reguera, B. (2020). Structural variation of potentially toxic epiphytic dinoflagellates on Thalassia testudinum from two coastal systems of Colombian Caribbean. Harmful Algae, 92(January), 101738. https://doi.org/10.1016/j.hal.2019.101738
Aumeerun, S., Soulange-Govinden, J., Driver, M., Rao, A., Ravishankar, G., & Neetoo, H. (2019). Macroalgae and Microalgae. In Handbook of Algal Technologies and Phytochemicals (p. 207).
Berdalet, E., Fleming, L., Gowen, R., Davidson, K., Hess, P., Backer, L., Moore, S., Hoagland, P. & Enevoldsen, H. (2016). Marine harmful algal blooms, human health and wellbeing: challenges and opportunities in the 21st century. Journal of the Marine Biological Association of the United Kingdom, 96(1), 61–91. https://doi.org/https//: 10.1017/ S00253 15415001733
Bomber, J., & Aikman, K. (1989). The Ciguatera Dinoflagellates. Biological Oceanography, 6, 291–311.
Bomber, J., Guillard, R., & Nelson, W. (1988). Roles of temperature, salinity, and light in seasonality, growth, and toxicity of ciguatera-causing Gambierdiscus toxicus Adachi et Fukuyo (Dinophyceae). J. Exp. Mar. Biol. Ecol., 115, 53–65.
Bomber, J., Rubio, M., & Norris, D. (1989). Epiphytism of dinoflagellates associated with the disease ciguatera: substrate specificity and nutrition. Phycologia, 28(3), 360–368. https://doi.org/10.2216/i0031-8884-28-3-360.1
Bravo, I., Fernández, M. L., Ramilo, I., & Martínez, A. (2001). Toxin composition of the toxic dinoflagellate Prorocentrum lima isolated from different locations along the Galician coast (NW Spain). Toxicon, 39(10), 1537–1545. https://doi.org/10.1016/S0041-0101(01)00126-X
Bravo, I., Rodríguez, F., Ramilo, I., & Afonso-Carrillo, J. (2020). Epibenthic Harmful Marine Dinoflagellates from Fuerteventura (Canary Islands), with Special Reference to the Ciguatoxin-Producing Gambierdiscus. J. Mar. Sci. Eng., 8, 0909.
Carlson, R., Morey-Gaines, G., Tindall, D., & Dickey, R. (1984). Ecology of Toxic Dinoflagellates from the Caribbean Sea Effects of Macroalgal Extracts on Growth in Culture. Sea Food Toxins, 24, 271– 287.https://doi.org/doi:10.1021/bk-1984-0262.ch024
Catuto-Magallan, R. (2019). Composición y abundancia de dinoflagelados epibentónicos asociados a macroalgas en dos playas de la Provincia de Santa Elena. Universidad Estatal Península de Santa Elena.
Chandia, P. (2020). Valor agregado a macroalgas chilenas de exportación: caracterización de ficocoloides, denominación de origen y diversificación comercial. Proyecto BBPP 18BPE-93853.
Chinain, M., Germain, M., Deparis, X., Pauillac, S., & Legrand, A. (1999). Seasonal abundance and toxicity of the dinoflagellate Gambierdiscus spp. (Dinophyceae), the causative agent of ciguatera in Tahiti, French Polynesia. Marine Biology, 135, 259–267. https://doi.org/doi: 10.1007/s002270050623
David, H., Laza-Martínez, A., Kromkamp, J. C., & Orive, E. (2018). Physiological response of Prorocentrum lima (Dinophyceae) to varying light intensities. FEMS Microbiology Ecology, 94(1), 1–12. https://doi.org/10.1093/femsec/fix166
Faust, M. (1995). Observation of sand-dwelling toxic dinoflagellates (Dinophyceae) from widely differing sites, incluiding two new species. Journal Phycol., 42, 154–159.
Faust, M. A. (1998). Mixotrophy in tropical benthic dinoflagellates. In: Reguera, B., Blanco, J. Fernandez, L., Wyatt, T. (Eds.) Harmful Algae. Xunta de Galicia and Intergovernmental Oceanographic Commission of UNESCO, Paris, Pp 390- 393.
Faust, M., & Gulledge, R. (2004). Identifying Harmful Marine Dinoflagellates. Journal of Applied Phycology, 16(1), 79. https://doi.org/10.1023/b:japh.0000019147.40273.1b
Faust, M. A. (1991). Morphology of Ciguatera-causing Prorocentrum lima (Pyrrophyta) from widely differing sites. J. Phycol., 27, 642–648.
Foden, J., Purdie, D., Morris, S., & Nascimento, S. (2005). Epiphytic abundance and toxicity of Prorocentrum lima populations in the Fleet Lagoon, UK. Harmful Algae, 4, 1063–1074. https://doi.org/https//:10.1016/j.hal.2005.03.004
Fukuyo, Y. (1981). Taxonomical Study on Benthic Dinoflagellates Collected in Coral Reefs. Bulletin of the Japanese Society of Scientific Fisheries, 47(8), 967–978.
GEOHAB. (2012). Global Ecology and Oceanography of Harmful Algal Blooms, GEOHAB Core Research Project: HABs in Benthic Systems. In A. Berdalet, E., Tester, P., Zingone (Ed.), Organization. IOC of UNESCO and SCOR, Paris and Newark.
Gu, S., Xiao, S., Zheng, J., Li, H., Liu, J., & Yang, W. (2019). ABC Transporters in Prorocentrum lima and Their Expression Under Different Environmental Conditions Including Okadaic Acid Production. Marine Drugs, 17(259), 1–16.
Guillard, R. R. L., & Hargraves, P. E. (1993). Stichochrysis immobilis is a diatom, not a chrysophyte. Phycologia, 32(3), 234–236. https://doi.org/10.2216/i0031- 8884-32-3-234.1
Hachani, M. A., Dhib, A., Fathalli, A., Ziadi, B., Turki, S., & Aleya, L. (2018). Harmful epiphytic dinoflagellate assemblages on macrophytes in the Gulf of Tunis. Harmful Algae, 77(June), 29–42. https://doi.org/10.1016/j.hal.2018.06.006
Hales, S., Weinstein, P., & Woodward, A. (1999). Ciguatera (Fish Poisoning), El Niño, and Pacific Sea Surface Temperatures. Ecosystem Health, 5, 20–25. https://doi.org/doi: 10.1046/j.1526-0992. 1999. 0990 3.x
Heredia-Tapia, A., Arredondo-Vega, B., Nuñez-Vázquez, E., Yasumoto, T., Yasuda, M., & Ochoa, J. (2002). Isolation of Prorocentrum lima (Syn. Exuviella lima) and diarrhetic shellfish poisoning (DSP) risk assessment in the Gulf of California, Mexico. Toxicon 4, 40, 1121–1127.
Hou, D., Liang, J., Zou, C., Li, H., Liu, J., & Yang, W. (2015). MRP functional activity and character in the dinoflagellate Prorocentrum lima. Journal of Applied Phycology, 28, 1667–1676. https://doi.org/https//:10.1007/s10811-015-0679-1
Hu, Tingmo, LeBlanc, P., Burton, I. W., Walter, J. A., McCarron, P., Melanson, J. E., Strangman, W., & Wright, J. L. C. (2017). Sulfated diesters of okadaic acid and DTX-1: Self-protective precursors of diarrhetic shellfish poisoning (DSP) toxins. Harmful Algae, 63, 85–93. https://doi.org/10.1016/j.hal.2017.01.012
Hu, W., Xu, J., Sinkkonen, J., & Wu, J. (2010). Polyketides from Marine Dinoflagellates of the Genus Prorocentrum, Biosynthetic Origin and Bioactivity of Their Okadaic Acid Analogues. Mini-Reviews in Medicinal Chemistry, 10, 51–61. https://doi.org/10.2174/138955710791112541
Irola-Sansores, E. D., Delgado-Pech, B., García-Mendoza, E., Núñez-Vázquez, E. J., Olivos-Ortiz, A., & Almazán-Becerril, A. (2018). Population dynamics of benthic-epiphytic dinoflagellates on two macroalgae from coral reef systems of the northern Mexican Caribbean. Frontiers in Marine Science, 5, 1–14. https://doi.org/10.3389/fmars.2018.00487
Karafas, S., York, R., & Tomas, C. (2015). Morphological and genetic analysis of the Coolia monotis species complex with the introduction of two new species, Coolia santacroce sp. nov. and Coolia palmyrensis sp. nov. (Dinophyceae). Harmful Algae, 46, 18–33. https://doi.org/10.1016/j.hal.2015.05.002
Kibler, S. R., Tester, P. A., Kunkel, K. E., Moore, S. K., & Litaker, R. W. (2015). Effects of ocean warming on growth and distribution of dinoflagellates associated with ciguatera fish poisoning in the Caribbean. Ecological Modelling, 316, 194–210. https://doi.org/10.1016/j.ecolmodel.2015.08.020
Lartigue, J., Jester, E. L. E., Dickey, R. W., & Villareal, T. A. (2009). Nitrogen source effects on the growth and toxicity of two strains of the ciguatera-causing dinoflagellate Gambierdiscus toxicus. Harmful Algae, 8, 781–791. https://doi.org/10.1016/j.hal.2008.05.006
Lassus, P., Chomerat, N., Hess, P., & Nezan, E. (2016). Microalgues toxiques et nuisibles de l’océan mondial. COI Manuels et Guides, 68 / Toxic and Harmful Microalgae of the World Ocean. IOC Manuals and Guides, 68.
Laza-Martinez, A., Orive, E., & Miguel, I. (2011). Morphological and genetic characterization of benthic dinoflagellates of the genera Coolia, Ostreopsis and Prorocentrum from the south-eastern Bay of Biscay. European Journal of Phycology, 46(1), 45–65. https://doi.org/10.1080/09670262.2010.550387
Lee, S., Hwang, B., Kim, H., Yih, W., & Jeong, E. (2015). A New Diol Ester Derivative of Dinophysistoxin-1 from Cultures of Prorocentrum lima Collected in South Korea. Bulletin of the Korean Chemical Society, 395–398. https://doi.org/10.1002/bkcs.10031
LeGresley, M., & McDermott, G. (2010). Counting chamber methods for quantitative phytoplankton analysis - haemocytometer, Palmer-Maloney cell and Sedgewick-Rafter cell. In Microscopic and molecular methods for Quantitative phytoplankton analysis, 25–30.
Levasseur, M., Thompson, P., & Harrison, P. (1993). Physiological acclimation of marine phytoplankton to different nitrogen sources. J. Phycol., 29, 587–595.
Lewis, N., Wolny, J., Achenbach, J., Ellis, L., Pitula, J., Rafuse, C., Rosales, D. & McCarron, P. (2018). Identification, growth and toxicity assessment of Coolia meunier (Dinophyceae) from Nova Scotia, Canada. Harmful Algae, 75, 45–56. https://doi.org/10.1016/j.hal.2018.04.001
Litaker, R. W., Vandersea, M. W., Faust, M. A., Kibler, S. R., Nau, A. W., Holland, W. C., Chinain, M., Holmes, M., & Tester, P. A. (2010). Global distribution of ciguatera causing dinoflagellates in the genus Gambierdiscus. Toxicon, 56(5), 711–730. https://doi.org/10.1016/j.toxicon.2010.05.017
Lobel, P., Anderson, D., & Durand-Clement, M. (1988). Assessment of Ciguatera Dinoflagellate Populations: Sample Variability and Algal Substrate Selection. The Biological Bulletin, 175(1), 94–101. https://doi.org/10.2307/1541896
López-Rosales, L., Gallardo-Rodríguez, J. J., Sánchez-Mirón, A., Cerón-García, M. del C., Belarbi, E. H., García-Camacho, F., & Molina-Grima, E. (2013). Simultaneous effect of temperature and irradiance on growth and okadaic acid production from the marine dinoflagellate Prorocentrum belizeanum. Toxins, 6(1), 229–253. https://doi.org/10.3390/toxins6010229
Mangialajo, L., Ganzin, N., Accoroni, S., Asnaghi, V., Blanfuné, A., Cabrini, M., Chavanon, F., Chiantore, M., Cohu, S., Costa, E., Fornasaro, D., Grossel, H., Marco-Miralles, F., Masó, M., Reñé, A., Rossi, A., Sala, M., Thibaut, T., Totti, C., Vila, M., & Lemée, R. (2011). Trends in Ostreopsis proliferation along the Northern Mediterranean coasts. Toxicon, 57(3), 408–420. https://doi.org/10.1016/j.toxicon.2010.11.019
Marr, J., Hu, T., Pleasance, S., Quilliam, M., & Wright, J. (1992). Detection of new 7- O-acyl derivatives of diarrhetic shellfish poisoning toxins by liquid chromatography-mass spectrometry. Toxicon, 30(12), 1621–1630.
Matsuhiro, B., & Urzúa, C. (1990). Agars from Gracilaria chilensis (Gracilariales). Journal of Applied Phycology, 2(3), 273–279. https://doi.org/https//:10.1007/BF02179785
McLachlan, J. L., Marr, J. C., Conlon‐Keily, A., & Adamson, A. (1994). Effects of nitrogen concentration and cold temperature on DSP‐toxin concentrations in the dinoflagellate Prorocentrum lima (prorocentrales, dinophyceae). Natural Toxins, 2(5), 263–270. https://doi.org/10.1002/nt.2620020504
Moreira-González, A. R., Fernandes, L. F., Uchida, H., Uesugi, A., Suzuki, T., Chomérat, N., Bilien, G., & Mafra, L. L. (2018). Variations in morphology, growth, and toxicity among strains of the Prorocentrum lima species complex isolated from Cuba and Brazil. Journal of Applied Phycology, 31(1), 519–532. https://doi.org/10.1007/s10811-018-1587-y
Morton, S., & Faust, M. (1997). Survey of Toxic Epiphytic Dinoflagellates from the Belizean Barrier Reef Ecosystem. Bulletin of Marine Science -Miami, 61(3), 899–906.
Morton, S., Norris, D., & Bomber, J. (1992). Effect of temperature, salinity and light intensity on the growth and seasonality of toxic dinoflagellates associated with ciguatera. Journal of Experimental Marine Biology and Ecology, 157, 79–90. https://doi.org/10.1016/0022-0981(92)90076-M
Murakami, Y., Oshima, Y., & Yasumoto, T. (1982). Identification of Okadaic Acid As a Toxic Component of a Marine Dinoflagellate Prorocentrum lima. Nippon Suisan Gakkaishi, 48(1), 69–72. https://doi.org/https//:10.2331/suisan.48.69
Nagahama, Y., Murray, S., Tomaru, A., & Fukuyo, Y. (2011). Species boundaries in the toxic dinoflagellate Prorocentrum lima (Dinophyceae, Prorocentrales), based on morphological and phylogenetic characters. Journal of Phycology, 47(1), 178–189. https://doi.org/10.1111/j.1529-8817.2010.00939.x
Nakahara, H., Sakami, T., Chinain, M., & Ishida, Y. (1996). The role of macroalgae in epiphytism of the toxic dinoflagellate Gambierdiscus toxicus (Dinophyceae). Phycological Research, 44(2), 113–117. https://doi.org/10.1111/j.1440- 1835.1996.tb00385.x
Nascimento, S. M., Purdie, D. A., & Morris, S. (2005). Morphology, toxin composition and pigment content of Prorocentrum lima strains isolated from a coastal lagoon in southern UK. Toxicon, 45(5), 633–649. https://doi.org/10.1016/j.toxicon.2004.12.023
Nascimento, S. M., Salgueiro, F., Menezes, M., Oliveira, F. de A., Magalhães, V. C. P., De Paula, J. C., & Morris, S. (2016). Prorocentrum lima from the South Atlantic: Morphological, molecular and toxicological characterization. Harmful Algae, 57, 39–48. https://doi.org/10.1016/j.hal.2016.05.006
Nishimura, T., Uchida, H., Noguchi, R., Oikawa, H., Suzuki, T., Funaki, H., hara, C., Hagino, K., Arimitsu, S., Tanii, Y., Abe, S., Hashimoto, K., Mimura, K., Tanaka, K., Yanagida., & I. Adachi, M. (2020). Abundance of the benthic dinoflagellate Prorocentrum and the diversity, distribution, and diarrhetic shellfish toxin production of Prorocentrum lima complex and P. caipirignum in Japan. Harmful Algae, 96, 101687. https://doi.org/10.1016/j.hal.2019.101687
Okolodrov, Y., Merino-Virgilio, F., Aké-Castillo, J., Aguilar-Trujillo, A., Espinoza- Matías, S., & Herrera-Silveira, J. (2014). Seasonal changes in epiphytic dinoflallelate assemblages near the Northern coast ot the Yucatan peninsula, Gulf of Mexico. Acta Botanica Mexicana, 107, 121–151.
Parsons, M., & Preskitt, L. (2007). A survey of epiphytic dinoflagellates from the coastal waters of the island of Hawai’i. Harmful Algae, 6(5), 658–669. https://doi.org/10.1016/j.hal.2007.01.001
Parsons, M., Settlemier, C., & Ballauer, J. (2011). An examination of the epiphytic nature of Gambierdiscus toxicus, a dinoflagellate involved in ciguatera fish poisoning. Harmful Algae, 10(6), 598–605. https://doi.org/10.1016/j.hal.2011.04.011
Paz, B., Vázquez, J., Riobó, P., & Franco, J. (2006). Study of the effect of temperature, irradiance and salinity on growth and yessotoxin production by the dinoflagellate Protoceratium reticulatum in culture by using a kinetic and factorial approach. Marine Environmental Research, 62(4), 286–300. https://doi.org/10.1016/j.marenvres.2006.04.066
Pearce, I., Marshall, J., & Hallegraeff, G. (2001). No Title. In: Hallegraeff, G.M., Blackburn, S.I., Bolch, C.J., Lewis, R.J. (Eds.), Harmful Algal Blooms 2000. Intergovernmental Oceanographic Commission of UNESCO, Hobart, Tasmania, 54–57.
Penna, A., Garcés, E., Vila, M., Giacobbe, M. G., Fraga, S., Lugliè, A., Lugliè, A., Bravo, I., Bertozzini, & E. Vernesi, C. (2005). Alexandrium catenella (Dinophyceae), a toxic ribotype expanding in the NW Mediterranean Sea. Marine Biology, 148(1), 13–23. https://doi.org/10.1007/s00227-005-0067-5
Praptiwi, R. A. (2014). Optimisation of high value metabolite production from benthic marine dinoflagellate Prorocentrum lima. (Robert Gordon University). https://doi.org/10.1177/0266242610391936
Rains, L. K., & Parsons, M. L. (2015). Gambierdiscus species exhibit different epiphytic behaviors toward a variety of macroalgal hosts. Harmful Algae, 49, 29–39. https://doi.org/10.1016/j.hal.2015.08.005
Reguera, B., Alonso, R., Moreira, Á., & Silvia, M. (2011). Guía para el diseño y puesta en marcha de un plan de seguimiento de microalgas productoras de toxinas. Manuales y Guías COI de UNESCO y OIEA, Paris y Viena. Manuales y Guías de La COI, 59, 1–49.
Stein, J. (1973). Handbook of Phycological Methods: Culture Methods and Growth Measurements (Cambridge).
Tarazona-Janampa, U. (2019). Effect of associated bacteria on growth and toxigenicity in cultured isolates of the dinoflagellate Prorocentrum lima from Mexico Effect of associated bacteria on growth and toxigenicity in cultured isolates of the dinoflagellate Prorocentrum lima from Me (Universidad Veracruzana, Mexico). https://doi.org/htpps//:10.13140/RG.2.2.12826.90567
Tarazona-Janampa, U., Cembella, A., Pelayo-Zárate, M., Pajares, S., Márquez- Valdelamar, L., Okolodkov, Y., Tebben, J., Krock, B., & Durán-Riveroll, L. (2020). Associated Bacteria and Their Effects on Growth and Toxigenicity of the Dinoflagellate Prorocentrum lima Species Complex From Epibenthic Substrates Along Mexican Coasts. Frontiers in Marine Science |, 7(569), 1–18. https://doi.org/10.3389/fmars.2020.00569
Tawong, W., Nishimura, T., Sakanari, H., Sato, S., Yamaguchi, H., & Adachi, M. (2014). Distribution and molecular phylogeny of the dinoflagellate genus Ostreopsis in Thailand. Harmful Algae, 37, 160–171. https://doi.org/10.1016/j.hal.2014.06.003
Tester, P. A., Kibler, S. R., Holland, W. C., Usup, G., Vandersea, M. W., Leaw, C. P., Mohammad-Noor, N., Faust, M., & Litaker, R. W. (2014). Sampling harmful benthic dinoflagellates: Comparison of artificial and natural substrate methods. Harmful Algae, 39, 8–25. https://doi.org/10.1016/j.hal.2014.06.009
Torgensen, T., Miles, C., Rundberget, T., & Wilkins, A. (2008). New Esters of Okadaic Acid in Seawater and Blue Mussels (Mytilus edulis). J. Agric. Food Chem, 56, 9628–9635.
Uchida, H., Watanabe, R., Matsushina, R., Uchida, N., Nagai, H., Kamio, M., Murata, M., Yasumoto, T., & Suzuki, T. (2014). A Convenient HPLC Method for Detection of Okadaic Acid Analogs as 9-Anthrylmethyl Esters with Automated Sample Cleanup by Column Switching. Journal of Aoac International, 97(2), 391–397. https://doi.org/10.5740/jaoacint.SGEUchida
Vale, P., Veloso, V., & Amorim, A. (2009). Toxin composition of a Prorocentrum lima strain isolated from the Portuguese coast. Toxicon, 54(2), 145–152. https://doi.org/10.1016/j.toxicon.2009.03.026
Vanucci, S., Guerrini, F., Milandri, A., & Pistocchi, R. (2010). Effects of different levels of N- and P-deficiency on cell yield , okadaic acid , DTX-1 , protein and carbohydrate dynamics in the benthic dinoflagellate Prorocentrum lima. Harmful Algae, 9(6), 590–599. https://doi.org/10.1016/j.hal.2010.04.009
Varkitzi, I., Hatzianestis, I., Pyrgaki, C., Pagou, K., Granelí, E., Pavlidou, A., Montesanto, B., & Economou-Amilli, A. (2010). Unbalanced N:P ratios and nutrient stress controlling growth and toxin production of the harmful dinoflagellate Prorocentrum lima (Ehrenberg) Dodge. Harmful Algae, 9, 304– 311. https://doi.org/10.1016/j.hal.2009.12.001
Varkitzi, I., Pagou, K., Pyrgaki, C., & Hatzianestis, I. (2017). A Biomass Upscale System for the Marine Dinoflagellate Prorocentrum lima and the Production of Bioactive Lipophilic Toxins. International Journal of Applied Sciences and Biotechnology, 5(4), 479–485. https://doi.org/10.3126/ijasbt.v5i4.18561
Wang, L., Wang, X., Wu, H., & Liu, R. (2014). Overview on biological activities and molecular characteristics of sulfated polysaccharides from marine green algae in recent years. In Marine Drugs (Vol. 12). https://doi.org/10.3390/md12094984
Wang, S., Chen, J., Li, Z., Wang, Y., Fu, B., Han, X., & Zheng, L. (2015). Cultivation of the benthic microalga Prorocentrum lima for the production of diarrhetic shellfish poisoning toxins in a vertical flat photobioreactor. Bioresource Technology, 179, 243–248. https://doi.org/https//:10.1016/j.biortech.2014.12.019
Wu, H., Chen, J., Peng, J., Zhong, Y., Guo, M., Tan, Z., Tan, Z., Zhai, Y., & Lu, S. (2020). Nontarget screening and toxicity evaluation of diol esters of okadaic acid and dinophysistoxins reveal intraspecies difference of Prorocentrum lima. Environmental Science & Technology, 1–40. https://doi.org/10.1021/acs.est.0c03691
Yang, A., Lee, S., Du Yoo, Y., Seop Kim, H., Ju Jeong, E., & Rho, J. (2017). Limaol: A Polyketide from the Benthic Marine Dinoflagellate Prorocentrum lima. Journal of Natural Products, 80, 1688–1692. https://doi.org/10.1021/acs.jnatprod.7b00127

