



ARTÍCULOS DE INVESTIGACIÓN
Determinación de concentraciones hormonales (estradiol y progesterona) durante la desviación folicular en llamas
Determination of hormone concentrations (estradiol and progesterone) during follicular detour in llamas
Journal of the Selva Andina Animal Science
Selva Andina Research Society, Bolivia
ISSN: 2311-3766
ISSN-e: 2311-2581
Periodicidad: Bianual
vol. 12, núm. 2, 2025
Recepción: 01 mayo 2025
Corregido: 01 agosto 2025
Aprobación: 01 septiembre 2025
Publicación: 01 octubre 2025

Resumen: El objetivo fue determinar mediante ultrasonografía y concentración de estradiol y progesterona durante la desviación folicular en llamas, como primer reporte en camélidos sudamericanos. Se utilizaron 10 hembras en condiciones del Altiplano Peruano, las que se evaluaron la desviación folicular desde la ablación folicular (día 0) hasta el día 6 con evaluaciones ultrasonográficas diarias con un equipo SonoStar SS8 con un transductor microconvexo lineal endocavitario a 6.5 MHz en modo 2B, las muestras sanguíneas fueron para determinar el estradiol y progesterona mediante ELISA, todos los datos fueron analizados mediante estadística y gráficos descriptivos en el programa Jamovi 2.23. Las concentraciones fueron evaluadas desde el día 0 a 6 siendo las concentraciones de estradiol y progesterona promedio de 0.9105 ng mL-1 y 1.11 ng mL-1 respectivamente que, aunque se muestra cambios numéricos mínimos se observó un patrón en ambas hormonas esteroides con un incremento de sus respectivas concentraciones el día 4 post ablación folicular. En conclusión, la desviación folicular en llamas inicio el día 4 post ablación folicular que coincide con el incremento de las concentraciones de estradiol y progesterona, sin embargo, es necesario realizar más estudios para determinar el proceso de desviación folicular en llamas.
Palabras clave: Desviación folicular, ELISA, estradiol, folículos, llamas, progesterona.
Abstract: The objective was to determine by ultrasonography and concentration of estradiol and progesterone during follicular deviation in llamas, as the first report in South American camelids. 10 females were used in conditions of the Peruvian Altiplano, which were evaluated for follicular deviation from follicular ablation (day 0) to day 6 with daily ultrasonographic evaluations with a SonoStar SS8 equipment with a linear endocavity microconvex transducer at 6.5 MHz in mode 2B, blood samples were to determine estradiol and progesterone by ELISA, all data were analyzed using statistics and descriptive graphs in the Jamovi 2.23 program. Concentrations were evaluated from day 0 to 6, with average estradiol and progesterone concentrations of 0.9105 ng mL-1 and 1.11 ng mL-1, respectively, which, although minimal numerical changes are shown, a pattern was observed in both steroid hormones with an increase in their respective concentrations on day 4 after follicular ablation. In conclusion, the llamas follicular deviation began on day 4 after follicular ablation that coincides with the increase in estradiol and progesterone concentrations; however, further studies are needed to determine the process of follicular deviation in llamas.
Keywords: ELISA, estradiol, follicular deviation, follicles, llamas, progesterone.
Introducción
La fisiología reproductiva en camélidos sudamericanos (CSA) posee características propias a diferencia de las demás especies domésticas, con una dinámica folicular en ondas sucesivas y sobrepuestas, así como ovulación inducida como principales particularidades1-3. Las características principales de la dinámica folicular en CSA son sus fases y duración que las clasifica en crecimiento variando de 3 a 9 días; maduración de 2 a 8 días y regresión de 3 a 8 días evaluadas en alpacas y llamas3-5, con tasas de crecimiento promedio en alpacas 0.43 mm/día y en llamas 0.5 a 0.9 mm/día2,5,6, resultados que permitieron caracterizar de forma general parte de la actividad ovárica en CSA, teniendo en cuenta que existen más fenómenos (reclutamiento, selección, desviación y regresión folicular) dentro la dinámica folicular.
En especies monoovulares como los camélidos, solo uno de muchos folículos se convierte en dominante este proceso, conocido como selección, que se caracteriza con la adquisición de una tasa de crecimiento mayor frente a los demás folículos (folículos subordinados) esta característica se denomina desviación folicular7,8, que inicia con un reclutamiento en promedio de 7 a 11 folículos por cohorte con diámetros de 4 mm (vacunos) y 6 mm (yeguas), alcanzando diámetros foliculares de desviación folicular de 8.5 a 7.7 mm en vacunos y de 22.5 a 19 mm en yeguas. Estudios actuales en camellos reportan diámetros de folículos reclutados entre 4.4 y 3.5 mm y folículos desviados de 7.43 y 7.75 mm en presencia de un solo folículo dominante (FD) y codominancia respectivamente8,9, resultados importantes para el conocimiento de la fisiología reproductiva de hembras. Sin embargo, no existe reportes sobre la desviación folicular en CSA que brinden un aporte importante para la aplicación de biotecnologías reproductivas.
En los últimos años el desarrollo de biotecnologías reproductivas ha requerido de un mayor conocimiento sobre fisiología reproductiva, contando con la ayuda de técnicas como análisis hormonal y principalmente de la ultrasonografía6,10; el eficiente manejo reproductivo con el uso de inseminación artificial (IA) y transferencia de embriones (TE) precisa de conocimientos amplios de la dinámica folicular y factores que la afectan4,11, el monitoreo de la desviación folicular permite explicar algunas particularidades en la TE en camélidos; se reportan algunas veces más de un embrión a ovulación simple12,13 y respuesta a los protocolos de multiovulación con la evaluación del tiempo que toma la desviación folicular y el número de folículos reclutados para predecir la probable respuesta a los protocolos. En tal sentido, el objetivo fue caracterizar mediante ultrasonografía y concentración de 17β-estradiol el proceso de desviación folicular en llamas, como un primer reporte en CSA.
Materiales y métodos
Animales y alimentación. El estudio fue realizado en las instalaciones de la Facultad de Medicina Veterinaria y Zootecnia, de la Universidad Nacional del Altiplano Puno ubicado a una altitud de 3812 metros sobre el nivel del mar (msnm) el experimento fue llevado entre los meses de mayo y agosto. Se seleccionaron diez (n=10) hembras no preñadas, multíparas, con edad entre 4 a 6 años, todas con una condición corporal entre 2.5 a 3.0 según la escala recomendada por Van Saun14. Los animales fueron alimentados con pastos naturales, agua ad libitum y suplementados diariamente con heno de avena.
Características generales de la ultrasonografía de ovarios. Los pasos previos fueron de sujeción y preparación de llamas higienizando la zona perineal y su vulva, además del transductor puesto que la evaluación fue realizada por vía transvaginal con un equipo SonoStar SS8 (SonoStar Thecnologies, China) con un transductor microconvexo lineal endocavitario (V6S9 multifrecuencia: examen transvaginal) a 6.5 MHz en modo 2B para observar un lado para cada ovario (Figura 1) con la opción de freeze se paralizó las imágenes15-17para su almacenamiento y posterior evaluación, tal como se detalla a continuación:
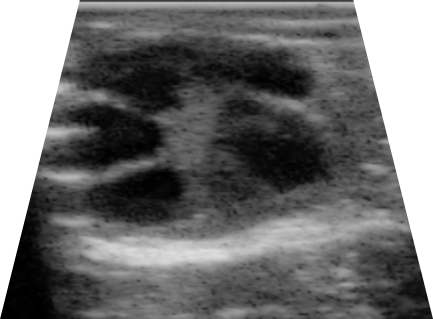
Ablación folicular o sincronización de onda folicular. Se procedió a realizar la ablación folicular (día 0) tal como recomienda diversos autores18,19 con algunas modificaciones de la presión de bomba de vacío de 110 mmHg en nuestro caso, seguidamente se evaluó diariamente para observar el reclutamiento determinado por la presencia de un nuevo pool de folículos con diámetros entre 1.5 a 2.5 mm registrado el número de folículos y el tiempo transcurrido, identificando a cada uno de los folículos con la terminología F1, F2, F3 y F4 según sea el caso tal como recomienda Goodman & Hodgen20.
Caracterización de la desviación folicular. Las evaluaciones fueron realizadas diariamente a partir del día de ablación folicular (día 0) durante las mañanas a cada uno de los animales, primero identificando a cada uno de los folículos como F1, F2, F3 y F4 según sea el caso, siendo para una solo FD el F1 como futuro folículo desviado9,20. Identificando a los folículos como estructuras redondeadas definidas y anecogénicas, las mediciones se hicieron por el interior de las paredes foliculares, tomando dos diámetros utilizando el promedio de estas como diámetro final de los folículos4,21.
Muestra sanguínea y evaluación hormonal (estradiol y progesterona). Las muestras fueron obtenidas mediante punción de la vena yugular diariamente (días 0, 1, 2, 3, 4, 5 y 6 post ablación folicular) en tubos con heparina que fueron centrifugados inmediatamente, el plasma sanguíneo fue almacenado a -20° C hasta la evaluación. La concentración de 17β-estradiol fue determinado usando un kit comercial de ELISA (Estradiol ELISA, 17β-estradiol antigénico, DiaMetra, Case for quality, Italy) y progesterona (Progesterone ELISA kit Enzo, Farmingdale, NY, USA) siguiendo los pasos del inserto del producto para su procesamiento con un equipo de ELISA (Organon Teknica, Microwell System, modelo Reader 230S).
Análisis estadístico. Los datos fueron analizados mediante estadística descriptiva para facilitar su interpretación, para la comparación tanto con un solo FD fueron sometidos a pruebas normalidad (Shapiro-Wilk) y homocedasticidad (Levene) resultando en todos ellos la no significancia estadística con un análisis de varianza (one way); las concentraciones de estradiol y progesterona solo fueron descritos desde el día de ablación hasta la desviación folicular. Los análisis estadísticos fueron realizados mediante el programa estadística (R versión 4.0.2)22 con el paquete Rcmdr y los gráficos mediante el programa Microsoft Excel®.
Resultados
Diámetros foliculares de un solo FD pre y post desviación folicular. Tabla 1 evalúa los diámetros foliculares pre y post desviación folicular, observando antes de desviación en ambos casos diámetros similares siendo 2.21±0.89, 2.24±0.89, 2.65±0.93, 2.25±0.67 y 2.37±0.66 para el F1, F2, F3, F4 y F5 respectivamente. Los diámetros post desviación folicular muestran diferencias importantes, este fenómeno en llamas de 6.01±0.73 para F1, 2.05±0.52 para F2, 2.25±0.54 para F3, 2.05±0.78 para F4 y 2.07±0.56 para F5 (folículos subordinados).
| Pre - desviación | Post - desviación (día 5) | |
| F1 | 2.21 ± .89 | 6.01 ± .73 |
| F2 | 2.24 ± .89 | 2.05 ± .52 |
| F3 | 2.65 ± .93 | 2.25 ± .54 |
| F4 | 2.25 ± .67 | 2.05 ± .78 |
| F5 | 2.37 ± .66 | 2.07 ± .56 |
| Valor de "p" | .9339 | ˂.0001 |
Las tasas de crecimiento del folículo pre y post desviación folicular. Fueron en presencia de un solo folículo de 0.656 mm/día y de 0.58 mm/día en presencia de codominancia mientras que los demás folículos con una tasa de decrecimiento que variaron de -0.01 mm/día a -0.24 mm/día, que confirman el proceso de desviación folicular (incremento de tasa de crecimiento) en las llamas evaluadas. También es necesario indicar que la diferenciación de los diámetros de los folículos desviados fue identificada entre el día 3 y 4 post ablación folicular que coincide con las concentraciones de hormonas que a continuación de especifica.
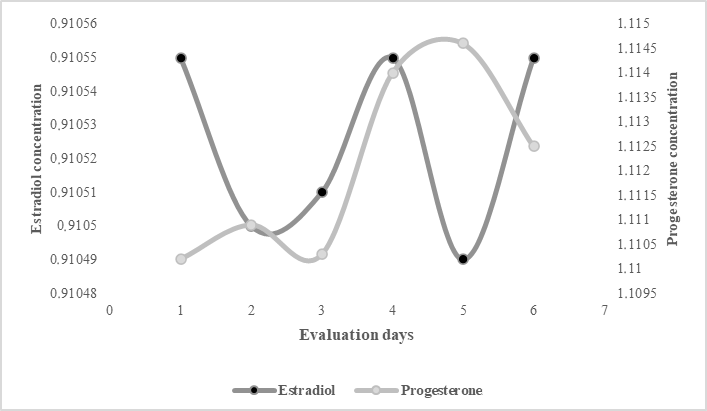
Concentración hormonal de estradiol y progesterona. Figura 2 muestra la relación existente entre la concentración de estradiol y progesterona al día 4 post ablación folicular, las concentraciones de 17β-estradiol poseen un incremento al inicio (antes de ablación estradiol folicular) debido a la presencia del FD de la anterior onda folicular, del mismo modo se observa una relación más directa por parte de la progesterona con los diámetros foliculares promedios evaluados para ambos casos de desviación folicular, coincidiendo el día 4 como el inicio de la diferenciación de los futuros FD aumentando su diámetro a diferencia de la disminución de diámetro de los folículos subordinados (desviación folicular en llamas).
Discusión
La presencia de dominancia simple es una característica reportada en CSA, camellos y vacunos6,9,23, sin embargo, se reporta la codominancia que consiste en el crecimiento de 2 folículos en una misma onda folicular en ambos casos observamos una relación directa con el aumento de las concentraciones de estradiol y progesterona desde el día 3 y 4 post ablación folicular, la desviación folicular es un fenómeno estudiado ampliamente en vacunos. Mencionan que existe un ligero aumento de gonadotropinas (FSH y LH) antes de la desviación folicular23,24, probablemente podría estar sucediendo el mismo fenómeno en CSA, sin embargo, el comportamiento de las gonadotropinas antes y después de la desviación folicular en camélidos no han sido estudiados.
La desviación folicular se define como un cambio en la tasa de crecimiento de los futuros FD a diferencia de los folículos subordinados8, fenómeno similar en llamas, observamos tasas diferenciadas de los futuros para un solo folículo en caso de codominancia, tasas de crecimiento similares a lo reportado en llamas y camellos6,9,16 durante la fase de crecimiento de la onda folicular y tasas de regresión para los folículos subordinados reportados en camélidos, camellos y vacunos6,8,9. El inicio de la desviación folicular en llamas inicia el día 4 post ablación folicular tanto en presencia de un solo FD con un diámetro de 4.01 mm, el día de inicio de desviación folicular fueron similares a lo reportado en camellos como especie más compatible a las llamas9 así como en vacunos con un tiempo parecido del inicio de desviación folicular25-27. Mientras que los futuros FD diferenciados el día 5 post ablación folicular (Tabla 1) siendo de 6.01 mm, infiriendo estos resultados como los primeros hallazgos en llamas.
Los niveles de estradiol y progesterona durante el proceso de desviación folicular tienen un patrón compatible con el crecimiento folicular observado durante el reclutamiento folicular (día 1, 2 y 3) incrementando juntamente con la desviación folicular los niveles hormonales el día 4 post ablación folicular (Figura 2) estos resultados solamente son descriptivos porque es el primer reporte de la desviación folicular en llamas, sin embargo, este patrón compatible entre el 17β-estradiol y diámetros foliculares (fases de crecimiento, estática y regresión) es similar a lo reportado en alpacas, llamas, guanacos y vicuñas durante la evaluación de la onda folicular en estas especies6,28-31. En conclusión, la desviación folicular en llamas inicio el día 4 post ablación folicular con diámetros de 4.01 mm en presencia de un FD con un patrón similar de las concentraciones de estradiol y progesterona durante la desviación folicular, siendo un primer reporte en camélidos sudamericanos; sin embargo, son necesarias mayor cantidad de artículos sobre el proceso de desviación folicular.
Literatura citada
1. Adams GP, Sumar J, Ginther OJ. Effects of lactational and reproductive status on ovarian follicular waves in llamas (Lama glama). J Reprod Fertil 1990;90(2):535-45. DOI: https://doi.org/10.1530/jrf.0.0900535. PMID: 2250251.
2. Cavilla MV, Bianchi CP, Maistruarena C, Aba MA. Ultrasonographic and endocrine characterization of follicular waves in llamas with a special reference to the overlapping phenomenon during successive waves. Reprod Domest Anim 2013;48 (6):923-30. DOI: https://doi.org/10.1111/rda.12187. PMID: 23758493.
3. Vaughan J. Ovarian function in South American camelids (alpacas, llamas, vicunas, guanacos). Anim Reprod Sci 2011;124(3-4):237-43. DOI: https://doi.org/10.1016/j.anireprosci.2010.08.031. PMID: 20875933.
4. Tibary A. Monitoring and controlling follicular activity in camelids. Theriogenology 2018;109: 22-30. DOI: https://doi.org/10.1016/j.theriogenology.2017.12.011. PMID: 29249328.
5. Vaughan JL, Macmillan KL, D'Occhio MJ. Ovarian follicular wave characteristics in alpacas. Anim Reprod Sci 2004;80(3-4):353-61. DOI: https://doi.org/10.1016/j.anireprosci.2003.08.002. PMID: 15036510.
6. Gallelli MF, Bianchi C, Zampini E, Aba M, Gambarotta M, Miragaya M. Plasma IGF1 and 17β-estradiol concentrations during the follicular wave in llamas. Front Vet Sci 2020;7:555261. DOI: https://doi.org/10.3389/fvets.2020.555261. PMID: 331 95527; PMCID: PMC7661775.
7. Gimenes LU, Carvalho NA, Sá Filho MF, Van-nucci FS, Torres-Júnior JR, Ayres H, et al. Ultra-sonographic and endocrine aspects of follicle deviation, and acquisition of ovulatory capacity in buffalo (Bubalus bubalis) heifers. Anim Reprod Sci 2011;123(3-4):175-9. DOI: https://doi.org/10.1016/j.anireprosci.2010.12.004. PMID: 21256685.
8. Ginther OJ, Beg MA, Donadeu FX, Bergfelt DR. Mechanism of follicle deviation in monovular farm species. Anim Reprod Sci 2003;78(3-4):239-57. DOI: https://doi.org/10.1016/s0378-4320(03)00093-9. PMID: 12818647.
9. Manjunatha BM, Al-Bulushi S, Pratap N. Ultra-sonographic characterization of follicle deviation in follicular waves with single dominant and codominant follicles in dromedary camels (Camelus dromedarius). Reprod Domest Anim 2014;49(2):239-42. DOI: https://doi.org/10.1111/rda.12260. PMID: 24325149.
10. Huanca W, Cordero A, Huanca Manami T, Adams GP. Reproductive biotechnologies in domestic South American camelids: advances and perspectives. Arch Latinoam Prod Anim 2007;15 (Supl 1):195-201.
11. Tibary A, Anouassi A, Khatir H. Update on reproductive biotechnologies in small ruminants and camelids. Theriogenology 2005;64(3):618-38. DOI: https://doi.org/10.1016/j.theriogenology.2005.05.016. PMID: 15964064.
12. Pacheco J, Vélez V, Pezo D. Evaluation of the efficiency of interspecies embryo transfer between alpacas and llamas obtained through single ovulation. Rev Investig Vet Perú 2016;27(1):64-9. DOI: http://dx.doi.org/10.15381/rivep.v27i1.11464
13. Pérez U, Quispe Y, Luque N, Rojas R, Condori E, Delgado A, et al. Ultrasonographic evaluation in Brown Swiss cattle subjected to a heat synchronization protocol in the Peruvian highlands. Rev Investig Vet Perú 2019;30(1):489-94. DOI: http://dx.doi.org/10.15381/rivep.v30i115688
14. Van Saun RJ. Nutritional requirements and assessing nutritional status in camelids. Vet Clin North Am Food Anim Pract 2009;25(2):265-79. DOI: https://doi.org/10.1016/j.cvfa.2009.03.003. PMID: 19460639.
15. Cancino AK, Aller JF, Rebuffi G, Alberio RH. Control de la dinámica folicular ovárica en llamas (Lama glama) en posparto temprano. Arch Zootec 2011;60(232):1009-20. DOI: https://dx.doi.org/10.4321/S0004-05922011000400017
16. Perez U, Gonzáles E, Huayta R, Apaza M, Quispe Y, Pérez M. Factors that affect the transfer of embryos from alpacas (Vicugna pacos) to llamas (Lama glama). Rev Investig Vet Perú 2019; 30(4):1645-52. DOI: http://dx.doi.org/10.15381/rivep.v20i4.17276
17. Ratto M, Gomez C, Berland M, Adams GP. Effect of ovarian superstimulation on COC collection and maturation in alpacas. Anim Reprod Sci 2007; 97(3-4):246-56. DOI: https://doi.org/10.1016/j.anireprosci.2006.02.002. PMID: 16530992.
18. Huanca WF, Hilari FY, Villanueva JC, Uchuari M, Huanca W. 100 Use of seminal plasma, human chorionic gonadotropin, and follicular ablation on the interval to follicular wave emergency and dominant follicle in alpacas (Vicugna pacos). Reprod Fertil Dev 2018;30:189-90. DOI: https://doi.org/10.1071/RDv30n1Ab100
19. Silva N, Huanca WF, Medina G, Huanca W. Application effect of seminal plasma, GnRH and follicular ablation on the ovarian dynamic in llamas (Lama glama). Rev Investig Vet Perú 2020;31(4):e19033. DOI: http://dx.doi.org/10.15381/rivep.v31i4.19033
20. Goodman AL, Hodgen GD. The ovarian triad of the primate menstrual cycle. Recent Prog Horm Res 1983;39:1-73. DOI: https://doi.org/10.1016/b978-0-12-571139-5.50005-7. PMID: 6415767.
21. Parraguez VH, Adams G, Ratto M, Raggi L. Camelids. In: DesCôteaux L, Colloton J, Gnemmi G, editors. Practical Atlas of Ruminant and Camelid Reproductive Ultrasonography. Oxford: Blackwell Publishing; 2009. p. 211-23. DOI: https://doi.org/10.1002/9781119265818.ch12
22. The RCore Team. R: ALanguage and Environment for Statistical Computing [Internet]. Vienna: Foundation for Statistical Computing; 2024 [cited June 2, 2025]. 3946 p. Retrieved from: https://cran.r-project.org/doc/manuals/r-release/fullrefman.pdf
23. Wiltbank MC, Fricke PM, Sangsritavong S, Sartori R, Ginther OJ. Mechanisms that prevent and produce double ovulations in dairy cattle. J Dairy Sci 2000;83(12):2998-3007. DOI: https://doi.org/10.3168/jds.S0022-0302(00)75201-5. PMID: 11132873.
24. Kulick LJ, Bergfelt DR, Kot K, Ginther OJ. Follicle selection in cattle: follicle deviation and codominance within sequential waves. Biol Reprod 2001;65(3):839-46. DOI: https://doi.org/10.1095/biolreprod65.3.839. PMID: 11514349.
25. Ginther OJ, Bergfelt DR, Kulick LJ, Kot K. Selection of the dominant follicle in cattle: role of two-way functional coupling between follicle-stimulating hormone and the follicles. Biol Reprod 2000;62(4):920-7. DOI: https://doi.org/10.1095/biolreprod62.4.920. PMID: 10727261.
26. Ginther OJ, Dangudubiyyam SV. Effect of number of 6-mm predeviation follicles and intraovarian patterns on right-side ovulation in heifers. Anim Reprod Sci 2019;202:73-9. DOI: https://doi.org/10.1016/j.anireprosci.2019.01.011
27. Sartori R, Fricke PM, Ferreira JC, Ginther OJ, Wiltbank MC. Follicular deviation and acquisition of ovulatory capacity in bovine follicles. Biol Reprod 2001;65(5):1403-9. DOI: https://doi.org/10.1095/biolreprod65.5.1403. PMID: 11673256.
28. Bravo PW, Fowler ME, Stabenfeldt GH, Lasley BL. Ovarian follicular dynamics in the llama. Biol Reprod 1990;43(4):579-85. DOI: https://doi.org/10.1095/biolreprod43.4.579. PMID: 2126962.
29. Chaves MG, Aba M, Agüero A, Egey J, Berestin V, Rutter B. Ovarian follicular wave pattern and the effect of exogenous progesterone on follicular activity in non-mated llamas. Anim Reprod Sci 2002;69(1-2):37-46. DOI: https://doi.org/10.1016/s0378-4320(01)00173-7. PMID: 11755715.
30. Miragaya MH, Aba MA, Capdevielle EF, Ferrer MS, Chaves MG, Rutter B, et al. Follicular activity and hormonal secretory profile in vicuna (Vicugna vicugna). Theriogenology 2004;61(4): 663-71. DOI: https://doi.org/10.1016/s0093-691x(03)00238-3. PMID: 14698056.
31. Riveros JL, Schuler G, Bonacic C, Hoffmann B, Chaves MG, Urquieta B. Ovarian follicular dynamics and hormonal secretory profiles in guanacos (Lama guanicoe). Anim Reprod Sci 2010;119(1-2):63-7. DOI: https://doi.org/10.1016/j.anireprosci.2009.11.005. PMID: 20022436.
Notas
__________
__________
__________
__________
__________
__________
__________
__________
__________
__________
Notas de autor
Uri Harold Perez Guerra E-mail address : uperez@unap.edu.pe
Enlace alternativo

