1. Introdução
A avifauna brasileira é representada por cerca de 1.900 espécies reconhecidas, correspondendo a mais de 60% das espécies encontradas na América do Sul (CBRO, 2014). O Estado de Minas Gerais tem registradas 753 espécies de aves (Andrade, 1997). Essa riqueza representa cerca de 40% da avifauna brasileira (CBRO, 2014). Em grande parte, a riqueza de espécies de aves em Minas Gerais se deve à variedade de formações vegetais no Estado, que inclui campos, matas, veredas, caatinga e cerrados (Franchin, 2009).
O bioma Cerrado é a maior, mais rica e, provavelmente, a mais ameaçada savana tropical do mundo em relação a sua avifauna (Franchin et al., 2008). É considerada a segunda maior ecorregião do Brasil, cobrindo 25% do território nacional. Recentemente este bioma começou a receber a mesma atenção conservacionista dispensada às florestas tropicais úmidas, uma vez que o grande crescimento das atividades econômicas já modificou cerca de 67% de suas áreas (Myers et al., 2000). No entanto, apesar de sua extensão e de sua importância para a conservação da biodiversidade, o Cerrado é pouco representado em termos de áreas protegidas. Apenas 3% de sua extensão original estão protegidos em parques e reservas federais e estaduais (Horta et al., 2002). Apesar de relativamente bem conservado em comparação com outras regiões do Brasil, o Espinhaço Meridional vem sofrendo diversos impactos ambientais que comprometem direta ou indiretamente sua avifauna. Dentre eles, destacam-se a mineração, a expansão urbana, o turismo descontrolado, a criação de gado e as queimadas (Vasconcelos et al., 2008).
Excelentes bioindicadores, as aves ocupam variados ambientes e são em geral facilmente detectáveis pelos pesquisadores, o que proporciona o uso de listagens desse grupo como uma das ferramentas para avaliação ambiental (Furness e Greenwood, 1993). O estudo sobre a alimentação das aves pode fornecer informações adicionais sobre a estrutura trófica de comunidades, bem como as condições físicas ambientais (Piratelli e Pereira, 2002), pois elas exploram recursos alimentares variados em habitats específicos (Villanueva e Silva, 1996). A estrutura trófica de um ecossistema é a organização de uma comunidade baseada nas relações de alimentação das populações. Estudos sobre a estrutura trófica das comunidades de aves ainda são raros, particularmente no Cerrado.
Neste contexto, este estudo busca fornecer informações sobre a estrutura trófica da avifauna em formações savânicas (cerrado típico e cerrado rupestre) de três áreas que se encontram em diferentes estados de conservação na Serra do Espinhaço Meridional, procurando responder as seguintes perguntas: Há diferença na estrutura trófica da avifauna entre as áreas de estudo? Quais espécies de aves são endêmicas e/ou ameaçadas e qual a similaridade do grupo entre as áreas estudadas?
2. Material e Métodos
2.1 Caracterização
da área de estudo
O estudo foi realizado em três áreas em diferentes estágios de degradação localizadas na porção meridional da Serra do Espinhaço (Figura 1). Submetidas a um clima regional do tipo Cwb, de acordo com a classificação climática de Köppen, apresentam clima tipicamente tropical, caracterizado por verões brandos e úmidos (outubro a abril) e invernos mais frescos e secos (junho a agosto). A precipitação média anual varia de 1250 a 1550 mm, onde a estação chuvosa inicia-se em novembro e termina em março, com média de precipitação pluviométrica 223,19 mm para o período. A estação seca inicia-se em junho, estendendo-se até agosto, com média de precipitação de 8,25 mm com períodos de transição, chuvoso-seco em abril e maio, e seco-chuvoso em setembro e outubro. A temperatura média anual situa-se na faixa de 18 a 19°C, sendo predominantemente amenas durante todo o ano, devido às superfícies mais elevadas do relevo. A umidade relativa do ar é quase sempre elevada, revelando médias anuais de 75,6% (Neves et al., 2005).
Área 1 – BL (Figura 1A): O trecho amostrado encontra-se situada entre as coordenadas 18°11’54”N/43°35’098”S e 18°12’23’’N/43º33’59’’S e engloba os seguintes ambientes: (a) uma área de cascalheira com cerca de 8,4 ha, está localizada dentro do Parque Estadual do Biribiri (PEBi). A qual originou-se com a retirada de cascalho para a construção da rodovia BR-367; (b) a rodovia BR-367; (c) a periferia da área urbanizada do campus JK da UFVJM; e (d) o antigo depósito de lixo da cidade de Diamantina, com cerca de 8,5 ha, desativado em 2002 e desde então em processo de recuperação.
O trecho inventariado encontra-se a uma altitude média de 1412 m com vegetação predominante de Campo rupestre e mancha de floresta Estacional Semidecidual. A vegetação é bastante heterogênea, considerando a presença de algumas famílias como: Solanaceae, Melastomataceae, Asteraceae (muitos exemplares de Eremanthus erythropappus introduzidos) e Passifloraceae (Passiflora setaceae, também introduzidos), também foi observado à presença de espécies exóticas e invasoras (p. ex. Musa paradisiaca, Brachiaria brizantha e Melinis minutiflora) (Marques, 2012).
A região da Serra do Espinhaço constituía-se na maior produtora (oficial) de diamantes do Brasil, sobretudo em decorrência da produção obtida no Rio Jequitinhonha. A presença de ouro nos numerosos veios de quartzo auríferos existentes na região é relatada em vários trabalhos e nos diversos relatórios sobre a geologia do Espinhaço. Esses tipos de explorações minerais eram muito comuns onde até hoje se encontra o Parque Estadual do Biribiri, sendo ainda possível encontrar resquícios e áreas completamente degradadas por esse tipo de atividade.
Área 2 – PF (Figura 1B): O trecho amostrado encontra-se sob as coordenadas 18°15’18”N/43°39’53”S e 18º15’44’’/43º39’59’’S e é uma área pertencente à Companhia de Saneamento de Minas Gerais (COPASA – MG), abrigando a nascente do Córrego das Pedras, manancial utilizado para o fornecimento de água para a população diamantinense (Campos, 2009).
A área possui altitude média de 1366 m e apresenta relevo plano, com afloramentos de rochas quartzíticas (Almeida-Abreu, 1996). A vegetação é caracterizada pelo predomínio de espécies herbáceas (principalmente das famílias: Xyridaceae, Eriocaulaceae, Cyperaceae, Gentianaceae, Lentibulariaceae, Bromeliaceae e Poaceae) e com raros arbustos, ausência de árvores de grande porte (Abreu-Filho et al. 2021), fitofisionomicamente pode ser classificada como predominantemente composta por Campo Limpo úmido, com inserções de Campos Rupestres e Capões de Mata.
Área 3 – RP (Figura 1C): O trecho estudado encontra-se inserido no Parque Estadual do Rio Preto (PERP) localizado no município de São Gonçalo do Rio Preto, sob as coordenadas 18°05’23”N/43°20’28”S e 18°06’59’’N/43º20’25’’S.
Comparando-se as três áreas de estudos, o PERP apresenta uma vegetação razoavelmente homogênea, com espécies nativas típicas do Cerrado, como o pequi (Caryocar brasiliensis). Nesse local de estudo, encontramos representantes das famílias Asteraceae, Myrsinaceae, Fabaceae, Myrtaceae, entre outras. Mesmo sendo a vegetação relativamente homogênea, a área tem ainda um padrão florístico bem diversificado, possuindo espécies restritas ás matas ciliares e de galeria da Serra do Espinhaço, tais como: Tibouchina candolleana, Lavoisiera imbricata e Cybianthus glaber (Foresto, 2008).
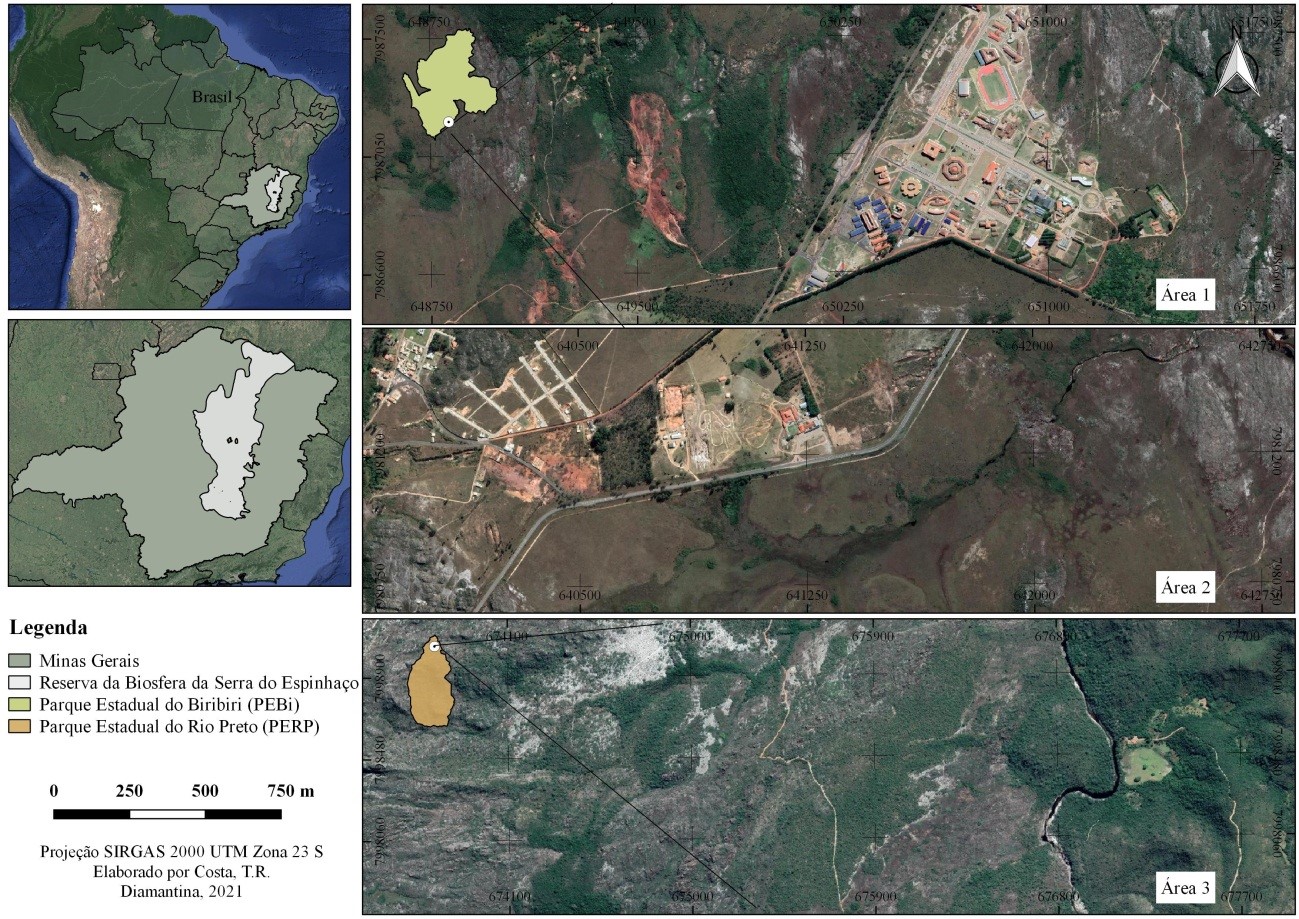 Figura 1. Localização das
áreas de estudo com destaque para Reserva da Biosfera da Serra do Espinhaço
(RBSE). Onde: Área 1 = Parque Estadual do Biribiri e
Antigo depósito de lixo de Diamantina (BL); Área 2 = Manancial APA Pau-de-Fruta
(PF); Área 3 = Parque Estadual do Rio Preto (RP)
NASA (2020); IBGE (2010).
Figura 1. Localização das
áreas de estudo com destaque para Reserva da Biosfera da Serra do Espinhaço
(RBSE). Onde: Área 1 = Parque Estadual do Biribiri e
Antigo depósito de lixo de Diamantina (BL); Área 2 = Manancial APA Pau-de-Fruta
(PF); Área 3 = Parque Estadual do Rio Preto (RP)
NASA (2020); IBGE (2010).
2.2 Coleta de dados
As amostragens foram realizadas no período de novembro de 2011 a janeiro de 2013. Totalizou-se 15 visitas em cada área de estudo, cada uma com duração de oito horas. As observações concentraram-se nas primeiras (6-10 h) e últimas (14-18 h) horas do dia, atendendo ao período de maior atividade das aves, perfazendo 360 horas de esforço amostral. Foram realizadas sete amostragens na estação seca (abril a outubro) e oito na estação chuvosa (novembro a março).
Foram utilizados dois métodos básicos: auditivo e visual. As amostragens foram feitas pelo método do Transecto Linear, considerando-se 25 m de cada lado da trilha. Foram percorridas em cada uma das áreas estudadas, transectos de 5 km dentro dos limites dos locais aproveitando-se de trilhas pré-existentes, lentamente e com paradas frequentes, registrando-se as espécies de aves vistas e, ou ouvidas. Assim foram visitados um total de 100 ha em cada área amostrada, levando-se em consideração os 5 km de transecto e os 200 m de buffer em cada lado das trilhas percorridas.
Para o método visual, utilizou-se de binóculos Nikon 10 × 50 mm, e sempre que possível, as aves foram registradas por meio de câmera digital com lente objetiva de 300 mm. Já para o método auditivo utilizou-se de gravação de vocalizações não identificadas em campo com o uso do gravador Sony ICD-PX312 eventualmente acoplado ao microfone unidirecional Yoga HT-81. Complementado por meio da utilização da técnica de playback, que consiste na simples reprodução da vocalização de uma espécie a fim de provocar a sua aproximação para fins de identificação.
Todas as espécies não reconhecidas em campo foram fotografadas e, ou tiveram sua vocalização registrada para posterior identificação por meio de bibliografia especializada (Gwynne et al., 2010) e comparação com o arquivo de vozes do Brasil (Vielliard 1995a; b). A classificação taxonômica seguiu Conselho Brasileiro de Registros Ornitológicos (CBRO, 2014).
O modelo utilizado para a definição das guildas tróficas das espécies de aves de cada uma das áreas estudadas foi classificado de acordo com os critérios e categorias definidos por Motta-Júnior (1990), a saber: (a) insetívoros (INS), dieta composta por ¾ ou mais de insetos e outros artrópodes; (b) onívoros (ONI), dieta composta por ¾ ou mais de insetos, artrópodes e frutos, em proporções similares; (c) frugívoros (FRU), dieta composta por ¾ ou mais de frutos e grãos ou sementes; (d) nectarívoros (NEC), dieta composta principalmente por néctar, mas também insetos e outros artrópodes; (e) carnívoros (CAR): dieta composta por ¾ ou mais de vertebrados vivos; (f) detritívoros (DET): dieta composta por ¾ ou mais de matéria orgânica em decomposição. Para a classificação das espécies foram utilizadas informações obtidas em literatura específica.
2.3 Métodos de análise do
estado de conservação das áreas estudadas
Foi avaliado o grau de degradação de cada área estudada, por meio de uma matriz de impactos proposta por Pereira (2003), adaptada por Santos e Vieira (2005). Para esta classificação, foram percorridos os mesmos transectos utilizados para a amostragem de aves, sendo observados os seguintes critérios: (i) intensidade do fogo; (ii) presença de rebanho bovino; (iii) extração vegetal (seletiva e corte raso) e mineral (rocha/solo e água) ; (iv) presença humana (provisória e permanente); (v) vias (trilha, estrada de terra e estrada pavimentada).
Para a caracterização qualitativa e quantitativa da vegetação das áreas estudadas utilizou-se o Método das Matrizes de Interação (Leopold et al., 1971). Esta matriz foi composta de linhas contendo os impactos avaliados, julgados como principais, aos quais os ambientes foram historicamente submetidos, e colunas contendo as três áreas estudadas. As interseções entre linhas e colunas foram divididas em quadrantes contendo pontuações (0 a 4) de avaliação de três características do impacto ambiental: quadrante 1 - severidade, quadrante 2 - espaço (extensão) e quadrante 3 - tempo (duração). O quadrante 4 continha a soma das pontuações dos outros três quadrantes, onde a área com maior valor total sugere maior degradação. As pontuações indicam: 0 - ausência do impacto, 1 – 1 até 25%, 2 – 26 até 50%, 3 – 51 até 75% e 4 – 76 até 100%.
2.4 Análise da dinâmica da paisagem
A quantificação estrutural da paisagem foi feita por meio de índices de composição e configuração espacial resultantes do software Fragstats® (Mcgarigal e Marks, 1995). A análise dos padrões espaciais da paisagem foi realizada pela conversão no Fragstats® de arquivos dos mapas categóricos de cobertura do solo, elaborados para 2013, em formato ASCII (American Standard Code for Information Interchange). A utilização de apenas um determinado conjunto de métricas, dentre várias centenas de índices e medidas existentes, é suficiente para se obter as interpretações ecológicas essenciais. Assim as métricas analisadas para este estudo podem ser agrupadas da seguinte maneira: métricas de área; métricas de forma; métricas de borda e área central; métricas do vizinho mais próximo (Metzger, 2006).
Na definição da cena de estudos e entrada no programa Fragstats, adotou-se como campo de trabalho, para cada área estudada, um retângulo de igual tamanho para todas as áreas, cujas dimensões foram de 3.500 × 3.500m (12,5km2 de área).
Dentre vários índices que o programa Fragstats calculou para os fragmentos e da paisagem circundante, nove foram selecionados para análise seguindo um critério de maior aplicabilidade aos objetivos do estudo. Foram eles: (1) área, (2) perímetro, (3) distância do vizinho mais próximo e (4) índice de proximidade entre as formações analisadas.
2.5 Análise da
riqueza de aves e das guildas tróficas
Para analisar
diretamente a similaridade e/ou dissimilaridade entre os locais amostrados foi
elaborado um diagrama de Venn, com base na presença e
ausência das espécies, e calculados índices de similaridade de Jaccard (Brower e Zar, 1984).
Para avaliar a similaridade das guildas tróficas das comunidades de aves entre
as diferentes áreas estudadas, foi utilizado o índice de Jaccard
(J) com base em dados qualitativos (presença e ausência). Para testar se a
riqueza de espécies e as guildas tróficas diferiram entre as diversas áreas foi
feita análise de variância (ANOVA) (Zar, 2010). Quando a ANOVA foi
significativa, o teste a posteriori de Tukey
foi utilizado para identificar quais guildas tróficas diferiram entre as áreas
estudadas. As análises estatísticas foram realizadas no programa PAST (PAleontological STatistics),
versão 2.15 (Hammer et al., 2001).
3. Resultados
A análise revela que o número e a densidade de fragmentos de Floresta Estacional Semidecidual do BL e a proximidade dos mesmos em relação a outros fragmentos presentes no local é maior do que se comparado às demais áreas. Da mesma forma, a área de campo rupestre dessa área, ainda que aparentemente mais degradada que as outras, foi consideravelmente maior. Para o PF, observou-se que as áreas de afloramentos rochosos e a proximidade das mesmas com outros afloramentos foram maiores, apesar da elevada concentração de formações do tipo campo limpo úmido na área. Embora a presença característica de espécies típicas de campos rupestres seja evidente, a área ainda apresentou um número de fragmentos de Florestas Estacionais Semideciduais maior que o RP. Com relação ao RP, observou-se um padrão intermediário entre as duas outras áreas descritas. Neste local, encontramos poucas áreas de afloramento rochoso, entretanto as mesmas são muito próximas entre si, além de Florestas Estacionais Semideciduais mais distantes entre si e de considerável densidade. As áreas de campos rupestres, do mesmo modo que no BL, encontram-se bem representadas e apresentam menores distâncias entre as formações semelhantes mais próximas. Contudo, a análise da dinâmica da paisagem pouco nos diz se não considerarmos a matriz de impacto.
De acordo com a matriz de impactos (Tabela 1), constatou-se que BL foi a área estudada que mais se encontra degradada. Observou-se que a presença humana permanente, a extração vegetal e mineral, as vias pavimentadas, o gado e o fogo nessa área são eventos antrópicos que mais causam impactos no local, somando 61 dos 80 pontos registrados nesta área. No caso da extração mineral realizada no BL, acredita-se que na maioria das vezes a mesma foi efetuada de forma ilegal por meio de artifícios que provocam alto impacto ambiental, como explosivos e máquinas de dragagem de sólidos. Em algumas visitas na área, ouviram-se explosivos sendo detonados, ainda que em uma distância considerável do transecto.
Tabela 1.
Matriz de impactos das áreas amostradas
durante o período de Novembro de 2011 a Janeiro de
2013: RP (Parque Estadual do Rio Preto); PF (Manancial APA Pau-de-Fruta); BL
(Parque Estadual do Biribiri e antigo depósito de
lixo de Diamantina/MG).
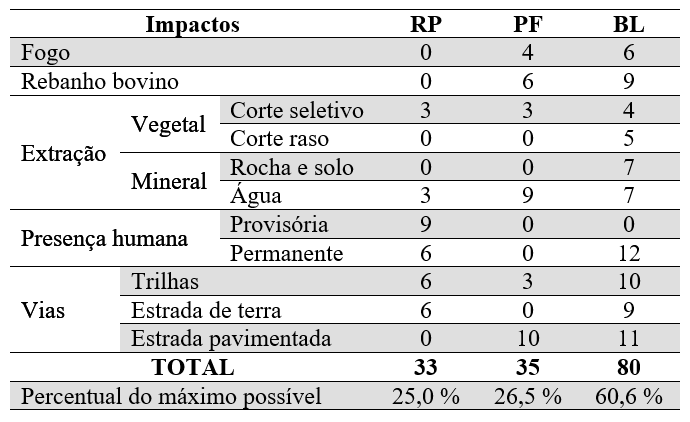 Fonte: Elaboração própria
Fonte: Elaboração própria
Para a área RP, os eventos mais impactantes foram à presença humana (provisória e permanente) e as vias (trilhas e estradas de terra), as quais somaram 27 dos 33 pontos registrados. Devido aos atrativos turísticos encontrados nesse Parque, durante todo ano o mesmo recebe visitas frequentes de pesquisadores e turistas, o que pode agravar ainda mais o estado de conservação dos ambientes ali encontrados.
Para o PF foi observada durante todo período de estudo uma elevada extração de água devido à presença de um dos mananciais que abastecem a cidade de Diamantina, sendo esta atividade realizada pela COPASA (Companhia de Saneamento de Minas Gerais). Em frente a essa área de estudo passa uma das rodovias mais importantes do norte de MG (BR 367), outro fator que pode colaborar para o aumento de impactos diversos como atropelamento de animais selvagens e poluição na área. Estes dois fatores somados representam 19 dos 35 pontos registrados para o local.
Notou-se a existência de algumas residências no RP e BL. No primeiro, as residências têm uma finalidade logística, de apoio a pesquisadores, turistas e funcionários residentes no local. Já no segundo, as residências são particulares e caracterizadas por plantios de espécies exóticas.
Não foi evidenciada a presença de erosões e voçorocas no RP e nem no PF, porém, no BL notou-se a ocorrência desse tipo de impacto em aproximadamente 50% da área amostrada. Em alguns locais, como na Cascalheira (uma das áreas amostradas no BL), existem iniciativas de programas de recuperação das áreas degradadas por parte de estudantes e professores da Universidade Federal dos Vales do Jequitinhonha e Mucuri (UFVJM).
Foi observado apenas no BL que algumas árvores foram cortadas de forma planejada, o que sugere um tipo de impacto aqui denominado como corte raso da vegetação, sendo caracterizadas por marcas de machado e motosserra em algumas árvores de maior porte. Considerando que o pior cenário de impactos possível, no qual todos os critérios estão com a maior pontuação alcançávelsome 132, o RP atingiu 25% (33 pontos), o PF 26,5 % (35 pontos) e o BL 60,6 % (80 pontos).
Foram amostradas 123 espécies de aves no trecho BL, 88 espécies em RP e 76 espécies em PF. Houve um padrão consistente nas três áreas para as guildas alimentares, a saber Insetívoros, Frugívoros e Onívoros (Tabela 2). As demais categorias alimentares foram representadas em menores proporções. Esta tendência se manteve em ambas as estações.
Tabela 2. Distribuição das
guildas tróficas das áreas amostradas durante as estações seca e chuvosa para o
período de Novembro de 2011 a Janeiro de 2013: RP
(Parque Estadual do Rio Preto/MG); PF (Manancial APA Pau-de-Fruta/MG); BL
(Parque Estadual do Biribiri e antigo depósito de
lixo de Diamantina/MG).
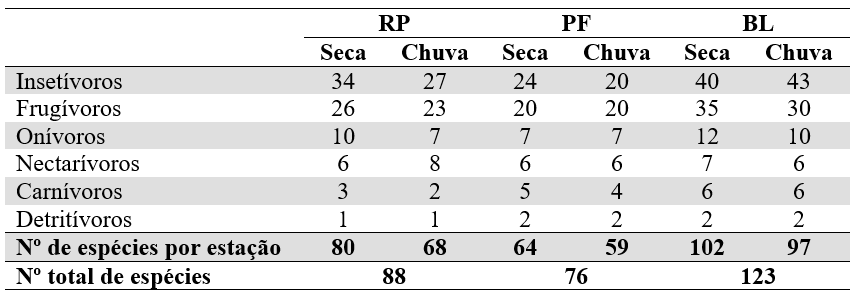 Fonte: Elaboração própria.
Fonte: Elaboração própria.
Para a estrutura trófica não houve diferenças significativas entre as áreas estudadas tanto para todo o período analisado (H = 5,670; p = 0,127), como para as duas estações seca (H = 5,436; p= 0,145) e chuvosa (H = 4,744; p = 0,191). A insetivoria foi a categoria alimentar predominante durante as duas estações nas três áreas, seguida pelas aves frugívoras e logo após onívoras. Entretanto, durante a estação seca houve um aumento de espécies onívoras em duas das três áreas estudadas, sendo elas BL e RP.
Ao longo do período amostral houve flutuação no número de espécies de aves entre as guildas tróficas predominantes nas três áreas de estudo. As guildas insetívora e frugívora sofreram variações durante todo o período, independente das estações, sendo uma das categorias mais evidente do que outra ou com padrões bastante próximos em determinado período de amostragem.
Com relação à similaridade, o diagrama de Venn (Figura 2) mostra que 41 espécies são comuns aos três ambientes amostrados. Entre elas, podemos citar o emberezídeo Zonotrichia capensis e o icterídeo Molothrus bonariensis, ambos considerados relativamente comuns durante o período de estudo. Quando considerado cada local amostrado, 37 espécies são exclusivas de BL, 22 de RP e apenas sete de PF. Nas comparações entre as áreas, 21 espécies são comuns ao RP e BL, 24 ao PF e BL e finalmente apenas quatro comuns ao RP e PF. Com relação ao índice de similaridade de Jaccard, houve maior similaridade da comunidade de aves entre BL-PF (48,51), seguido por RP- BL (41,61) e por fim PF- RP (37,82). A similaridade entre as estações seca e chuvosa foi bastante próxima nas três áreas estudadas. O índice de Jaccard aponta que 68,18% da comunidade de aves é semelhante entre as estações para o RP, 66,22% para o PF e 64,22% para o BL (Figura 2).
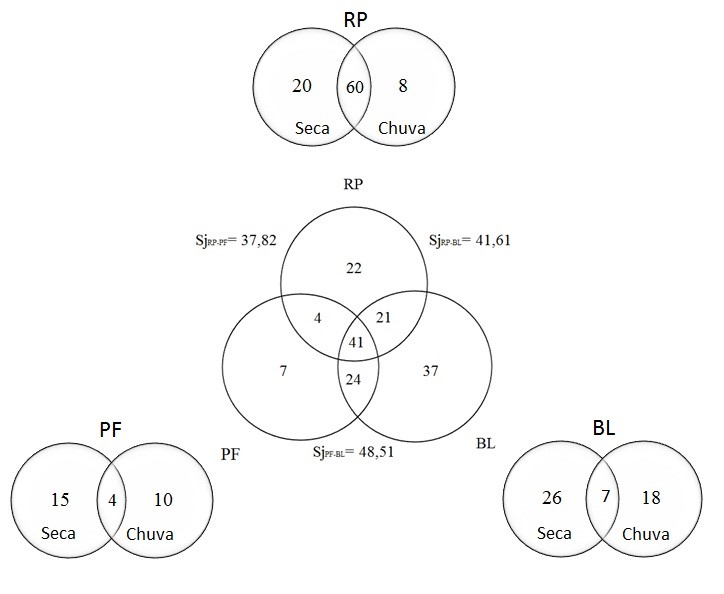 Figura 2.
Diagramas de Venn mostrando a similaridade das avifauanas dos locais estudados com os devidos valores de
similaridade de Jaccard (cento) e em cada local
estudado em relação às estações seca e chuvosa. RP = Parque Estadual do Rio
Preto; PF = Manancial APA Pau-de-Fruta; BL = Parque Estadual do Biribiri e Antigo depósito de lixo de Diamantina.
Fonte: Elaboração própria
Figura 2.
Diagramas de Venn mostrando a similaridade das avifauanas dos locais estudados com os devidos valores de
similaridade de Jaccard (cento) e em cada local
estudado em relação às estações seca e chuvosa. RP = Parque Estadual do Rio
Preto; PF = Manancial APA Pau-de-Fruta; BL = Parque Estadual do Biribiri e Antigo depósito de lixo de Diamantina.
Fonte: Elaboração própria
4. Discussão
O crescimento demográfico e a ocupação de áreas pelas atividades agropecuárias, mineradoras e urbanas afetam drasticamente na composição e estrutura de diversos grupos faunísticos (Ganem e Drummond, 2011). Para duas das áreas amostradas BL e PF foram evidenciados a ação da pressão destas atividades. Sendo no BL a expansão da Universidade Federal dos Vales do Jequitinhonha e Mucuri (UFVJM), associada aos distúrbios passados realizados no Parque Estadual do Biribiri, bem como as ações de deposição de lixo as principais causas. Já no PF, embora em menor intensidade, em decorrência do crescimento urbano de Diamantina. Enquanto que no RP, por se tratar de unidade de conservação de proteção integral, e durante o trabalho estar fechada à visitação pública, foram evidenciados o menor número de impactos sobre a avifauna. Supressão da vegetação original, redução das áreas remanescentes, extração de recursos minerais (solo, rocha, água) e naturais (lenha, flores, frutos, caça) estão entre os principais impactos identificados nas áreas de estudo.
A supressão da vegetação pode empobrecer a fauna de insetos e reduzir alguns micro-habitatsimportantes, afetando as aves insetívoras (Sodhi et al., 2004). Além disso, este processo pode levar a fragmentação de ambientes, fenômeno amplamente distribuído e associado à expansão de fronteiras de desenvolvimento humano (Viana et al., 1997). São vários os trabalhos que abordam os efeitos da fragmentação florestal sobre as comunidades de aves (Gimenes e Anjos, 2003). Os resultados obtidos nesses estudos têm variado consideravelmente, o que segundo Restrepo et al. (1997), provavelmente reflete a complexa relação entre a modificação do habitat e a perda da biodiversidade.
Em seu estudo avaliando os efeitos da exploração de madeira sobre a comunidade de aves em uma floresta do Pará, Henriques et al. (2008) observaram que o procedimento de ordenação demonstrou que a similaridade entre as amostras diminuiu após a exploração madeireira em relação à similaridade observada entre as amostras do período de pré-exploração. Isto indica que apesar das diferenças existentes na composição da comunidade e na abundância de algumas espécies de aves entre as parcelas localizadas em floresta controle e em floresta manejada no período anterior a exploração, essas diferenças foram aprofundadas em decorrência da exploração madeireira. Outros estudos têm demonstrado que entre 14% (Johns, 1996) e 61% (Thiollay, 1992) da avifauna identificada em uma área podem ser significativamente afetadas pela exploração madeireira. Frugívoros tendem a ser mais resilientes aos efeitos da exploração madeireira do que insetívoros (Guilherme e Cintra, 2001). Eles são adaptados para forragear sobre recursos que estão amplamente distribuídos, muitas vezes de maneira disjunta, e que são frequentemente disponíveis durante um tempo limitado (Levey, 1988). Portanto, essas espécies são relativamente mais hábeis em explorar os ambientes criados pela exploração madeireira (Mason e Thiollay, 2001).
O histórico de distúrbios de cada área auxilia a compreender os padrões encontrados neste trabalho. No caso do BL, antes de 2005, o antigo depósito de lixo estava em pleno funcionamento e a rodovia MG 367 que leva até o norte de MG possuía trechos de estrada de terra o que a tornava de baixo fluxo de veículos. A atividade de extração de minerais da cascalheira, um dos locais visitados nesse estudo, estava inativa desde a década de 50. A partir do ano de 2005, iniciou-se a construção dos prédios da Universidade, o antigo depósito de lixo foi desativado, e reiniciou o processo de extração da cascalheira (que durou apenas um ano) e a rodovia MG 367, aumentou consideravelmente o fluxo. As demais áreas (PF e RP) apresentam um histórico de distúrbio menos intenso e impactante. O PF continua enfrenando os mesmos problemas com as queimadas desde o seu reconhecimento como área de proteção ambiental. Contudo de alguns anos até o presente, houve um aumento do fluxo na rodovia que margeia a área, além das constantes pressões urbanas devido a sua proximidade com Diamantina. Já o RP, sendo um Parque relativamente bem monitorado (controle de queimadas e do turismo, excelente infraestrutura e funcionários bem treinados), tem seu impacto basicamente concentrado na visitação, que em algumas épocas do ano pode ir além da que o ambiente pode suportar (Silva, 2005).
Muitos dos incêndios que ocorrem nos ambientes campestres dos topos de montanha do leste do Brasil, também foram observados nas três áreas estudadas. Estes são causados por turistas que acampam nessas áreas, por criadores de gado que possuem pastagens nas adjacências ou por ex-proprietários, descontentes por não terem sido pagos por suas terras desapropriadas pela criação de reservas (Ribeiro, 2006). As modificações ambientais causadas pelo fogo nos campos rupestres incluem o empobrecimento da flora nativa, facilitando a ocorrência de espécies de plantas invasoras que competem por espaço e luz com as espécies nativas e endêmicas (Vasconcelos et al., 2002). De acordo com Metzger (2010), é desejável que sejam mantidos entre 60 a 70% do habitat original para que a paisagem tenha uma estrutura adequada para fins de conservação, atendendo ao limiar de percolação.
O RP atua como refúgio para espécies endêmicas e ameaçadas de extinção, além disso, alguns dos habitats encontrados nesta área estão se tornando cada vez mais raros na região do Cerrado brasileiro, como os campos rupestres, as matas ciliares, que margeiam o Rio Preto e as cachoeiras. Entretanto, é possível que ocorra em alguns momentos de intensa visitação turística, a qual pode desencadear um processo de defaunação nos pontos mais atrativos, conforme observado em outros trabalhos (Pivatto e Sabino, 2007). Contudo este efeito não foi observado neste estudo, devido ao fato do RP ter permanecido fechado a visitação pública durante toda a realização deste estudo.
Para as áreas estudadas houve um predomínio de espécies insetívoras na estrutura trófica da avifauna nos três ambientes estudados, padrão semelhante ao sugerido por Sick (1997), como modelo para a região Neotropical. Resultado corroborado por Pivatto e Sabino (2007) em uma área de cerrado sul-matogrossense e Vieira et al. (2013) analisando a estrutura trófica de quatro fitofisionomias de Cerrado no Parque Estadual da Serra Azul, no Mato Grosso. De acordo com Sekercioglu et al. (2002), aves insetívoras são mais susceptíveis às mudanças ambientais bruscas, devendo mover para outras áreas à procura de insetos, quando estes se tornam escassos. Ao longo do período amostral ocorreram diversas flutuações na riqueza de aves nos três ambientes amostrados, tanto para as áreas mais abertas como o PF, como para as florestais (RP e BL), contudo as aves insetívoras permaneceram como as de maior riqueza.
Oliveira e Frizas (2008) observaram em seu estudo que a comunidade de insetos apresenta um padrão de sazonalidade na distribuição destes ao longo do ano, havendo uma maior proporção de coleta na estação chuvosa (81,1%). A sazonalidade na distribuição e a abundância de insetos são um fenômeno relativamente bem conhecido, sendo particularmente importante para sistemas neotropicais onde a sazonalidade é determinada pelo contraste de períodos de seca e chuva. No início da estação chuvosa ocorre um aumento na produção de folhas e ramos novos, recurso importante para insetos, consequentemente afeta a riqueza e distribuição de aves insetívoras, conforme observado.
Para as aves frugívoras, a menor riqueza geral e as flutuações observadas podem estar relacionadas a dois fatores, não excludentes. O primeiro relacionado ao estado de degradação e da paisagem local, onde as alterações ambientais nos locais amostrados podem ter favorecido a uma tendência ao aumento de aves onívoras e possivelmente de insetívoras menos especializadas e um decréscimo de frugívoros e insetívoros mais especializados.
Outro fator pode estar relacionado é a variação no padrão fenológico das espécies vegetais, na qual a disponibilidade de frutos, sementes e flores pode influenciar diretamente a presença destes em um determinado local ou estação, uma vez em que a maior oferta de frutos carnosos ocorre no final da estação chuvosa (Oliveira, 2008). A relativa escassez de frutos em determinadas épocas do ano pode obrigar os frugívoros a alterar a dieta ou realizar deslocamentos em busca de novas áreas de alimentação. Vieira et al. (2013), também observaram que no fim da estação chuvosa, as aves frugívoras apresentaram um predomínio momentâneo sobre as insetívoras.
Pertencente às espécies frugívoras, o subgrupo das granívoras, composto por indivíduos da família Emberizidae, ocorreram predominantemente em áreas abertas de forma independente da sazonalidade climática (Vieira et al., 2013). Em formações naturais, como os campos rupestres, sujos e limpos, a maior disponibilidade de sementes ocorre no período seco, como o observado nas áreas abertas das áreas de estudo. Contudo em áreas de invasão de gramíneas exóticas e ecossistemas agropecuários ativos, como os encontrados no BL, a disponibilidade de grãos provavelmente favoreceram a ocupação e manutenção de aves granívoras no local.
O bioma Cerrado apresenta marcada sazonalidade climática, com efeitos sobre o regime das chuvas, o qual altera a disponibilidade de água e nutrientes no solo, com impactos diretos no desenvolvimento das plantas e sua fenologia (Oliveira, 2008). Nos períodos de seca a oferta de recursos tanto para frugívoros como para insetívoros é reduzida, assim muitas espécies tendem a se deslocar para habitats mais favoráveis e estáveis, em busca de alimento, como matas ciliares. Neste sentido os locais com maior proporção de ambientes ripários, como RP e BL, propiciam maior riqueza e permanência da avifauna independente da sazonalidade climática.
Willis (1976) afirmou que espécies que possuem disponibilidade de alimento durante o ano inteiro, como as insetívoras, ou onívoras que utilizam técnicas alimentares variadas e podem utilizar o alimento de acordo com as condições oferecidas, tendem a predominar em um determinado ambiente, assim com encontrado em todas as áreas amostradas.
Espécies onívoras não requerem sítios específicos de forrageamento (Motta-Júnior, 1990), sendo a terceira categoria trófica mais representativa em todas as áreas amostradas, independentemente da proporção de formações abertas ou florestais encontrada em cada local. O predomínio de espécies onívoras em um dado ambiente pode ser indicativo de área alterada e de fragmentos menores. Conforme verificado neste estudo, no qual BL que possui maior redução da vegetação original e elevado grau de antropização, quando comparada com as demais áreas, apresentou maior riqueza desta guilda em ambas estações (cerca de 17% a mais na estação seca e 30% na chuvosa).
A ausência de flutuações nos padrões de riqueza das espécies de nectarívoras, reflete o perfil fenológico das espécies vegetais da região estudada, onde o recurso floral está disponível tanto nas formações abertas como florestais ao longo de todo o ano (Carrara et al., 2013).
Em relação as demais guildas tróficas, as aves carnívoras e detritívoras estiveram pouco representadas assim como observado por Carrara et al. (2013) e Vieira et al. (2013). A baixa representatividade destas guildas deve-se ao fato de possuírem dieta mais especializada e requererem ambientes abertos como principal habitat para alimentação (Motta-Júnior, 1990). Outra razão é a difícil visualização em áreas mais fechadas, o que não se aplica a esse estudo devido às florestas dos locais amostrados possuírem árvores mais baixas comparando-se as da floresta Atlântica ou Amazônia. A baixa riqueza de aves carnívoras e detritívoras nas áreas de estudo pode estar relacionada à alta sensibilidade à presença humana e animal, possuindo um sistema de alerta mais aguçado quando detectam qualquer sinal de uma possível ameaça ou predador (Aleixo, 1999).
Os padrões de riqueza, similaridade e estrutura trófica refletiram a tendência observada da estrutura da paisagem e da vegetação, onde locais com maior proporção das áreas florestais (BL e RP) apresentaram maior afinidade, se comparado com aquele de maior quantidade de habitats abertos (PF), em detrimento ao estado de degradação observado para as áreas de estudo. Contudo a relativa elevada riqueza no BL, ambiente de maior degradação, pode estar associada ao fato de algumas espécies, ditas oportunistas, como Thamnophilus doliatus, encontrada neste estudo, mudarem a composição de sua dieta em ambientes alterados (Poulin et al., 1994). Corroborando com esta tendência, Silva (1986) indica que ambientes perturbados propiciam uma dieta mais variada, possibilitando assim maior riqueza nestes ambientes.
O número e tamanho das formações florestais pode ter sido outro fator responsável pela maior ou menor similaridade da comunidade de aves entre as áreas, conforme já observado por outros autores (Athiê e Dias, 2012). O PF por se tratar de uma área na qual a fitofisionomia de campo rupestre é marcante e possuir pequenos capões de mata, pode não possuir habitats suficientes para a persistência de populações de determinadas espécies, apresentando características mais homogêneas em relação às duas outras áreas estudadas. Para áreas abertas, Ausden (2004) sugere que em virtude da simplificação do ambiente, há uma redução na disponibilidade de atrativos para as aves, sobretudo abrigo, alimento e locais para a nidificação.
A paisagem dos locais estudados é composta por um mosaico de diferentes níveis de heterogeneidade formado por unidades com algum grau de interação. A heterogeneidade de cada área é determinada por características do ambiente físico (geomorfologia, solo, umidade, estrutura da vegetação) e pelo regime de perturbações, naturais ou antrópicas (fogo, desmatamento, extrativismo, estradas, visitação turística). Neste contexto o gradiente de heterogeneidade das paisagens, associado aos demais fatores citados anteriormente, reflete também o de riqueza (BL-RP-PF). Assim, ainda que a matriz de impactos tenha apontado que o RP e PF estejam sofrendo menos impactos se comparados ao BL, a homogeneidade da vegetação desses locais, pode contribuir para a baixa riqueza relativa de espécies de aves.
5. Conclusão
De maneira geral, as áreas apresentam estado de conservação adequado. No entanto, em uma delas, o BL, registramos um maior grau de impacto ambiental. Apesar da situação conservacionista deste local estar muito aquém do desejado, é possível afirmar que as áreas comportam uma grande riqueza de aves distribuídas em seis guildas tróficas e ocupam diferentes hábitats, com destaque para espécies de sub-bosque, frugívoros florestais, espécies ameaçadas e endêmicas, o que demonstra a importância da conservação desses ambientes naturais para a manutenção de tais populações.
Duas hipóteses podem elucidar os padrões encontrados, a saber: 1) apesar de certas alterações da comunidade de aves, sobretudo no BL, os efeitos resultantes das ações antrópicas não parecem ainda ser evidentes para a avifauna das áreas amostradas. Se considerarmos a estrutura trófica, é possível perceber que a mesma se comporta de modo equilibrado, com a presença de espécies de aves como predadores de topo de cadeia e grandes frugívoros; 2) os dados sugerem que em ambientes savânicos, que são naturalmente fragmentados, o grupo aves apresenta uma maior resiliência aos ambientes antropizados se comparados às formações florestais. Isso ocorre uma vez que nestas a estrutura trófica predominante baseia-se em frugívoros, residentes e dependentes das florestas, enquanto que em nosso estudo a estrutura trófica predominante foia dos insetívoros, independentemente do local ou estação. Assim os padrões encontrados por este estudo reforçam a necessidade melhor compreensão de ambientes antropizados, principalmente aqueles em áreas de formações savânicas, onde a avifauna indica uma tendência a apresentar maior plasticidade e amplitude ambiental.
Agradecimentos
O presente trabalho foi realizado com apoio da
Coordenação de Aperfeiçoamento de Pessoal de Nível Superior – Brasil (CAPES) -
Código de Financiamento 001. Ao IEF, a licença concedida e a todos os
funcionários do Parque Estadual do Rio Preto (PERP) e do Parque Estadual do Biribiri (PEBi).
Referências
Abreu Filho, A. P. ; Costa, C. R. ; Gomes, I.R. ; Viana, A. J. S. ; Tassinari, D. ; Vidal-Torrado, P. ; Silva, A. C. (2021). Os solos e a evolução de paisagens na Serra do Espinhaço Meridional, Brasil. Revista Espinhaço,10(1).
Aleixo A. (1999). Effects of selective logging on a bird community in the Brazilian Atlantic Forest. Condor, 101, p.537-548.
Almeida-Abreu P.A. (1996). O Caminho das Pedras. Geonomos, v.4, n.1, p.77-93.
Andrade M.A. (1997). Aves Silvestres de Minas Gerais. Belo Horizonte: CIPA.
Athiê S.; Dias M.M. (2012). Frugivoria por aves em um mosaico de Floresta Estacional Semidecidual e reflorestamento misto em Rio Claro, São Paulo, Brasil. Acta Botânica Brasileira, 26(1), p.84-93.
Ausden M. (2004). Habitat management. In: Sutherland WJ.; Newton I.; Green RE. (eds.). Bird Ecology and Conservation – A handbook of techniques. Techniques in Ecology & Conservation Series, Oxford University Press, Oxford, USA, p.329-369.
Brower J.E.; Zar J.H. (1984). Field & laboratory methods for general ecology. 2 ed. Wm. C. Brown Publishers, Dubuque, Iowa, 226p.
Campos J.R.R. (2009). Caracterização, mapeamento, volume de água e estoque de carbono da turfeira da Área de Proteção Ambiental Pau-de-Fruta, Diamantina/MG. Dissertação de Mestrado. UFVJM/MG.
Carrara LA.; Faria LCP.; Garcia FI.; Antas PTZ. (2013). Avifauna da Estação Ecológica Estadual de Acauã e chapadas do alto do vale do rio Jequitinhonha: ecótono de três biomas em Minas Gerais. Ornithologia, 5(2), p.58-77.
CBRO - Comitê Brasileiro de Registros Ornitológicos. (2014) Lista das Aves do Brasil, 11ª Edição, 1/1/2014. http://www.cbro.org.br. Acesso em: 04/01/2014.
Foresto E.B. (2008). Levantamento florístico dos estratos arbustivo e arbóreo de uma mata de galeria em meio a campos rupestres no Parque Estadual do Rio Preto, São Gonçalo do Rio Preto. Dissertação de Mestrado. USP/SP.
Franchin A.G. (2009). Avifauna em áreas urbanas brasileiras, com ênfase em cidades do Triângulo Mineiro/Alto Paranaíba. Tese de Doutorado. UFU/MG.
Franchin A.G.; Juliano R.F.; Kanegae M.F.; Marçal Júnior O. (2008). Birds in the Tropical Savannas. In: Del Claro K.; Oliveira PS.; Rico-Gray V.; Barbosa AAA.; Bonet A. (eds.) International Commission on Tropical Biology and Natural Resources in Encyclopedia of Life Support Systems (EOLSS), Developed under the Auspices of the UNESCO, Eolss Publishers, Oxford, UK.
Furness R.W.; Greenwood J.J. (1993). Birds as monitors of environmental change. Chapman & Hall, London.
Ganem R.S.; Drummond J.A. (2011). Biologia da Conservação: As bases científicas da proteção da biodiversidade. In: Ganem RS. (org.) Conservação da Biodiversidade, Legislação e Políticas Públicas.
Gimenes M.R.; Anjos L. (2003) Efeitos da fragmentação florestal sobre as comunidades de aves. Acta Scientiarum, Biological Sciences, 25(2), p.391-402.
Guilherme E.; Cintra R. (2001). Effects of intensity and age of selective logging and tree girdling on an understorey bird community composition in central Amazonia, Brazil. Ecotropica, 7, p.77-92.
Gwynne J.A.; Ridgely RS.; Tudor G.; Argel M. (2010). Aves do Brasil – Pantanal e Cerrado. Wildlife Conservation Society. Ed. Horizonte. 2010.
Hammer Ø.; Harper DAT.; Ryan PD. (2001). PAST: Palaeontological Statistics software package for education and data analysis. Palaeontologia Electronica, 4(1), p.9.
Henriques L.M.P.; Wunderle JR J.M.; Oren D.C.; Willig M.R. (2008). Efeitos da exploração madeireira de baixo impacto sobre a comunidade de aves de sub-bosque na Floresta Nacional do Tapajós, Pará, Brasil. Acta Amazonica, 38(2), p.267-290.
Horta A.; Dias B.; Santo C.V.E.; Costa CR.; Furlani C.; Hermann G.; et al. (orgs). (2002) Cerrado e Pantanal. p.175-214.
Johns A.G. (1996). Bird population persistence in Sabahan logging concessions. Biological Conservation, 75, p.3-10.
Leopold L.B.; Clarke F.E.; Hanshaw B.B.; Balsley R. (1971). A procedure for evaluating environmental impact; US Geological Circular 645 – N71 –36757; Washington: DC, US Dept. of the Interiore; Geol. Survey. In: Conservation of Natural Resources.
Levey D.J. (1988). Spatial and temporal variation in Costa Rican fruit and fruit-eating bird abundance. Ecological Monographs, 58, p.251-269.
Marques I.C. (2012). Uso de composto orgânico e espécies do cerrado na revegetação de área remanescente da extração de cascalho em Diamantina/MG. Dissertação de Mestrado. UFVJM/MG.
Mason D.; Thiollay J.M. (2001). Tropical forestry and the conservation of Neotropical birds. p. 167-191.
Mcgarigal K.; Marks B.J. (1995). Fragstats: spatial patterns analysis program for quantifiying landscape structure. Portland: USDA, Forest Service, Pacific Northwest Research Station, 122p.
Metzger J.P. (2010). O código florestal tem base científica? Natureza & Conservação, 8(1), p. 1-5.
Metzger J.P.; Alves L.F.; Goulart G.; Teixeira A.M.G.; Simões S.J.C.; Catharino E.L.M. (2006). Uma área de relevante interesse biológico, porém pouco conhecida: a Reserva Florestal do Morro Grande. Biota Neotropica, 6(2).
Motta-júnior J.C. (1990). Estrutura trófica e composição das avifaunas de três ambientes terrestres na região central do estado de São Paulo. Ararajuba, 1, p.65-71.
Myers N.; Mittermeier R.A.; Mittermeier C.G.; Fonseca G.A.B.; Kent J. Biodiversity hotspots for conservation priorities. Nature, 403, p.853-858.
Neves S.C.; Abreu P.A.A.; Fraga L.M.S. (2005). Fisiografia, In: Silva AC.; Pedreira L.C.V.S.F.; Abreu P.A.A. Serra do Espinhaço Meridional, Paisagens e Ambientes. Belo Horizonte: O Lutador: 47-58.
Oliveira CM.; Frizzas M.R. (2008). Insetos de Cerrado: distribuição estacional e abundância. Boletim de Pesquisa e Desenvolvimento, 216, p.1-26.
Oliveira P.E.A.M. (2008). Fenologia e biologia reprodutiva das espécies de Cerrado, p. 273-290, vol. 1. Brasília/DF: Embrapa Cerrados.
Pereira J.A.A. (2003). Efeitos dos impactos ambientais e da heterogeneidade ambiental sobre a diversidade e estrutura da comunidade arbórea de 20 fragmentos de florestas semidecíduas da região do Alto Rio Grande, Minas Gerais. 156 p. Tese de Doutorado. UFMG/MG.
Piratelli A.J.; Pereira M.R. (2002). Dieta de aves na região leste de Mato Grosso do Sul. Ararajuba, v.10, n.2, p.131-139.
Pivatto M.A.C.; Sabino J. (2007). O turismo de observação de aves do Brasil: breve revisão bibliográfica e novas perspectivas. Atualidades Ornitológicas, 139, p.10-13.
Poulin B.; Lefebvre G.; Mcneil R. (1994). Characteristics of feeding guilds and variation in diets of bird species of three adjacent tropical sites. Biotropica, v.26, p.187-197.
Restrepo C.; Renjifo L.M.; Marples P. (1997). Frugivorous birds in fragmentedneotropical montane forests: landscape pattern and body mass distribution. Chicago: The University of Chicago Press,12: 171-189.
Ribeiro K.T. (2006). Quem causa os incêndios florestais – o tempo seco ou o fósforo aceso? Disponível em: . Acesso em: 03/07/2013.
Santos R.M.; Vieira FA. (2005). Análise estrutural do componente arbóreo de três áreas de Cerrado em diferentes estádios de conservação no município de Três Marias, Minas Gerais, Brasil. Revista Cerne, 4(11), p.399-408.
Sekercioglu C.H.; Ehrlich PR.; Daily G.C.; Aygen D.; Goehring D.; Sandí R.F. (2002). Disappearance ofinsectivorous birds from tropical forest fragments. PNAS, 99, p.263-267.
Sick H. (1997). Ornitologia brasileira. Edição revista e ampliada por José Fernando Pacheco. Editora Nova Fronteira, Rio de Janeiro.
Silva A.C. (2005). Solos. In: Silva AC.; Pedreira LCVSF.; Almeida Abreu PA. Serra do Espinhaço Meridional: Paisagens e Ambientes. Belo Horizonte: O Lutador: 50-78.
Silva J.M.C. (1986). Estrutura trófica e distribuição ecológicada avifauna de uma floresta de terra firme na Serra dos Carajás, estado do Pará. Em: Congresso Brasileiro de Zoologia, 13, Cuiabá. Resumos, Cuiabá: Universidade Federal de Mato Grosso. 189p.
Sodhi N.S.; Koh L.P.; Brook B.W.; NG P.K.L. (2004). Southeast Asian biodiversity: an impending disaster. Trends Ecology Evololution, 19, p.654–660.
Thiollay JM. (1992). Influence of selective logging on bird species diversity in a Guianan rain forest. Conservation Biology, 6, p.47-63.
Vasconcelos M.F. (2008). Mountaintop endemism in eastern Brazil: why some bird species from campos rupestres of the Espinhaço Range are not endemic to the Cerrado region? Revista Brasileira de Ornitologia, 16(4), p. 348–362.
Vasconcelos M.F.; D’angelo-Neto S.; Rodrigues M. (2002). A range extension for the Cipó Canastero Asthenes luizae and the consequences for its conservation status. Bulletin of the British Ornithologists’ Club, 122, p.7-10.
Viana V.M.; Tabanez A.A.J.; Batista J.L.F. (1997). Dynamics and restoration of forest fragments in the Brazilian Atlantic moist Forest. In: Laurance WF.; Bierregard RO. (eds). Tropical forest remnants: ecology management and conservation of fragmented communities. Chicago: University of Chicago Press. p. 351-365.
Vieira F.M.; Purificação K.N.; Castilho L.S.; Pascotto M.C. (2013). Estrutura trófica da avifauna de quatro fitofisionomias de Cerrado no Parque Estadual da Serra Azul. Ornithologia, 5(2), p. 43-57.
Vielliard J.M. (1995a). Canto de aves do Brasil. Campinas, Sociedade Brasileira de Ornitologia, CD.
Vielliard J.M. (1995b). Guia sonoro das aves do Brasil. Campinas, Sociedade Brasileira de Ornitologia, Fundação O Boticário de Proteção à Natureza, CD 1.
Villanueva R.E.V.; Silva M. (1996). Organização trófica da avifauna do Campus da Universidade Federal de Santa Catarina (UFSC), Florianópolis, SC. Biotemas, 9(2), p. 57-69.
Willis E.O. (1976). Effects of a cold wave on an Amazonian avifauna in the upper Paraguay drainage, western Mato Grosso, and suggestions on Oscine-Suboscine relationships. Acta Amazônica, 6, p. 379-394.
Zar J.H. (2010). Biostatistical Analysis. 5nded. New Jersey, Prentice-Hall, 944p.








