

Simulando la dinámica de transmisión de pacientes coinfectados con la Covid-19 y dengue
Observador del Conocimiento, vol.. volumen 5, núm. 3, 2020
Observatorio Nacional de Ciencia, Tecnología e Innovación


Artículos de Investigación
Recepción: 28 Junio 2020
Aprobación: 22 Julio 2020
Resumen: Recientemente se han detectado pacientes infectados por la Covid-19 y con dengue en Tailandia y Singapur al mismo tiempo (coinfectados), y por tanto, se deben comenzar a diseñar medidas preventivas para el monitoreo de estos casos especiales en Latinoamérica. A raíz de ello, se presenta un modelo matemático que permite analizar este tipo de coinfección en la población humana. Finalmente, se resuelve analítica y numéricamente el modelo.
Palabras clave: Covid-19, coexistencia, dengue, Latinoamérica, Tailandia, Singapur.
Abstract: Patients infected with Covid-19 and with Dengue have been detected in Thailand and Singapore at the same time (coinfected), it is necessary to monitor these cases in Latin America. For that reason we present a mathematical model that allows analyzing this type of coinfection in the human population. Finally, the model is analytically and numerically resolved according to a possible scenario in a given country.
Keywords: Covid-19, coinfected, dengue, Latin America, Thailand, Singapore.
Simulando la dinámica de transmisión de pacientes coinfectados con la Covid-19 y dengue
Introducción
A lo largo de la historia humana se han registrado diversos pacientes infectados con dos o más infecciones al mismo tiempo. Este proceso es conocido como coinfección, observado en pacientes con HIV y Tuberculosis, HIV y hepatitis, dengue y chikungunya, entre otros más.
Recientemente se publicaron tres casos que presentan dengue y Covid-19 al mismo tiempo en Tailandia y Singapur (Yan, G. et, al. y Joob, B., 2020). Dichas publicaciones lanzan una alerta sanitaria por un posible crecimiento de este tipo de brotes epidémicos en el mundo
Recordemos que la Organización Mundial de la Salud declaró a la Covid-19 como una nueva pandemia en marzo de 2020; y para el 6 de julio de este año se han registrado más de once millones de casos, superando la barrera de los quinientos mil muertos. En paralelo, se ha documentado que un tercio del planeta está en riesgo de contraer dengue, enfermedad que además presenta cuatro serotipos diferentes, y todos ellos circulando al mismo tiempo en Latinoamérica. Lamentablemente, ambas enfermedades carecen de una vacuna que ayude a minimizar su impacto en el mundo.
Asimismo, se debe señalar que en la literatura científica existen modelos generales para considerar coinfección, tales como el desarrollado por Ackleh and Allen (Ackleh, AS., 2003), posteriormente se generalizó con el tiempo [4, y ver todas las citas en dicho trabajo]. Sin embargo, no se ha considerado la Covid-19 en este tipo de abordaje matemático.
Finalmente, se presenta un modelo hipotético para ilustrar las posibles consecuencias de este tipo de coinfección a raíz de la posibilidad de que los asintomáticos por la Covid-19 puedan estar infectados con dengue.
Modelo matemático
Se propone un modelo del tipo compartimental basado en un esquema del tipo Susceptible-Infectado-Recuperado. Es un modelo ideal porque se considera únicamente un solo tipo de serotipo de dengue, y a su vez, se omite el hecho de que los pacientes se puedan volver a infectar con otro serotipo diferente. Asimismo, se ha considerado una tasa de muerte constante en el tiempo.
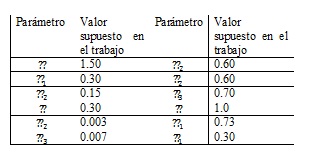
Toda la población es susceptible a contraer estas dos enfermedades (no hay inmunidad adquirida) y se denota como S(t), mientras que I1(t) y I2(t) representan a los pacientes infectados con dengue y Covid-19, respectivamente. I3(t) indican aquellos pacientes coinfectados por ambas enfermedades, y las personas recuperadas se simbolizan con R(t). Los parámetros y los valores considerados en el trabajo se muestran en la Tabla 1.
El sistema de ecuaciones diferenciales que se propone en el trabajo es el siguiente:
Cuya nomenclatura es la misma que se ha explicado en trabajos anteriores (Isea, 2020; Isea y Lonngren, 2018). La metodología para resolver este sistema de ecuaciones se ha publicado tanto analítica como numéricamente para la Covid-19 (Isea, 2020), así como en el caso del dengue ( Isea,2014; Isea y Lonngren, 2018), por lo que solo se van a indicar los resultados analíticos en el trabajo.
Discusión
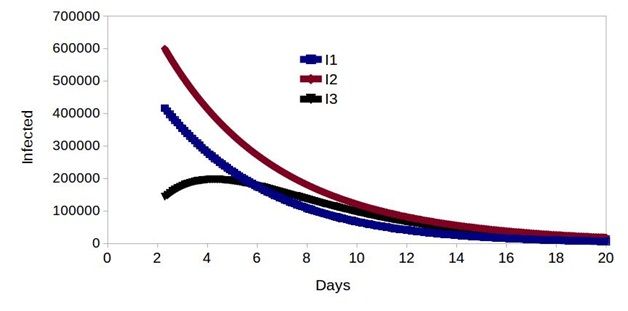
En la Figura 1 se muestra un caso hipotético donde se ha considerado un número máximos de casos de infección por dengue (color rojo), y por la Covid-19 (azul), tal que ambas enfermedades comienzan a descender en el tiempo. Sin embargo, se observa un máximo de contagios en aquellos pacientes en los que coexisten ambas enfermedades (color negro), probablemente causado por los pacientes asintomáticos con la Covid-19 que fueron infectados con dengue, aunque dicha conjetura se debe validar con datos reales.
Conclusiones
El trabajo presenta la dinámica de transmisión de pacientes coinfectados por dengue y con la Covid-19, empleando para ello un modelo del tipo compartimental. Este es preliminar, pero ilustra la complejidad de las soluciones encontradas analíticamente. Asimismo, se presenta la posibilidad de un crecimiento de casos de pacientes coinfectados por ambas enfermedades tras la pandemia por la Covid-19, a raíz de que los pacientes asintomáticos se pueden contagiar con dengue. Por ello, es necesario realizar pruebas moleculares que descarten la Covid-19 aunque el diagnóstico sea dengue.
Resultados
El sistema de ecuaciones diferenciales se resuelve de acuerdo al procedimiento descrito en (Isea, 2020; Isea y Lonngren, 2018).
El primer paso fue identificar tres puntos de equilibrio del sistema de ecuaciones:
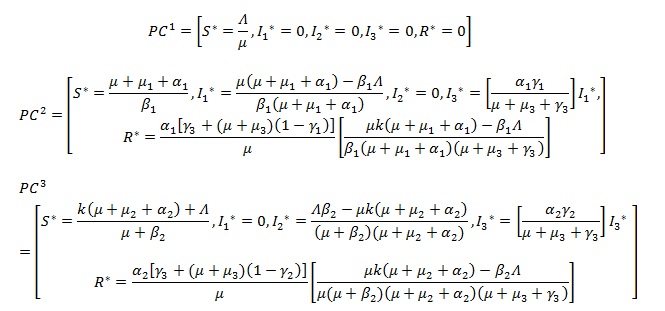
Existe un cuarto punto crítico, pero no se logró culminar dicha expresión para incluirla en el trabajo por la complejidad de la misma
El Jacobiano del sistema es
Finalmente, solo se logró determinar los autovalores de los dos primeros puntos críticos en vista de la complejidad de las expresiones anteriores, es decir, los autovalores para el primer punto son:
Mientras que los autovalores para el son:
De modo que la estabilidad del sistema dependerá de los valores de los parámetros obtenidos a partir de un ajuste por mínimos cuadrados cuando se dispongan de datos reales.
A modo de ejemplo, el primer punto crítico ( ) estaría ubicado en:
De acuerdo con los valores indicados en la Tabla 1. Este resultado muestra que la mayoría de las personas son susceptibles a contraer dichas enfermedades. Asimismo, es un punto de equilibrio no-endémico en vista de que los casos infectos son cero.
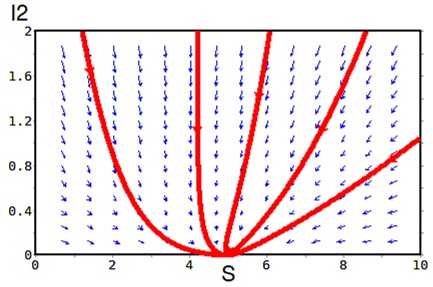
Los autovalores obtenidos tras evaluar el Jacobiano en dicho punto crítico son [-0.50, -0.10, -1.09, -0.30], es decir, todos los valores son negativos y por ende, es un punto de equilibrio como se puede apreciar en la figura 2 (al considerar I1=0).
Referencias
Yan G, Lee CK; Lam LTM et al. (2020). Covert Covid-19 and false positive dengue serology in Singapore. Lance Infect. Recuperado en: Epub doi:10.1016/S1473-3099(20)30158-4
Joob B, Wiwanitkit V. (2020). Covid-19 can present with a rash and be mistaken for dengue. J. Am. Acad. Dermatol. Recuperado en: Epub doi: 10.1016/j.jaad.2020.03.036
Ackleh, AS and Allen LJS (2003). Competitive exclusion and coexistence for pathogens in an epidemic epidemic model with variable population size. J. of Mathematical Biology, Vol 47(2): 153-168.
Hethcote, HW; Wang, W. and Li, Y. (2005). Species coexistence and periodicity in host-host pathogens models. J. Math. Biol. Vol 51: 629-645.
Isea, R. (2020). La dinámica de transmisión del Covid-2019 desde una perspectiva matemática. Revista Observador del Conocimiento, Vol 5(1): 15-23.
Isea, R. (2014). Analysis of an SEIR-SEI four-strain epidemic dengue model with primary and secondary infections. Revista Electrónica Conocimiento Libre y Licenciamiento, Vol 7(5): 3-9.
Isea, R. y Lonngren, KE. (2018). Toward an early warning system for Dengue, Malaria and Zika in Venezuela. Acta Scientific Microbiology, Vol 1(3): 30-35.

