Resumen: El uso de plantas ricas en taninos (PRT) con propiedades antihelmínticas (AH) es una alternativa para el control de nematodos gastrointestinales (NGI) en especies de interés ganadero. La atención en plantas con estas propiedades se debe principalmente a la aparición y extensión de poblaciones parasitarias resistentes a los antihelmínticos. Recientemente en Yucatán se ha reportado el efecto de AH de extractos vegetales sobre huevos de Haemonchus contortus mediante la prueba de inhibición de la eclosión. Entre las principales especies vegetales con propiedades AH destacan los extractos etanólicos y hexánicos, principalmente del follaje de Lysiloma latisiliquum, Laguncularia racemosa, Rizophora mangle y Avicennia germinans, Theobroma cacao y Coffea arabica. Sin embargo, recientemente se ha observado que las leguminosas son una importante fuente de metabolitos secundarios como Leucaena leucocephala, Lysiloma latisiliquum, Acacia cornígera y Mimosa bahamensis. La evidencia demuestra que los metabolitos secundarios que contienen algunas leguminosas forrajeras afectan diversos procesos biológicos de los nematodos gastrointestinales de rumiantes, por lo que podría ser una alternativa para el control de helmintos en la producción de pequeños rumiantes.
Palabras clave:Antihelmínticos, forrajes, leguminosas, metabolitos, nematodos, nutracéutico, rumiantes, taninos.
Abstract: The use of plants rich in tannins (PRT) with anthelmintic properties (AH) is an alternative for the control of gastrointestinal nematodes (NGI) in species of cattle interest. The attention in plants with these properties is mainly due to the appearance and extension of parasitic populations resistant to anthelmintics. Recently, in Yucatan, the effect of AH from plant extracts on Haemonchus contortus eggs has been reported by the hatching inhibition test. Among the main plant species with AH properties are ethanolic and hexane extracts, mainly from the foliage of Lysiloma latisiliquum, Laguncularia racemosa, Rizophora mangle and Avicennia germinans, Theobroma cacao and Coffea arabica. However, it has recently been observed that legumes are an important source of secondary metabolites such as Leucaena leucocephala, Lysiloma latisiliquum, Acacia cornigera and Mimosa bahamensis. The evidence shows that the secondary metabolites that contain some forage legumes affect various biological processes of the gastrointestinal nematodes of ruminants, so it could be an alternative for the control of helminths in the production of small ruminants.
Keywords: Anthelmintics, forages, legumes, metabolites, nematodes, nutraceuticals, ruminants, tannins.
ARTÍCULOS DE REVISION
La importancia de los metabolitos secundarios en el control de nematodos gastrointestinales en ovinos con énfasis en Yucatán, México
The importance of secondary metabolites in the control of gastrointestinal nematodes in sheep with emphasis on Yucatán, Mexico
Selva Andina Research Society
Recepción: 01 Marzo 2018
Aprobación: 01 Septiembre 2018
Publicación: 01 Octubre 2018
Una limitante de importancia económica para el desarrollo de la ganadería bajo las condiciones del trópico son las infestaciones por parásitos gastrointestinales1, que se reflejan en baja conversión alimenticia, mortalidad de los animales, reducción de los parámetros productivos y reproductivos, además del alto costo para su control, entre otros, que deriva en pérdidas económicas para los productores.2
Por mucho tiempo, la principal estrategia empleada por los productores para el control de parásitos gastrointestinales en rumiantes fue la aplicación de compuestos antihelmínticos sintéticos. Estos fármacos por su gran eficacia, amplio espectro y poder residual, tuvieron un éxito inicial, e incluso se llegó a pensar en que estos serían la solución final para la presencia de NGI, creando un falso sentido de seguridad en los productores, quienes sustituyeron el diagnóstico y el asesoramiento profesional, por la casi exclusiva utilización de drogas en forma irracional e indiscriminada.1
La aparición y extensión de poblaciones parasitarias en diversas especies resistentes a los antihelmínticos, la creciente preocupación por la inocuidad alimentaria, así como el impacto negativo sobre el medio ambiente de los fármacos antihelmínticos, son las principales razones que impulsaron la búsqueda de métodos alternativos al uso de fármacos sintéticos en el control de NGI en pequeños rumiantes.3,4 Por tal motivo, el uso de plantas ricas en taninos (PRT) con propiedades antihelmínticas (AH) es una opción para el control de NGI en especies de interés ganadero5,6,7,3,8,9, por lo que estas podrían desempeñar un papel preponderante en el control no convencional de las parasitosis en el futuro.
Los compuestos bioactivos (CBA) de las plantas tienen la capacidad de interactuar con proteínas de NGI, modificando sus propiedades físicas y químicas.3 Existen diversos métodos que han sido utilizados in vitro e in vivo, para validar y comprender sus propiedades AH de las plantas.10 Recientemente en Yucatán, se reportó el efecto AH de extractos vegetales sobre huevos de H. contortus mediante la prueba de inhibición de eclosión11, evaluando extractos etanólico, hexánico y diclorometano de Phytolacca icosandra, reportándose diferencias del efecto AH de cada extracto, teniendo una mayor eficacia los extractos etanólicos y hexánicos. Por otra parte12, evaluaron extractos hidro-acetónicos del follaje de Lysiloma latisiliquum, Laguncularia racemosa, Rizophora mangle y Avicennia germinans. Así mismo, semilla y cascarilla de Theobroma cacao y Coffea arabica, resultando mayor efecto AH en los extractos de R. mangle y cáscara de T. cacao.
Existe una amplia variedad de CBA. Sin embargo, se ha considerado a los taninos como principal agente responsable de la acción AH de las plantas, aunque se han reportado diversos compuestos secundarios principalmente saponinas, glucósidos10, y lectinas que presentan actividad AH sobre NGI de rumiantes. No obstante, se ha reportado una enorme variabilidad en la susceptibilidad de los NGI hacia diversas plantas y sus derivados.13 Esta variación en la respuesta AH ha sido estudiada por diversos autores, quienes atribuyen las variaciones del efecto AH a la especie y procedencia del NGI14,15,12, al tipo de hospedero16 así como a factores propios de las plantas y del tipo de bioensayo.17
En recientes estudios realizados en el estado de Yucatán, fue posible determinar que H. contortus, aislados en la región, presentan menor susceptibilidad in vitro a extractos acetónicos ricos en taninos obtenidos de plantas de la vegetación local, en comparación con otros aislados de la misma especie provenientes de regiones templadas que los pequeños rumiantes no han sido expuestos a este tipo de vegetación.15,12 Estos resultados sugieren que la exposición previa de los NGI a los metabolitos secundarios de las plantas ha propiciado la generación de resistencia en los parásitos, ocasionando variaciones en la susceptibilidad en diferentes aislados. Así mismo18, registraron las especies de plantas forrajeras presentes en la vegetación nativa que son consumidas por los pequeños rumiantes en pastoreo, así como la forma y tamaño de bocados, logrando determinar el nivel de consumo. Se presume que la susceptibilidad de los NGI hacia los extractos de plantas taníferas pudiera estar influenciado por el historial y nivel de su consumo, por parte de los rumiantes, presentándose el mayor efecto AH hacia las que se tiene menor consumo y/o historial de exposición. A pesar que se ha propuesto que la exposición previa a las plantas influye sobre la susceptibilidad de H. contortus, esta hipótesis no ha sido probada ampliamente, ni se ha establecido si existe una relación entre el nivel de consumo de las plantas y el grado de susceptibilidad in vitro de H. contortus hacia las mismas.
Las plantas, a diferencia de otros organismos, destinan una cantidad significativa del carbono asimilado y de la energía a la síntesis de una amplia variedad de moléculas orgánicas que no parecen tener una función directa en los procesos metabólicos primarios como la fotosíntesis, respiración, asimilación de nutrientes, transporte de solutos o síntesis de proteínas, carbohidratos o lípidos, y las cuales se denominan como metabolitos secundarios.19
Se considera que existen alrededor de 1200 compuestos secundarios, presentando una distribución variable dentro del reino vegetal. Generalmente cada tipo de MS se presenta en una sola especie o grupo de plantas taxonómicamente relacionadas.20,21,22
Los MS tienen diversas funciones, que están relacionadas con las interacciones ecológicas entre planta y medio ambiente, principalmente en defensa de la planta contra depredadores y patógenos, actuando como atrayentes o repelentes de animales, propiciándole sabor amargo a las plantas, reducir su digestibilidad y palatabilidad en los herbívoros e incluso convirtiéndolas en tóxicas para estos, inhibiendo así el desarrollo de insectos, nematodos, hongos, bacterias, mejorando el crecimiento de las plantas y la consistencia.23,20,19,24 También protegen a las plantas del estrés abiótico, como las radiaciones ultravioletas.25
En menor medida, los MS también actúan dentro de la reproducción como atrayentes de polinizadores y animales que se alimentan de los frutos, como pigmentos de flores y/o frutos19, así como también participan en la comunicación de las plantas con otros organismos.25
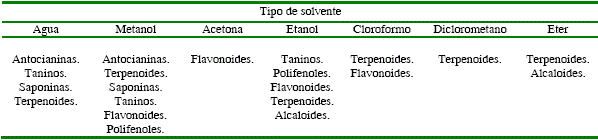
La mezcla de metabolitos secundarios es única para cada especie19, presentando variaciones a lo largo del año22, ya que diversos factores, como radiación solar, edad, estado fenológico de la planta, nutrición, estrés hídrico, procedencia geográfica, precipitación, interacción con herbívoros, condiciones de recolección del vegetal interacciones bióticas entre otras, influyen para que genere mecanismos de adaptación entre ellos, que determinan la producción de MS.23 Se sabe que estos compuestos son más comunes en la vegetación tropical que en los ecosistemas templados, y los ambientes húmedos en comparación a los secos.26 Por otra parte, además de la variación estacional, los MS no se distribuyen uniformemente entre todos sus componentes estructurales, al igual, en las yemas en crecimiento, hojas jóvenes, órganos reproductores, dispersión, y en general todas las partes en crecimiento anual, existe mayor concentración, reactividad y diversidad de MS.26 Las plantas rastreras contienen menores concentraciones de metabolitos secundarios que las arbóreas, tabla 1.22,27
Distribución de metabolitos secundarios en diversas especies vegetales
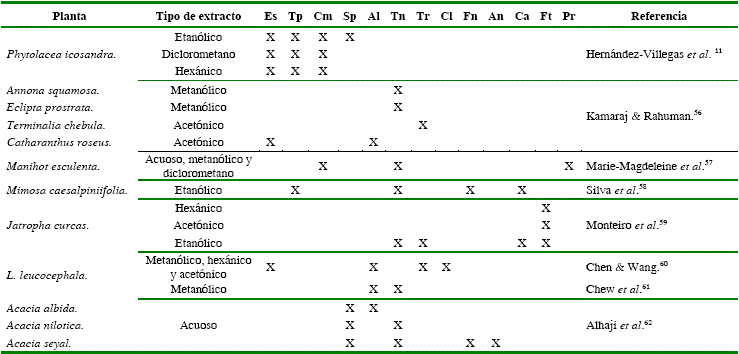
*EAH- Evaluación antihelmíntica, Al- Alcaloides, An- Antocianinas, Ca- Catequinas, Cl- Clorofilas, Cm- Cumarinas, Es- Esteroles, Fn- Fenoles, Ft- Fitoesteroles, Fv- Flavonoides, Pr- Proantocianidoles, Sp- Saponinas, Tp- Terpenoides, Tn- Taninos, Tr- Triperpenoides.
Actualmente, los sistemas de producción ganadera consideran que la nutrición apropiada se puede proporcionar a través del monocultivo. Sin embargo, los rumiantes pueden satisfacer sus necesidades de nutrientes y regular su ingesta de compuestos secundarios cuando se les ofrece una variedad de alimentos. Esta variedad es fundamental, ya que las plantas les proporcionan una gran variedad de productos químicos, con un potencial de mejorar su salud y el bienestar. Por ejemplo, los MS, que protegen a las plantas de depredadores y plagas, también afectan negativamente los procesos celulares y metabólicos de los herbívoros. Empero, a dosis bajas en mezclas apropiadas, estos compuestos pueden presentar efectos beneficiosos sobre la salud y nutrición animal.
La variedad de alimentos permite que los animales expresen sus preferencias alimentarias, que a la vez mejoran su bienestar, mediciones conductuales pueden representar una herramienta importante para evaluar este efecto en el ganado.28 En el estado de Yucatán18, registraron especies, así como la forma y tamaño de plantas forrajeras consumidas por pequeños rumiantes pastoreando para determinar el nivel de consumo. Las observaciones realizadas durante tres días consecutivos en dos ocasiones al mes, con intervalo de al menos diez días entre cada observación durante un año. Se acompañó a un rebaño mixto compuesto por ovejas y cabras, en los circuitos de pastoreo cotidiano por cuatro horas al día. El consumo de todos los materiales vegetales se registró en tres ovejas y tres cabras previamente habituadas a la presencia de los observadores humanos. Los datos se registraron en diferentes categorías de acuerdo al grupo taxonómico y el tamaño de cada bocado.
Debido al importante impacto económico de los NGI en la industria ovina mundial4 y a raíz de la aparición de la resistencia antihelmíntica (RAH), ha surgido el interés por estudiar las propiedades antihelmínticas de diversos MS de las plantas, entre ellos los taninos, como una alternativa para el control de NGI de rumiantes.29,30 El efecto ocasionado por el consumo de plantas taníferas sobre las poblaciones de NGI pueden clasificarse en directos e indirectos.31 Los efectos directos son las interacciones que tienen sobre las funciones fisiológicas de los NGI, interfiriendo sobre los procesos de eclosión, desarrollo y motilidad de larvas infectantes, alimentación y reproducción de las fases adultas.17,4,32,12 Por otra parte, los efectos indirectos constituyen la mejora en la absorción de proteínas, ya que los MS favorecen que estas sean asimiladas a nivel de duodeno. Se ha demostrado que una mayor asimilación de proteínas está asociada con la mejora en la inmunidad del hospedero.31 Existe variabilidad en los valores de respuesta que presentan los extractos de las plantas ricas en taninos (PRT) sobre NGI, asociados principalmente con la dinámica temporal y espacial que se observa en la concentración y composición de los compuestos polifenólicos en la naturaleza.4
Otra fuente de variación la constituye la modalidad del bioensayo que se utiliza para validar la acción AH de los compuestos secundarios. Generalmente los estudios se han llevado a cabo in vitro, bajo la suposición de que la intensidad y el tipo de efecto observado en contra los parásitos sea similar al que se presentará en el hospedero. Este tipo de pruebas presentan varias ventajas, como la obtención de resultados a menor tiempo e inversión, con mayor control de las condiciones, son fáciles de realizar y repetir, además, se pueden realizar en diversas etapas del ciclo biológico de los nematodos, pueden ser evaluados extractos enteros o purificados sin el riesgo de inferencia en los resultados a causa de otros componentes de las plantas (Figura 1). Sin embargo, en la mayoría de los casos, el material debe ser extraído de la planta, por lo que de acuerdo al solvente utilizado, será el tipo y cantidad de MS en el extracto, además en ocasiones, la modalidad in vitro no es posible reproducir totalmente las condiciones ambientales que se presentarán in vivo, por la diferencia fisiológicas entre el sitio de predilección del parásito en el hospedero, así como factores propios del hospedero que afectan la biodisponibilidad de los compuestos bioactivos.
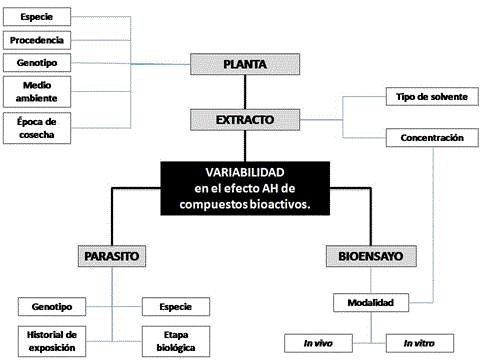
Figura 1
Factores que influyen en la variabilidad del efecto AH de los compuestos bioactivos presentes en las plantas
Por lo anterior se consideran más confiables los resultados obtenidos de estudios in vivo que los in vitro. Sin embargo, los ensayos in vitro son de gran utilidad, ya que representan un primer acercamiento en la selección inicial de especies y concentraciones más adecuadas para llevar a cabo ensayos en condiciones in vivo.10
Un factor a considerar en la variación del efecto de los MS, tiene origen en la metodología que se emplea para su evaluación. La técnica de extracción de los MS es uno de los principales elementos a considerar, ya que esta juega un rol importante en su evaluación, debido a que la metodología y solvente utilizados en la extracción influyen sobre el tipo y cantidad de metabolitos presentes en el extracto.33 (Tabla 2)
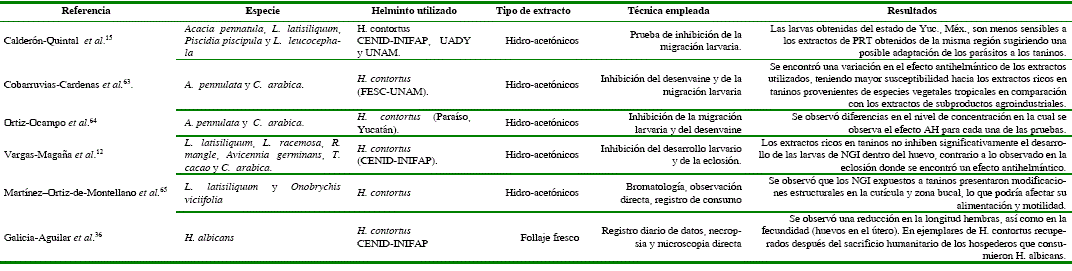
La actividad nematicida de los extractos ricos en taninos de diversas leguminosas y plantas leñosas ha sido probada en modalidad in vitro.34 Incluso se ha descrito el efecto AH in vivo que resulta de consumir los forrajes de las plantas ricas en taninos.35,36,37 Varios estudios in vitro han señalado la influencia que tienen los taninos condensados sobre los NGI de los ovinos al afectar diversos procesos biológicos de éstos.15,35,12 Así mismo, también se han comparado la susceptibilidad de aislados de H. contortus de diferente procedencia geográfica15, evaluaron el efecto AH sobre la migración larvaria de cuatro plantas ricas en taninos (PRT) locales (Acacia pennatula, L. latisiliquum, Piscidia piscipula y L. leucocephala), los resultados permitieron sugerir la adaptación del aislado Campus de Ciencias Biológicas y Agropecuarias- Universidad Autónoma de Yucatán (CCByA-UADY )hacia los extractos de plantas ricas en taninos (PRT) de Yucatán, al encontrar que este era menos sensible que los aislados Centro Nacional de Investigación Disciplinaria-Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias y Facultad de Estudios Superiores de Cuautitlán-Universidad Nacional Autónoma de México CENID-INIFAP y FESC-UNAM. Resultados similares fueron reportados por12, quienes evaluaron las diferencias en la susceptibilidad de seis aislados de H. contortus procedentes de México y Francia hacia extractos de subproductos agroindustriales y de PRT. Los resultados obtenidos sugieren una menor susceptibilidad de aislados de H. contortus con historial de contacto con PRT. Los resultados de ambos estudios sugieren que NGI presentan una adaptación hacia las plantas forrajeras nativas, esto quizás por la exposición constante, lo que genera una presión en la selección, eliminando selectivamente a NGI susceptibles de la población genéticamente heterogénea, produciéndose un incremento de individuos portadores de genes que confieren resistencia a los metabolitos secundarios y son transmitidos a la siguiente generación.38 (Tabla 3).
Reporte de efectos antihelmínticos de los taninos sobre NGI en investigaciones previas en México
Entre los bioensayos in vitro, se encuentra la inhibición de eclosión de huevos (Egg Hatch Assay, EHA por sus siglas en ingles). Originalmente, esta prueba fue diseñada para la evaluación del efecto AH de los benzimidazoles, pero en la actualidad, también se emplea para determinar el efecto AH de compuestos secundarios de las plantas. La prueba consiste en incubar por 48 h, huevos de NGI en concentraciones seriadas de compuestos con propiedades AH, para posteriormente contabilizar el porcentaje de huevos que eclosionan en cada una de las concentraciones, los resultados se contrastan con el grupo control, para determinar la eficacia se calcula la concentración eficaz 50 (CE50), que es la concentración requerida para evitar la eclosión del 50% de los huevos.39
Se han descrito dos efectos diferentes de los AH en contra de los huevos de nematodos: i) impidiendo la formación del embrión o ii) impidiendo la salida de la larva del huevo (inhibición de eclosión). Este ensayo tiene la ventaja de que permite obtener resultados en forma rápida, ya que los huevos que se utilizan en ella, son obtenidos en el momento de un animal donador. Presenta la desventaja de la obtención de huevos al ser necesario procesar a las heces en un lapso no mayor a 3 h, ya que de lo contrario se corre el riesgo de que las larvas se desarrollen y eclosionen.40,39 (Tabla 4).
Algunos estudios para detección de efecto AH de extractos de plantas hacia NGI mediante la técnica de Inhibición de la eclosión
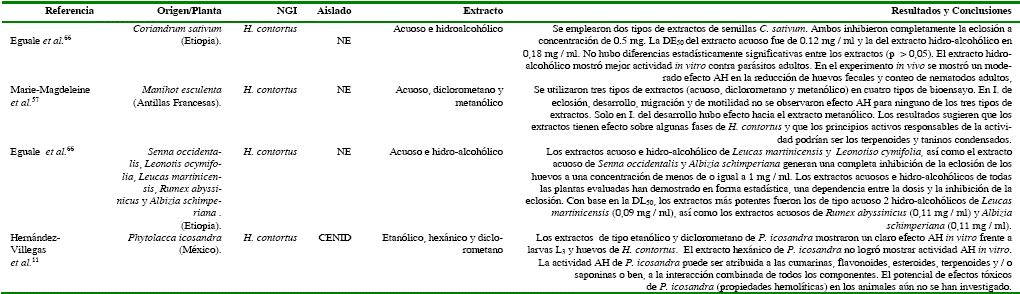
NE- No especific
Las áreas de vegetación secundaria nativa son fuente de nutrientes para los pequeños rumiantes en pastoreo.41 En el estado de Yucatán la vegetación secundaria, abarca extensiones de plantaciones de henequén abandonadas, también áreas agrícolas de temporal que es practicada en las comunidades rurales. En Yucatán se considera que este tipo de ecosistema está compuesto por alrededor de 1980 especies florísticas, de ellas 201 son reportadas con potencial forrajero, siendo la mayoría leguminosas.42,43 Los animales que pastorean en vegetación secundaria deben utilizar una comunidad mucho más diversa y variable con respecto a las praderas de gramíneas. Esta variabilidad permite al herbívoro la posibilidad de seleccionar su dieta en base a sus necesidades.41 Recientemente en Yucatán, se realizan observaciones para determinar el nivel de consumo de pequeños rumiantes en pastoreo en vegetación heterogénea nativa44,18, a la fecha ha sido posible identificar las especies y el nivel de su consumo (Tabla 5).
Especies forrajeras con diferente nivel de consumo por cabras en pastoreo

(González-Pech et al. datos por publicar)
Es una especie nativa de Mesoamérica, pertenece a la familia Polygonaceae Juss, conocida en la Península de Yucatán con el nombre maya de Dzidzilché. Un arbusto o árbol pequeño con alrededor de 3 m de alto, presenta una corteza profundamente fisurada, hojas alternas y simples, de ovadas a elípticas, peciolo corto, base redondeada a obtusa. Las flores son panículas racemosas de color verdoso, se desarrollan de yemas que aparecen al final o previa a la estación de crecimiento.45 La especie se distribuye en México desde Oaxaca (Istmo de Tehuantepec), sur de Tabasco, Campeche, Yucatán y Quintana Roo, formando parte importante en la estructura florística de la selva baja caducifolia. Es considerada como la especie más ampliamente distribuida en el centro y norte de la Península de Yucatán.46 Es de gran importancia en la industria apícola, la miel producida con esta especie es de alta estima.47
Árbol o arbusto caducifolio o perennifolio, de 3 a 6 m (hasta 12 m) de altura con un diámetro de hasta 25 cm, copa redondeada, ligeramente abierta y rala, hojas alternas, bacinadas, de 9 a 25 cm de largo, verde grisáceas y glabras. Tronco usualmente torcido y se bifurca a diferentes alturas. Ramas cilíndricas ascendentes. Desarrolla muchas ramas finas cuando crece aislado. Las flores se encuentran en cabezuelas, con 100 a 180 flores blancas, de 1.2 a 2.5 cm de diámetro, flor de 4.1 a 5.3 mm de largo, pétalos libres, el fruto se encuentra en vainas oblongas de color verde cuando están tiernas y cafés cuando maduras, conteniendo de 15 a 30 semillas.48
Es de amplia distribución en las regiones tropicales y subtropicales de México, en altitudes que van de 0 a 900 msnm. Prospera en ambientes adversos. Se adapta muy bien a las tierras bajas, crece desde sitios secos con 350 mm/año hasta húmedos con 2300 mm/año y temperatura media anual de 22 a 30 ºC. Es necesario un período seco de cuatro a seis meses.49
Es un árbol perteneciente a la familia Leguminosae, el árbol alcanza hasta 20 m de altura y 70 cm de diámetro normal, representativo de la selva mediana subperennifolia, particularmente abundante, frecuente, con alta regeneración natural en sitios con vegetación secundaria de 9 a 12 años de edad derivados de selvas medianas y bajas subperennifolias50, sobre suelos calizos y de bosque seco próximo a las costas, con buen drenaje y a elevaciones menores de 400 msnm.51 Un árbol de 15-20 m de altura, con diámetros de 60 a 70 cm, de fuste recto, se ramifica desde un 50 % de su altura total, copa redondeada, ramas ascendentes. La corteza gris pardusco, algunas lenticelas blancas y circulares. Tiene hojas compuestas, bipinnadas, de 11 a 20 cm incluyendo el pecíolo. Los frutos son vainas de 9 a 15 cm de largo, 2 a 4 cm de ancho, dehiscentes, en forma aplanada, agudas, de color café oscuro.51
Un arbusto de la familia de las Fabáceas. Esta especie puede alcanzar hasta 10 m de altura. Presenta hojas bipinnadas, con raquis principal de 12 a 14 cm de longitud, 8 a 10 pares de hojuelas de 4 a 6 cm de largo y pecíolo acanalado de 0.5 a 2 cm, cada hojuela con 22 a 32 pares de pinnas de 3 a 7 mm de largo y 7 a 17 mm entre par de pinnas. Inflorescencia en espiga con flores sésiles de corolas amarillas de 1.1 a 1.5 mm de largo, ligeramente más largas que el cáliz. Legumbre color caoba, usualmente erecta, rolliza, 5 a 9 cm de longitud por 1.3 a 1.8 cm de anchura, ápice puntiagudo, semillas color pardo obscuro.48 Poseen un par de espinas considerablemente infladas, ahuecadas hacia afuera, que están en pares, de más de 2 cm de largo, ubicadas en la base de cada hoja. Estas espinas generalmente son de tonalidad café, aunque algunas veces también se presentan de color marfil o amarillas. Los peciolos presentan nectarios y unos pequeños órganos nutritivos, denominados cuerpos de Belt que se localizan en el extremo de cada foliolo.26
Este tipo de acacia crece extraordinariamente rápido y son particularmente abundantes en áreas perturbadas, donde la competencia entre especies colonizadoras de rápido crecimiento es con frecuencia muy intensa.26 Tanto la flor como su fruto, se observa en el periodo de abril-agosto.52 En México se la observa en la Península de Yucatán, en la vertiente del Golfo desde Tabasco hasta Tamaulipas, mientras que en la del Pacifico es común en los estados de Chiapas, Oaxaca y Guerrero.52 Se le utiliza para fines medicinales, como combustible y como forraje ocasional. Es conocida por su relación simbiótica con las hormigas del género Pseudomyrmex (P. ferruginea, P. belti, P. nigrosincta.26,52
Arbusto que llega a medir 8 m de altura, hojas verdes muy pequeñas. Flores abundantes de color rosa o blanco, en forma de cabezas globosas. Se considera caliente. Crece a orilla de los caminos y en zonas de vegetación secundaria derivada de selvas bajas y medianas caducifolias, en selvas bajas subcaducifolias y selvas altas sub perennifolias.53 Tiene una amplia distribución en América, desde Brasil hasta México, se la encuentra en los estados de Campeche, Chiapas, Quintana Roo, Tabasco, Veracruz y Yucatán.52,53 Destaca su uso en el tratamiento de quemaduras y heridas superficiales de la piel y problemas gastrointestinales, en la construcción de cercas y postería, como combustible y para la recuperación de suelos y vegetación.52,53
Árbol de la familia de leguminosas que se distribuye en las selvas bajas, medianas y vegetación secundaria del sureste de México.54 Se le emplea para la elaboración de artículos menores de madera, y como forrajera.55 También se le conoce por su importante aportación a la industria apícola. Es considerada como uno de los mejores combustibles.54
Los parámetros algunos compuestos fenólicos se pueden observar en la tabla 6.
Contenido de algunos compuestos fitoquímicos en seis especies forrajeras consumidas por caprinos en Yucatán (g/ kg MS)
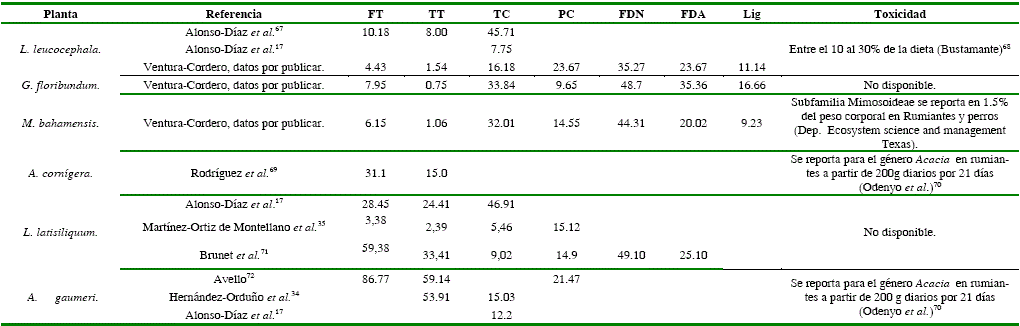
TF=Total fenoles, TT= Total taninos, TC= Taninos condensados, PC= Proteína cruda, FDN=Fibra detergente neutra, FDA= Fibra detergente acida, Lig= Lignina.
El uso masivo e inadecuado de compuestos antihelmínticos, han propiciado a nivel global la proliferación de poblaciones de NGI de rumiantes con resistencia. Lo anterior, aunado a una creciente concientización sobre la inocuidad alimentaria, así como también el impacto negativo de los fármacos sobre el medio ambiente, han despertado el interés por evaluar estrategias alternativas al uso de medicamentos sintéticos para el control de parásitos.
Entre estas opciones distintas al uso de fármacos, se encuentra el empleo de plantas ricas en compuestos bioactivos o metabolitos secundarios. Estos son compuestos fitoquímicos cuya función primaria está en la defensa de la planta contra herbívoros y patógenos. Desde hace tiempo se conoce que dichos compuestos bioactivos que contienen las leguminosas forrajeras tienen la capacidad de modificar diversos procesos biológicos de los nematodos gastrointestinales de rumiantes, principalmente la eclosión y desenvaine de larvas, así como el conteo fecal de huevecillos. Sin embargo, a pesar de que esta es una de las opciones más prometedoras, sobre todo en regiones tropicales, todavía existe un largo camino por recorrer, ya que el gran número de factores que influyen sobre la disponibilidad y concentración de MS, propicia una gran variabilidad en el efecto antihelmíntico in vivo e in vitro, sobre todo en esta última modalidad, por lo que es necesario continuar e incrementar las investigaciones que permitan conocer a fondo cuales compuestos generan mayor actividad antihelmíntica, así como también las especies de plantas que los contienen. Por otra parte, es importante señalar que hasta la fecha la opción más viable para proporcionar estos compuestos bioactivos a los rumiantes, es el pastoreo directo, por lo que también resulta necesario realizar evaluaciones a fin de poder determinar el manejo eficiente de los rumiantes. Por ultimo cabe resaltar que, si bien está ampliamente demostradas las propiedades antihelmínticas de una amplia gama de plantas, este no puede ser un método único en el control de NGI en rumiantes, por lo que deberá de ser empleado en combinación con otras estrategias.
http://www.scielo.org.bo/scielo.php?script=sci_arttext&pid=S2311-25812018000200004&lng=es&nrm=iso (html)
Al Campus de Ciencias Biológicas y Agropecuarias de la Universidad Autónoma de Yucatán.
Al Instituto Nacional de Investigaciones, Forestales, Agrícolas y Pecuarias
froyitovarroo@hotmail.com
Distribución de metabolitos secundarios en diversas especies vegetales

*EAH- Evaluación antihelmíntica, Al- Alcaloides, An- Antocianinas, Ca- Catequinas, Cl- Clorofilas, Cm- Cumarinas, Es- Esteroles, Fn- Fenoles, Ft- Fitoesteroles, Fv- Flavonoides, Pr- Proantocianidoles, Sp- Saponinas, Tp- Terpenoides, Tn- Taninos, Tr- Triperpenoides.

Figura 1
Factores que influyen en la variabilidad del efecto AH de los compuestos bioactivos presentes en las plantas
Reporte de efectos antihelmínticos de los taninos sobre NGI en investigaciones previas en México

Algunos estudios para detección de efecto AH de extractos de plantas hacia NGI mediante la técnica de Inhibición de la eclosión

NE- No especific
Especies forrajeras con diferente nivel de consumo por cabras en pastoreo

(González-Pech et al. datos por publicar)
Contenido de algunos compuestos fitoquímicos en seis especies forrajeras consumidas por caprinos en Yucatán (g/ kg MS)

TF=Total fenoles, TT= Total taninos, TC= Taninos condensados, PC= Proteína cruda, FDN=Fibra detergente neutra, FDA= Fibra detergente acida, Lig= Lignina.