INTRODUCCIÓN
Los Policloruros
de Bifenilo (PCB’s) son compuestos orgánicos clorados
sintéticos caracterizados por una baja reactividad y excelentes propiedades
aislantes eléctricas y térmicas. Su principal aplicación es su uso como fluidos
dieléctricos en capacitores y transformadores o en intercambiadores de calor
(Huang & Hong, 2000). Se produjeron cerca de 1,5 millones de Tm de PCB’s en todo el mundo entre 1929 y 1979, hasta su
prohibición en el Acta de Control de Sustancias Tóxicas (TSCA) (Habibullah-Al-Mamun, et al., 2019; Wong, et al., 2004; Xing et al., 2005).
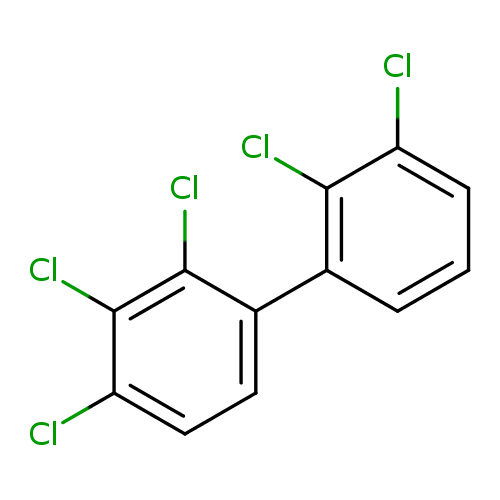 Figura 1.
Estructura molecular del Aroclor 1254.
Figura 1.
Estructura molecular del Aroclor 1254.
Los equipos eléctricos obsoletos que operaron con aceites dieléctricos con PCB’s, al ser desechados en vertederos comunes sin los controles y cuidados apropiados, son una fuente importante de contaminación. El aceite contaminado con PCB’s puede derramarse en el suelo y llegar a cuerpos de agua subterráneas o superficiales ya sea accidentalmente o por corrosión y ruptura de los tanques que los almacenan (Habibullah-Al-Mamun et al., 2019; Law & Jepson, 2017). Una vez presentes en el agua, estos contaminantes pueden incorporarse a la cadena alimentaria y acumularse en organismos acuáticos, los cuales al ser consumidos por seres humanos llegan a causar graves daños a su salud (Atmaca et al., 2019; Nadarajan et al., 2017).
Aroclor 1254 es el nombre comercial de una mezcla de PCB’s producidos por la corporación Monsanto, y su numeración es debido a que poseen 12 átomos de carbono y 54% en peso de átomos de cloro, su estructura se presenta en la Figura 1. Esta mezcla fue la segunda más producida en el mundo y es especialmente tóxica por sus propiedades similares a la de las dioxinas (Lopera & Aguire, 2006; Parent et al., 2016). Sobre las posibilidades de eliminación de los PCB’s, debe considerarse que estos son sustancias inertes, tóxicas y térmicamente estables, por tanto, su descomposición natural es poco probable y los tratamientos convencionales son poco efectivos (Moreno, 2016; Law & Jepson, 2017). La toxicidad de los PCB’s sumada a la resistencia que tienen a la oxidación por microorganismos, hace que tratamientos biológicos sean inaplicables (Izquierdo & Peña, 2016), aspecto que motiva la aplicación de métodos alternativos de tratamiento como son los procesos de oxidación avanzada (POA’s).
Actualmente, el uso de equipos eléctricos que contienen aceites con PCB’s está prohibido en Ecuador y los aún existentes son almacenados por el Ministerio de Energía y Recursos Naturales No Renovables a la espera de una solución viable para el tratamiento de estos aceites contaminados (Frías & Gia, 2014).
En este trabajo se propone estudiar la transferencia de fase del Aroclor 1254 desde el aceite dieléctrico hacia una fase acuosa para su posterior degradación fotocatalítica empleado TiO2 irradiado con electrones acelerados.
MATERIALES Y
MÉTODOS
Cuantificación de Aroclor 1254 en aceite dieléctrico y fase acuosa
Para todas las pruebas se utilizó
como estándar un aceite dieléctrico proporcionado por el Laboratorio de
Análisis de Residuos de Contaminantes Orgánicos del Ministerio de Electricidad
y Recursos Naturales. El Aroclor 1254 presente en el aceite
dieléctrico se determinó mediante cromatografía de gases acorde al método ASTM
D 4059. Las inyecciones se realizaron en un cromatógrafo de gases Modelo 6890
(Agilent) equipado con un automuestrador G4513A
(Agilent) y un detector de captura de electrones (ECD). Se usó una columna para
compuestos halogenados con composición 5% fenil-polimetilsiloxano
(30 m de largo, 0,25 mm de diámetro interno, 0,25 µm de espesor de film,
Agilent HP-5). Para la construcción de la curva de calibración se prepararon
soluciones de 0,1; 0,25; 0,5; 1,0; 1,5 y 2,0 mg de Aroclor
1254/L de solvente, y se inyectaron al cromatógrafo por duplicado,
posteriormente se inyectaron soluciones estándar de concentración conocida de Aroclor 1254 para comparar el resultado obtenido con el
valor de concentración conocida. El software ChemStations
versión A.08.03 fue utilizado para controlar la elución y registrar los
cromatogramas.
Transferencia de Aroclor 1254 a fase acuosa
Se probaron dos alternativas para
transferir las moléculas de Aroclor 1254 a la fase
acuosa. La primera alternativa fue con Polietilenglicol 400 (PEG 400) debido a
sus características anfipáticas capaces de atrapar las moléculas de Aroclor 1254 y llevarlas a la fase acuosa. A 25 mL de solución de PEG 400 al 10% (v/v), se agregaron 250 µL
de aceite dieléctrico usado y se mezcló con agitación a 120 rpm durante 3 h. La
segunda alternativa fue empleando Tritón® X-100 aplicando el mismo
procedimiento mencionado para el PEG 400. La cuantificación de Aroclor 1254 se realizó mediante la toma de alícuotas de
las mezclas de aceite dieléctrico con los agentes de transferencia de fase (PEG
400 o Tritón® X-100) cada hora (tres alícuotas en total para cada alternativa).
El contenido de Aroclor 1254 en el aceite tratado con
PEG 400 o Tritón® X-100 fue cuantificado mediante cromatografía de gases, descrito
previamente.
Degradación de Aroclor 1254 por fotocatálisis heterogénea con TiO2
irradiado
Para la degradación fotocatalítica de Aroclor 1254 se utilizó TiO2 rutílico microparticulado (Ti-Pure® R-902+, DuPont), previamente irradiado. La irradiación del TiO2 se realizó con un acelerador de electrones ELU-6U. Se colocó el TiO2 en bolsas transparentes de polietileno y se sometieron dichas bolsas a irradiación con dosis de 20 y 60 kGy. Luego de que el Aroclor 1254 ya estuvo en fase acuosa, ésta fue sometida al tratamiento por fotocatálisis heterogénea con TiO2 y radiación UV como fuente de energía. El estudio cinético de fotodegradación de Aroclor 1254 se realizó con 50 mL de la fase acuosa obtenida del tratamiento del aceite y 50 mg de TiO2 (Wong et al., 2004).
El TiO2 fue dispersado en la fase acuosa por sonicación por 10 min mediante un baño ultrasónico (CPXH, Branson). Luego la mezcla se sometió a radiación ultravioleta con una lámpara UV T8 de 15 W de potencia (Zhejiang Changhong). Se tomaron alícuotas de 1 mL cada 20 min durante las dos primeras horas y, posteriormente, una alícuota de 1 mL cada 60 min hasta completar las 4 h de tratamiento. Además, se realizaron ensayos con TiO2 (sin irradiar e irradiado) en presencia radiación UV y en ausencia de esta, con la finalidad de evaluar la influencia de la adsorción en la remoción de Aroclor 1254 del agua.
Mineralización de Aroclor 1254
El grado de mineralización se siguió
mediante COT. Las mediciones de COT en las fases acuosas (tratadas y sin
tratar) se realizaron mediante el Método Estándar 9060 (American Public Health Asosciation
[A.P.H.A], 1995). Las mediciones de COT se llevaron a cabo con un analizador de
Carbono Orgánico Total TOC-5000A. Dado que el agente de transferencia es un
compuesto orgánico, se espera de éste un aporte al contenido de COT de la fase
acuosa resultante del tratamiento del aceite dieléctrico. Es decir, el
contenido de COT en la fase acuosa después de haber transferido el Aroclor 1254 del aceite a la fase acuosa es, esencialmente,
la suma del carbono orgánico aportado por el agente de transferencia y el Aroclor 1254.
RESULTADOS
Transferencia de Aroclor 1254 a la fase acuosa
En
la Tabla 1, se presenta la transferencia porcentual de moléculas de Aroclor 1254 alcanzada al añadir 250 µL de aceite
dieléctrico a 25 mL de soluciones de PEG 400 y Tritón
X-100 al 10% v/v, respectivamente, después de mantenerlas en agitación
constante a 120 rpm durante 3 horas.
Tabla 1.
Porcentaje de transferencia de Aroclor 1254 a la fase acuosa en función del tiempo de
agitación.
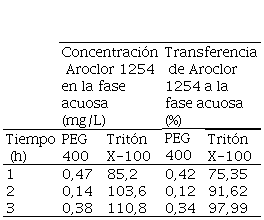 Nota: La concentración inicial de Aroclor 1254 en el aceite dieléctrico usado en estos
ensayos fue 11.307,0 mg/L.
Nota: La concentración inicial de Aroclor 1254 en el aceite dieléctrico usado en estos
ensayos fue 11.307,0 mg/L.
|
Concentración Aroclor
1254 en la fase acuosa (mg/L)
|
Transferencia de Aroclor
1254 a la fase acuosa (%)
|
|
Tiempo (h)
|
PEG 400
|
Tritón X-100
|
PEG 400
|
Tritón X-100
|
|
1
|
0,47
|
85,2
|
0,42
|
75,35
|
|
2
|
0,14
|
103,6
|
0,12
|
91,62
|
|
3
|
0,38
|
110,8
|
0,34
|
97,99
|
Como
se puede evidenciar en la Tabla 1, el porcentaje de transferencia de fase
oleosa a fase acuosa del Aroclor 1254, es mucho mayor
cuando se emplea Triton X-100, por lo que los
estudios de degradación se precederán con este agente de transferencia.
Fotodegradación
de Aroclor 1254 con TiO2 irradiado
Utilizando
Tritón X-100 como el agente de transferencia de fase, se evaluó la degradación fotocatalítica de Aroclor 1254 con
TiO2 sin irradiar e irradiado, dosis de 20 y 60 kGy,
(Figura 2). Para los ensayos de degradación, se usaron 50 mg de TiO2
por cada 50 mL de fase acuosa a tratar, equivalente a
una concentración de 100 mg/L (Wong et
al., 2004), y esta cantidad se mantuvo constante para todos los ensayos.
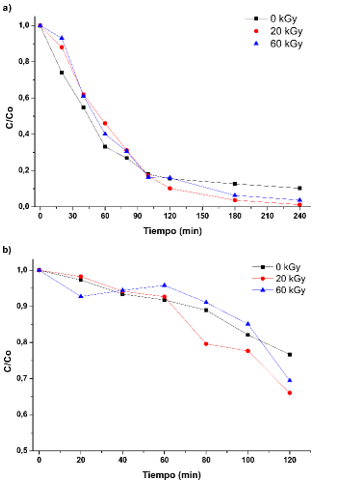 Figura
2.
Degradación fotocatalítica de Aroclor 1254 en fase acuosa y b) Adsorción de Aroclor 1254 en TiO2 sin irradiar e irradiado
(20 kGy y 60 kGy).
Figura
2.
Degradación fotocatalítica de Aroclor 1254 en fase acuosa y b) Adsorción de Aroclor 1254 en TiO2 sin irradiar e irradiado
(20 kGy y 60 kGy).
En la Tabla 2 se presentan las constantes de velocidad de pseudo primer
orden para las reacciones de degradación fotocatalítica
de Aroclor 1254. Además, también se calcularon los
tiempos de vida media del Aroclor 1254, en cada caso.
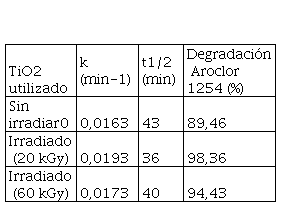
Tabla 2.
Constante de velocidad, tiempos de vida media (t1/2)
y porcentaje de degradación para el Aroclor 1254, de acuerdo a los tratamientos realizados al TiO2
utilizado.
|
TiO2 utilizado
|
k (min-1)
|
t1/2
(min)
|
Degradación
Aroclor 1254
(%)
|
|
Sin irradiar0
|
0,0163
|
43
|
89,46
|
|
Irradiado (20 kGy)
|
0,0193
|
36
|
98,36
|
|
Irradiado (60 kGy)
|
0,0173
|
40
|
94,43
|
Mineralización de Aroclor 1254
En la Figura 3 se muestra el COT luego de la fotodegradación,
con TiO2 irradiado a diferentes dosis. Además, se muestra un estudio de la
cantidad de COT que aporta cada compuesto presente en la muestra (Triton X-100 y Aroclor).
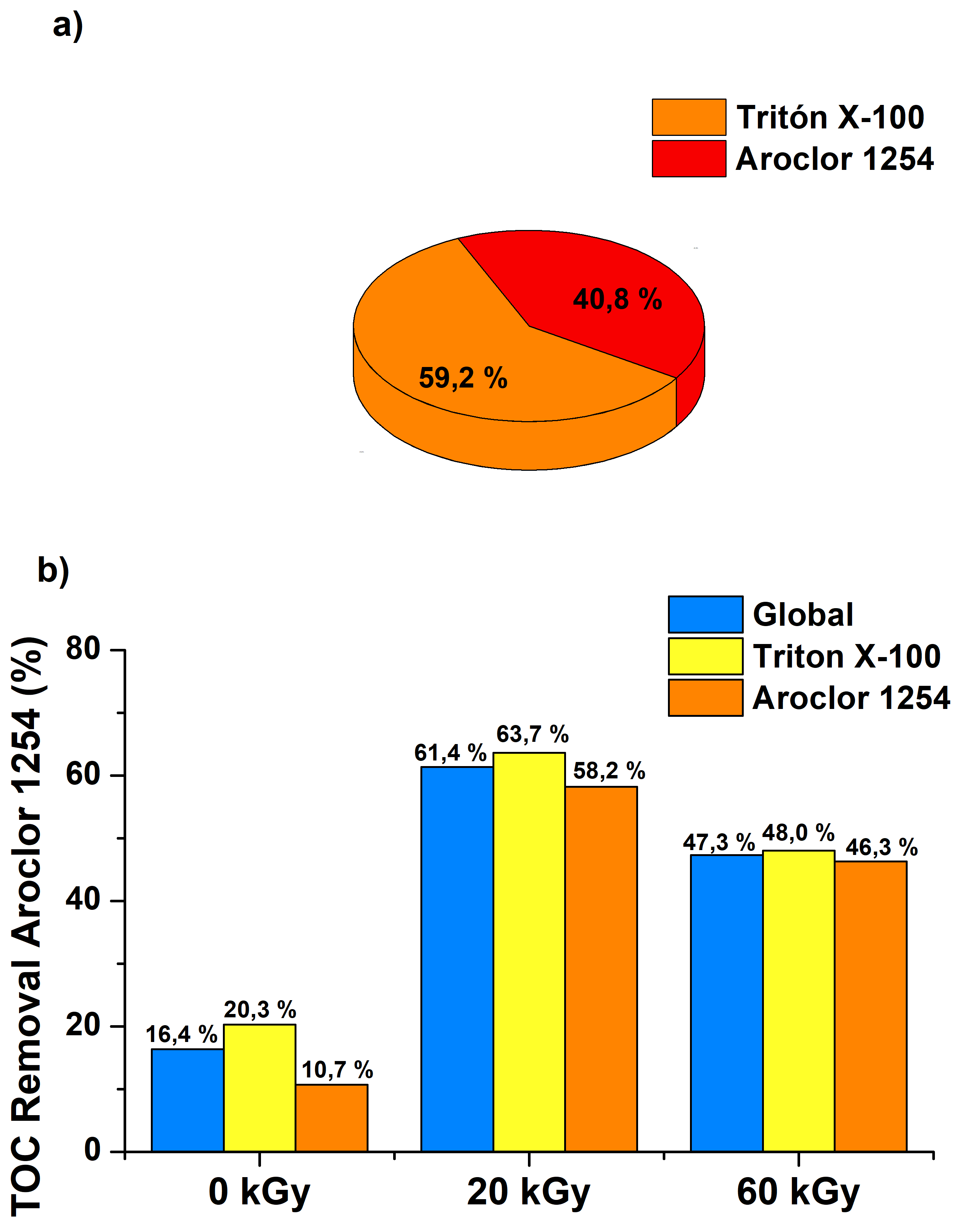 Figura 3
Porcentajes de remoción de COT mediante fotodegradación con TiO2 sin irradiar (0 kGy) e irradiado (20 kGy y 60 kGy): a) aporte de COT del Tritón X-100 y Aroclor 1254, b) COT global y de cada uno de los
aportantes.
Figura 3
Porcentajes de remoción de COT mediante fotodegradación con TiO2 sin irradiar (0 kGy) e irradiado (20 kGy y 60 kGy): a) aporte de COT del Tritón X-100 y Aroclor 1254, b) COT global y de cada uno de los
aportantes.
DISCUSIÓN
Transferencia de Aroclor 1254 a la fase acuosa
En la Tabla 1, se
evidencia que a pesar de las características anfipáticas del PEG 400 y de haber
sido exitosamente utilizado en el pasado para transferir PCB’s desde moluscos contaminados hacia disoluciones
acuosas (Nadarajan et al., 2017), la eficiencia no es la misma cuando se busca
transferir los PCB’s de aceite dieléctrico a un
solvente polar como el agua. La
eficiencia en la transferencia del Aroclor 1254 de la
fase oleosa a la fase acuosa con el Tritón X-100 es mucho mayor gracias a la
formación de micelas. Se generan estructuras de forma esférica en las que los
grupos funcionales hidrofílicos se ubican en la parte externa, mientras que, la
parte hidrofóbica de las moléculas se orienta hacia el centro de la esfera,
donde quedan atrapadas las moléculas hidrofóbicas de PCB’s
(Fröschl et al.,
1997). Por esta razón, se seleccionó el Tritón X-100 como agente de
transferencia de fase para los estudios de degradación del Aroclor
1254. Una explicación teórica ampliada se publicará más adelante incluyendo
estudios que respalden esta afirmación.
Degradación de Aroclor 1254 por fotocatálisis heterogénea con dióxido de
titanio irradiado
La Figura 2a muestra la fotodegradación de Aroclor 1254 en fase acuosa con TiO2 sin irradiar (0 kGy) e irradiado (20 y 60 kGy). La degradación del Aroclor 1254 sobre los tres tipos de TiO2 (de acuerdo a los tratamientos realizados) tienen un comportamiento similar hasta aproximadamente 100 min. Las curvas muestran que después de 240 min, el TiO2 irradiado a 20 kGy permite alcanzar una mayor remoción del Aroclor 1254. Por otro lado, la Figura 2b muestra la adsorción del Aroclor 1254 en función del tiempo, en ausencia de luz. Con este experimento se pudo confirmar que el TiO2 irradiado a 20 kGy adsorbe más Aroclor 1254 respecto de los otros TiO2. Como consecuencia de la irradiación, la superficie del TiO2 sufre modificaciones superficiales, ocasionando que el comportamiento adsortivo del TiO2 cambie dependiendo de la dosis irradiada (Cropper, 1962). En este trabajo para el caso del TiO2 irradiado a 20 kGy se alcanza la mayor degradación del Aroclor 1254, lo cual se asocia a la mayor adsorción encontrada en el TiO2 irradiado a esta dosis (resultados preliminares). Por lo que, se puede concluir preliminarmente que al someter a diferentes dosis de irradiación un material semiconductor, este adquiere propiedades adsortivas particulares, que pueden favorecer la adsorción de determinadas moléculas; y esto a su vez promover una mejor transferencia de masa hacia los sitios activos del fotocatalizador, provocando una degradación más rápida de los contaminantes.
Estudios realizados sobre el efecto de radiación gama en fotocatálisis con TiO2, han reportado que la aplicación de radiación gama con dosis cercanas a 28 kGy incrementan la actividad fotocatalítica del TiO2 debido a la aparición de “defectos” superficiales generados por la radiación, cuyo tipo y concentración es proporcional a la dosis de irradiación aplicada en el fotocatalizador (Kralchevska et al., 2012).
Otro estudio similar concluye que la aplicación de radiación en nanotubos de TiO2 incrementa su actividad fotocatalítica por el aumento de la generación de radicales hidroxilos (•OH) (Zhang et al., 2017). Estos datos apoyan la interpretación de los resultados representados en la Figuras 3, y a pesar de que la fuente de irradiación es diferente, se pudo lograr un efecto similar si se bombardea con electrones acelerados en dosis equivalentes (Chitose et al., 2003).
En la Tabla 2 se presentan las constantes de velocidad de pseudo primer orden para la degradación fotocatalítica de Aroclor 1254 con el TiO2 sin irradiar e irradiado. Se corrobora con estos resultados, que la degradación en el TiO2 irradiado es más rápido que el no irradiado.
Mineralización de Aroclor 1254
Se pudo determinar el aporte del Tritón X-100 y el Aroclor 1254 al COT global. Se encontró que el Tritón X-100 aporta con un 59,2% al COT global mientras que el Aroclor 1254 con el restante 40,8%, Figura 3a.
Después del tratamiento fotocatalítico con el TiO2 sin irradiar e irradiado, nuevamente se determinó el contenido de COT para identificar cual TiO2 permite una mayor mineralización.
Los resultados mostrados en la Figura 3b, indican que sobre TiO2 sin irradiar se obtuvo la remoción de COT mayor, tanto del COT global como de los aportantes al COT individual. Con el TiO2 irradiado solo se logra mineralizar 10,7% del Aroclor 1254 en 240 min de reacción. Para tiempos iguales de reacción, cuando se utilizó el TiO2 irradiado, se alcanzaron mayores remociones de COT, y fue con el TiO2 irradiado con dosis de 20 kGy que se logró la mayor remoción de COT asociada al Aroclor 1254 (58,2 %). Es posible observar mayor mineralización de Aroclor 1254 cuando se utilizó TiO2 irradiado; resultado igualmente destacado por Chitose et al. (2003), quienes reportaron la mejora en la mineralización de la materia orgánica cuando el fotocatalizador es irradiado.
CONCLUSIÓN
Se obtuvo que el mejor agente de transferencia de fase para el Aroclor 1254, en altas concentraciones, desde el aceite dieléctrico hacia la fase acuosa es el Tritón X-100.
Respecto al fotocatalizador utilizado, tanto del TiO2 sin irradiar (0 kGy) como del irradiado (20 y 60 kGy), permitió la degradación de Aroclor 1254 en fase acuosa. Sin embargo, con el TiO2 irradiado se logró una mayor degradación y mineralización, comparado con el TiO2 sin irradiar. Luego de 240 min de reacción, con el TiO2 irradiado a la dosis de 20 kGy se logró la mayor degradación (98,36%) y mineralización del Aroclor 1254 (63,7% de remoción del COT debido al Aroclor 1254). Se confirmó lo sugerido en estudios previos: el uso de radiaciones ionizantes, en este caso electrones acelerados, mejora las características fotocatalíticas del TiO2.
LISTA DE REFERENCIAS
American Public Health Association, A. P. H. A. (1995). Standard methods for the examination of water and wastewater. Washington, DC: American Public Health Association. (Vol. 21).
Atmaca, E., Das, Y. K., Yavuz, O., & Aksoy, A. (2019). An evaluation of the levels of organochlorine compounds (OCPs and PCBs) in cultured freshwater and wild sea fish eggs as an exposure biomarker for environmental contamination. Environmental Science and Pollution Research, 26(7), 7005–7012. https://doi.org/10.1007/s11356-019-04207-0
Camargo Moreno, C. E. (2014). Biotratamiento de Aceites Dieléctricos Usados (tesis de maestría). Universidad Nacional de Colombia. Obtenido de:
Chitose, N., Ueta, S., Seino, S., & Yamamoto, T. A. (2003). Radiolysis of aqueous phenol solutions with nanoparticles. 1. Phenol degradation and TOC removal in solutions containing TiO2 induced by UV, γ-ray and electron beams. Chemosphere, 50(8), 1007–1013. https://doi.org/10.1016/S0045-6535(02)00642-2
Cropper, W. H. (1962). Radiation Effects on the Reactivity of Solid Surfaces: Defects produced in solids by radiation fields can enter into chemical reactions on the surface. Science, 137(3534), 955–961. https://doi.org/10.1126/science.137.3534.955
Frías, M. M., & Gia, J. (2014). Descomposición del Bifenilo Policlorado (PCB) Aroclor 1260 en aceites dieléctricos, por radiólisis del agua, inducida por radiación gamma del isótopo de cobalto 60. Universidad Central Del Ecuador.
Fröschl, B., Stangl, G., & Niessner, R. (1997). Combination of micellar extraction and
GC-ECD for the determination of polychlorinated biphenyls (PCBs) in water.
Fresenius’ Journal of Analytical
Chemistry, 357(6), 743–746. https://doi.org/10.1007/s002160050241
Habibullah-Al-Mamun,
M., Ahmed, M. K., Islam, M. S., Tokumura, M., & Masunaga, S. (2019). Occurrence, distribution and possible
sources of polychlorinated biphenyls (PCBs) in the surface water from the Bay
of Bengal coast of Bangladesh. Ecotoxicology
and environmental safety, 167, 450-458.
https://doi.org/10.1016/j.ecoenv.2018.10.052
Huang, Q., &
Hong, C.-S. (2000). TiO2 photocatalytic degradation of PCBs in
soil-water systems containing fluoro surfactant. Chemosphere, 41(6), 871–879.
https://doi.org/10.1016/S0045-6535(99)00492-0
Izquierdo Condoy,
M., & Peña Pontón, E. (2016). Diseño
de sistemas de biodegradación aerobia y anaerobia a escala piloto para la
descontaminación de aceites dieléctricos con bifenilos policlorados (PCB’s) (tesis de pregrado). Escuela Politécnica
Nacional. Obtenido de: https://bibdigital.epn.edu.ec/handle/15000/16557
Kralchevska, R., Milanova, M., Tsvetkov, M., Dimitrov, D., & Todorovsky,
D. (2012). Influence of
gamma-irradiation on the photocatalytic activity of Degussa P25 TiO2.
Journal of Materials Science, 47(12),
4936–4945. https://doi.org/10.1007/s10853-012-6368-4
Law, R. J., &
Jepson, P. D. (2017). Europe’s insufficient pollutant remediation. Science, 356(6334), 148.
Lopera Posada, E., & Aguire Cardona, J. (2006). Purification of mineral insulating oil contaminated
with polychlorinated biphenyls (PCB’s). Dyna, 73(150), 75–88.
Nadarajan, R., Bakar, W. A. W. A., Ali, R., & Ismail, R.
(2017). Method for
polychlorinated biphenyls removal from mussels and its photocatalytic dechlorination. Applied
Catalysis B: Environmental, 218, 327–337. https://doi.org/10.1016/j.apcatb.2017.06.066
Parent, A. S.,
Pinson, A., Woods, N., Chatzi, C., Vaaga, C. E., Bensen, A.,
Westbrook, G. L. (2016). Early exposure to Aroclor
1254 in vivo disrupts the functional synaptic development of newborn
hippocampal granule cells. European
Journal of Neuroscience, 44(12), 3001–3010. https://doi.org/10.1111/ejn.13437
Wong, K. H., Tao,
S., Dawson, R., & Wong, P. K. (2004). Optimization of photocatalytic
oxidation of 2,2′,3,3′- tetrachlorobiphenyl. Journal of Hazardous Materials, 109(1–3), 149–155. https://doi.org/10.1016/j.jhazmat.2004.03.006
Xing, Y., Lu, Y.,
Dawson, R. W., Shi, Y., Zhang, H., Wang, T., Ren, H. (2005). A spatial temporal
assessment of pollution from PCBs in China. Chemosphere,
60(6 SPEC. ISS.), 731–739. https://doi.org/10.1016/j.chemosphere.2005.05.001
Zhang, Q., Ye, S.,
Chen, X., Song, X., Li, L., & Huang, X. (2017). Photocatalytic degradation
of ethylene using titanium dioxide nanotube arrays with Ag and reduced graphene
oxide irradiated by γ-ray radiolysis. Applied Catalysis B: Environmental, 203, 673–683. https://doi.org/10.1016/j.apcatb.2016.10.034
Notas
[1] Pontificia Universidad Católica del Ecuador, Escuela de Ciencias Químicas, Quito, Ecuador. (gabriel.almeida@epn.edu.ec; lmfernandez@puce.edu.ec; *correspondencia: pespinoza646@puce.edu.ec)
[2] Escuela
Politécnica Nacional, Departamento de Ciencias Nucleares, Quito, Ecuador. (gabriel.almeida@epn.edu.ec; william.villacis@epn.edu.ec)
[3] Universidad
Simón Bolívar, Departamento de Química, Caracas, Venezuela. (lfernandez@usb.ve)
[4] Laboratorio
de Análisis Químico de Contaminantes Orgánicos, Ministerio de Electricidad y
Recursos Naturales no Renovables, Quito, Ecuador. (cesar.castro@meer.gob.ec)
Notas de autor
pespinoza646@puce.edu.ec









